Clear Sky Science · pl
Prolinowo/serynowo-bogaty białkowy koiled-coil 1 łagodzi miażdżycę poprzez przebudowę metabolizmu tryptofanu pośredniczoną przez Akkermansia muciniphila
Jak drobnoustroje jelitowe i ukryty gen kształtują zdrowie serca
Miażdżyca — powolne zatykanie i bliznowacenie tętnic — zwykle przypisuje się wysokiemu poziomowi cholesterolu i zapaleniu. To badanie ujawnia zaskakującego, nowego uczestnika: mało poznany gen ludzki o nazwie PSRC1, który chroni tętnice, współdziałając z bakteriami jelitowymi lubiącymi śluz oraz cząsteczką powstającą z białek pokarmowych. Razem tworzą łańcuch zdarzeń sięgający od jelita grubego do komórek odpornościowych w ścianie naczyń, co może otworzyć drogę do precyzyjnych terapii dla osób o podwyższonym ryzyku chorób sercowo-naczyniowych.
Gen, który strzeże tętnic
Naukowcy skupili się na PSRC1, genie wcześniej wskazanym w dużych badaniach genetycznych jako powiązanym z chorobą wieńcową. Wcześniejsze prace na myszach sugerowały, że utrata PSRC1 pogarsza miażdżycę, częściowo przez zaburzenie mikrobiomu jelitowego. W tym badaniu zespół potwierdził, że myszy pozbawione PSRC1 rozwijały większe, bardziej kruche blaszki miażdżycowe mimo tego samego tłustego pokarmu co myszy kontrolne. Ich ściany tętnic wykazywały większe odkładanie tłuszczu, większe martwe strefy wewnątrz blaszek i mniej wspierającego kolagenu — wszystkie cechy charakterystyczne dla niebezpiecznych zmian podatnych na pęknięcie, które mogą wywołać zawały i udary.
Kiedy znika warstwa śluzu i kluczowy mikroorganizm
Aby sprawdzić, jak gen gospodarza może wpływać na mikroby w jelicie, naukowcy zbadali jelita myszy pozbawionych PSRC1. Stwierdzili, że ochronna warstwa śluzu pokrywająca jelito grube była cieńsza, z mniejszą liczbą komórek kubkowych produkujących śluz i osłabionymi połączeniami międzykomórkowymi. Uszkodzony barierowy nabłonek sprzyjał utracie korzystnych bakterii. Szczególnie mocno uszczuplono jeden szczep, Akkermansia muciniphila, która normalnie rozwija się, żywiąc się śluzem i pomagając go utrzymać. Ponieważ Akkermansia wiązana była z ochroną przed otyłością, zapaleniem i miażdżycą, jej zanik dawał wiarygodne wyjaśnienie związku między utratą PSRC1 a pogorszeniem choroby naczyń. 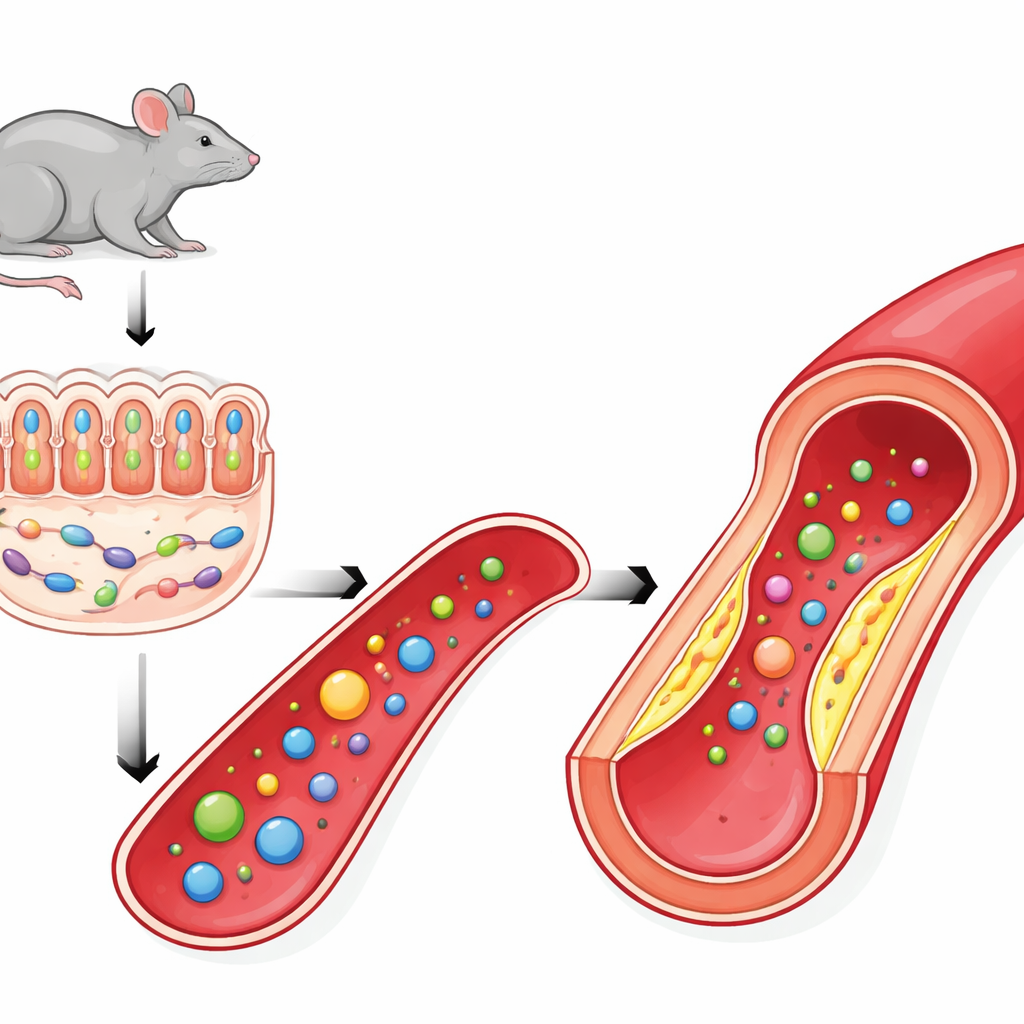
Od białka w diecie do sygnału ochronnego
Zespół skupił się następnie na tryptofanie — egzogennym aminokwasie z pożywienia, który bakterie jelitowe mogą przekształcać w różne cząsteczki sygnałowe. U myszy pozbawionych PSRC1 kilka związków pochodnych tryptofanu spadło we krwi, szczególnie indolilo-3-octowy kwas (IAA), produkt znany ze zdolności tłumienia zapalenia i stresu oksydacyjnego w modelach eksperymentalnych. IAA może aktywować receptor wewnątrz komórek odpornościowych zwany receptorem hydrokarbonów aromatycznych (AHR), który z kolei reguluje geny pomagające ograniczać zapalenie i śmierć komórek. U mutantów aktywność AHR i jej wskaźniki były obniżone w wątrobie, jelicie grubym i — co kluczowe — w makrofagach rezydujących w blaszkach miażdżycowych — komórkach odpornościowych pochłaniających tłuszcze, które w zależności od zachowania mogą stabilizować lub destabilizować blaszki.
Linia życia mikroba i cząsteczki dla komórek odpornościowych
Aby sprawdzić, czy przywrócenie Akkermansia lub IAA może uratować uszkodzony układ, badacze potraktowali myszy pozbawione PSRC1 żywymi lub zahartowanymi (zabitymi) preparatami Akkermansia po oczyszczeniu rodzimych bakterii antybiotykami. Tylko żywe bakterie istotnie zmniejszyły rozmiar blaszek, poprawiły ich strukturę i podniosły poziom IAA we krwi, jednocześnie przywracając aktywność AHR w makrofagach. Bezpośrednie podawanie IAA myszy również zmniejszyło obciążenie blaszek i uczyniło je bardziej stabilnymi — z mniejszą liczbą umierających makrofagów oraz większą ilością mięśni gładkich i kolagenu. W hodowlach komórkowych zwiększenie ekspresji PSRC1 w makrofagach podniosło poziom białka AHR przez spowolnienie jego rozkładu za pośrednictwem enzymu odznaczającego UCHL3, podczas gdy wyciszenie PSRC1 czyniło komórki bardziej podatnymi na śmierć pod wpływem stresu. Dodanie IAA odwracało ten sygnał pro-śmierci, ale tylko gdy AHR był aktywny, co wskazuje, że ochronny efekt IAA przebiega przez ten receptor.
Wskazówki od pacjentów
Naukowcy przyjrzeli się także próbkom krwi od osób poddawanych ocenie serca. W porównaniu z osobami bez znaczących zwężeń wieńcowych, pacjenci z chorobą wieńcową mieli niższe krążące stężenia IAA oraz niższą ekspresję PSRC1 i genu reagującego na AHR w komórkach odpornościowych krwi. Analiza statystyczna sugerowała, że wyższa ekspresja PSRC1 szła w parze z wyższym poziomem IAA i silniejszym sygnałem AHR, co powtarza wyniki z myszy i wspiera ideę istnienia wspólnej osi PSRC1–Akkermansia–IAA–AHR u ludzi.
Nowe ścieżki ku spersonalizowanym terapiom sercowym
W sumie praca kreśli obwód od jelita do tętnicy: PSRC1 pomaga utrzymać zdrową barierę śluzową i wspiera Akkermansia, która z kolei produkuje IAA z tryptofanu pokarmowego. IAA aktywuje AHR w makrofagach, ograniczając ich śmierć i pomagając utrzymać blaszki miażdżycowe mniejsze i bardziej stabilne. Gdy PSRC1 zostaje utracony, ten łańcuch słabnie — Akkermansia zanika, IAA spada, sygnalizacja AHR słabnie, a makrofagi częściej umierają, powiększając niebezpieczne jądro blaszek. 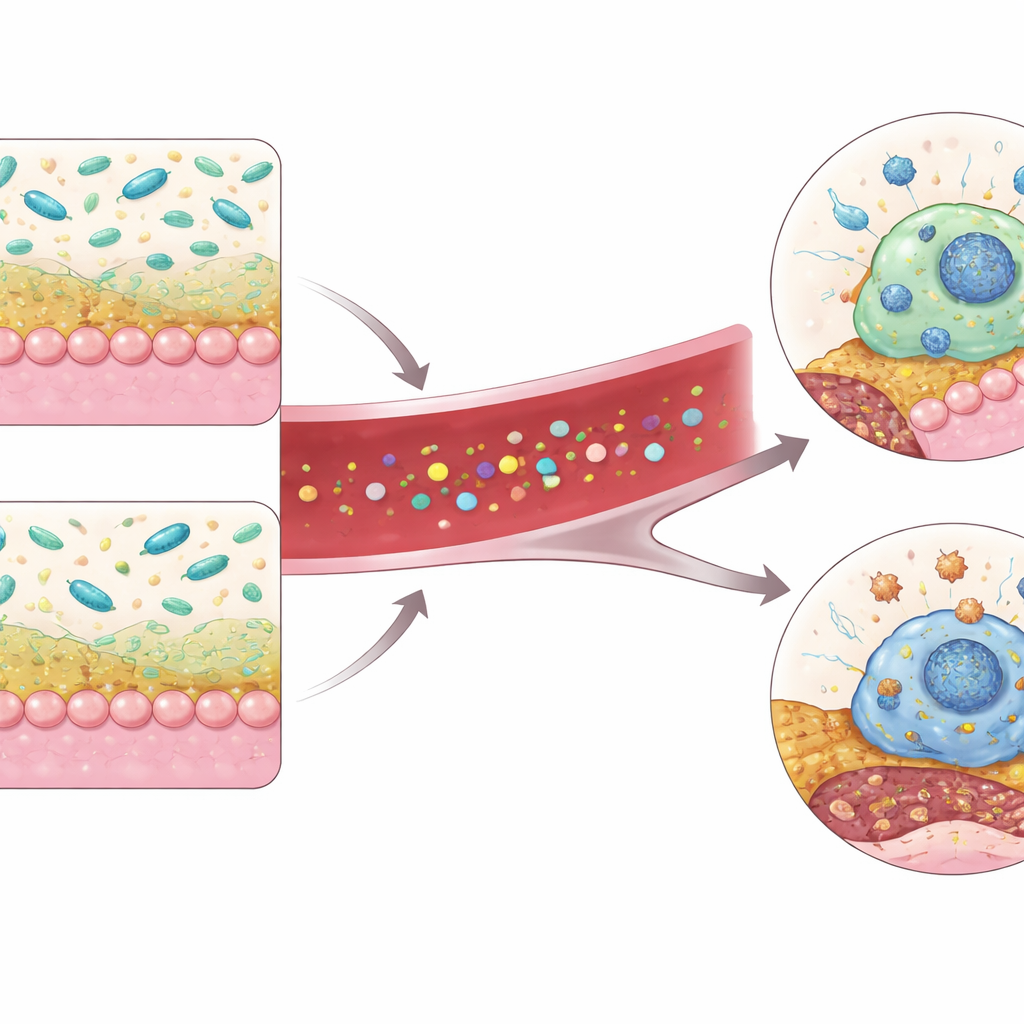
Cytowanie: Wu, Q., Hu, K., Wang, Q. et al. Proline/serine-rich coiled-coil 1 alleviates atherosclerosis via remodeling tryptophan metabolism mediated by Akkermansia muciniphila. Exp Mol Med 58, 848–863 (2026). https://doi.org/10.1038/s12276-026-01668-5
Słowa kluczowe: miażdżyca, mikrobiom jelitowy, metabolizm tryptofanu, Akkermansia muciniphila, indolilo-3-octowy kwas