Clear Sky Science · fr
Proline/serine-rich coiled-coil 1 atténue l’athérosclérose via le remodelage du métabolisme du tryptophane médié par Akkermansia muciniphila
Comment les microbes intestinaux et un gène méconnu façonnent la santé cardiaque
L’athérosclérose — l’encrassement et la cicatrisation progressifs des artères — est généralement imputée à un taux de cholestérol élevé et à l’inflammation. Cette étude met en lumière un acteur nouveau et surprenant : un gène humain peu étudié nommé PSRC1 qui protège les artères en collaborant avec un microbe intestinal adepte du mucus et avec une molécule issue des protéines alimentaires. Ensemble, ils forment une chaîne d’événements qui va du côlon aux cellules immunitaires logées dans la paroi artérielle, et pourraient ouvrir la voie à des traitements de précision pour les personnes à risque élevé de maladies cardiaques.
Un gène qui protège les artères
Les chercheurs se sont penchés sur PSRC1, un gène déjà signalé par de larges études génétiques comme associé à la maladie coronarienne. Des travaux antérieurs chez la souris suggéraient qu’une perte de PSRC1 aggrave l’athérosclérose, en partie en perturbant le microbiote intestinal. Ici, l’équipe confirme que des souris déficientes en PSRC1 développent des plaques plus volumineuses et plus fragiles dans leurs artères, malgré un régime hyperlipidique identique à celui des souris témoins. Les parois artérielles présentaient des dépôts lipidiques plus importants, de plus larges zones nécrotiques au sein des plaques et moins de collagène de soutien — autant de signes de lésions dangereuses susceptibles de se rompre et de déclencher infarctus et AVC.
Quand la couche de mucus et un microbe clé disparaissent
Pour comprendre comment un gène de l’hôte peut affecter les microbes intestinaux, les scientifiques ont examiné les intestins des souris déficientes en PSRC1. Ils ont constaté que la couche protectrice de mucus recouvrant le côlon était plus mince, avec moins de cellules à mucus (goblets) et des jonctions entre cellules intestinales affaiblies. Cette barrière endommagée favorise la perte de bactéries bénéfiques. Un microbe en particulier, Akkermansia muciniphila, qui se nourrit normalement de mucus tout en contribuant à le maintenir, était fortement appauvri. Étant donné le lien établi entre Akkermansia et la protection contre l’obésité, l’inflammation et l’athérosclérose, sa disparition fournit un lien plausible entre la perte de PSRC1 et l’aggravation de la maladie artérielle. 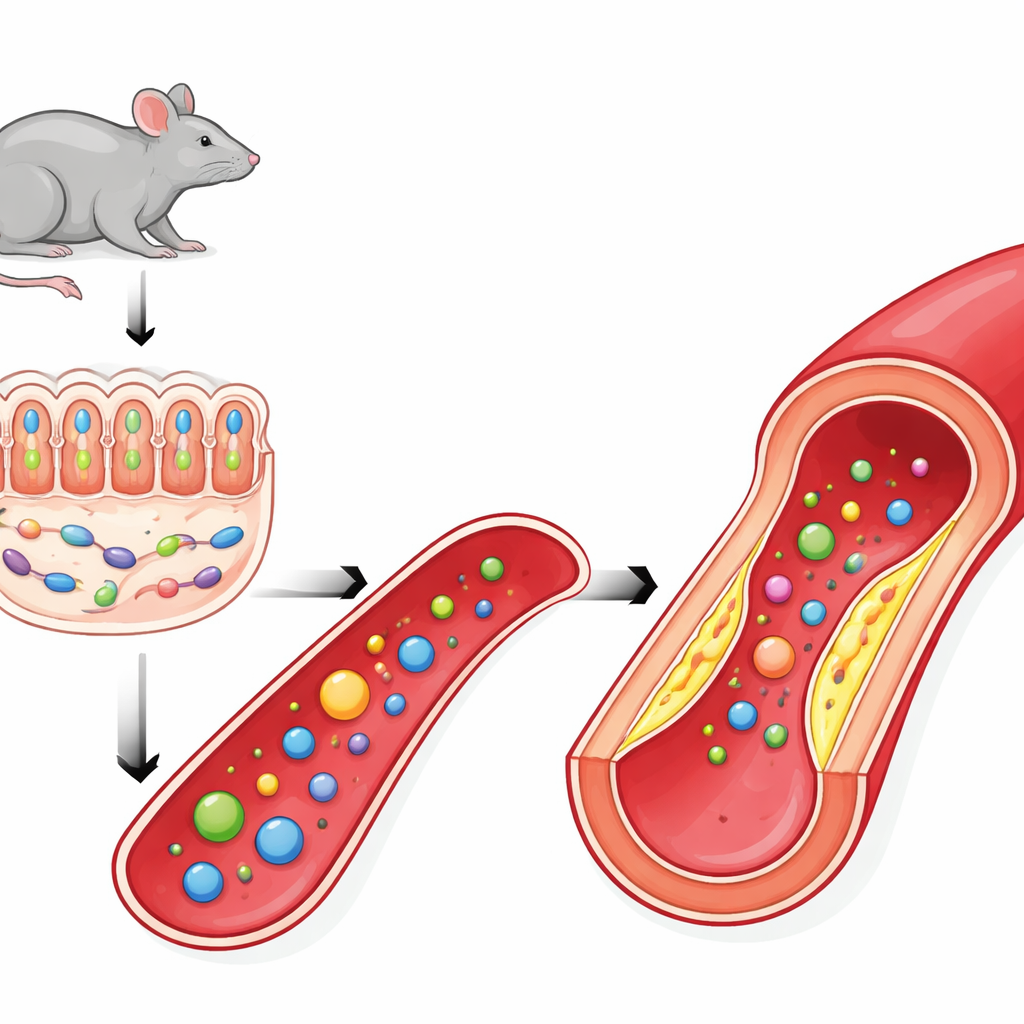
De la protéine alimentaire à un signal protecteur
L’équipe s’est ensuite intéressée au tryptophane, un acide aminé essentiel issu de l’alimentation que les bactéries intestinales peuvent transformer en divers messagers chimiques. Chez les souris déficientes en PSRC1, plusieurs composés dérivés du tryptophane diminuaient dans le sang, en particulier l’acide indole-3-acétique (IAA), un métabolite connu pour atténuer l’inflammation et le stress oxydatif dans des modèles expérimentaux. L’IAA peut activer un senseur intracellulaire des cellules immunitaires, le récepteur des hydrocarbures aromatiques (AHR), qui contrôle à son tour des gènes limitant l’inflammation et la mort cellulaire. Chez les souris mutantes, l’activité de l’AHR et ses marqueurs en aval étaient réduits dans le foie, le côlon et, de manière cruciale, dans les macrophages résidant dans les plaques — ces cellules immunitaires qui phagocytent les lipides et peuvent soit stabiliser soit déstabiliser les plaques selon leur comportement.
Une ligne de vie microbe–molécule pour les cellules immunitaires
Pour tester si restaurer Akkermansia ou l’IAA pouvait réparer le système altéré, les chercheurs ont traité des souris déficientes en PSRC1 avec Akkermansia vivante ou tuée à la chaleur après avoir éliminé leur flore native par antibiotiques. Seules les bactéries vivantes ont significativement réduit la taille des plaques, amélioré la structure des lésions et augmenté les taux sanguins d’IAA, tout en restaurant l’activité de l’AHR dans les macrophages. L’administration directe d’IAA aux souris a également réduit la charge en plaques et rendu celles-ci plus stables, avec moins de macrophages mourants et davantage de cellules musculaires lisses et de collagène. En culture cellulaire, l’augmentation de PSRC1 dans les macrophages augmentait la quantité de protéine AHR en ralentissant sa dégradation via une enzyme de dé-tagage appelée UCHL3, tandis que l’inhibition de PSRC1 rendait les cellules plus susceptibles de mourir sous stress. L’ajout d’IAA inversait ce signal pro-apoptotique, mais seulement si l’AHR était actif, indiquant que l’effet protecteur de l’IAA s’exerce via ce récepteur.
Indices tirés de patients humains
Les chercheurs ont aussi analysé des échantillons sanguins de personnes soumises à une évaluation cardiaque. Par rapport aux individus sans sténoses coronaires significatives, les patients atteints de maladie coronarienne présentaient des niveaux circulants d’IAA plus bas et une expression réduite de PSRC1 ainsi que d’un gène répondant à l’AHR dans leurs cellules immunitaires sanguines. Les analyses statistiques suggèrent qu’une expression plus élevée de PSRC1 va de pair avec des taux d’IAA plus élevés et une signalisation AHR plus forte, faisant écho aux résultats murins et soutenant l’idée d’un axe PSRC1–Akkermansia–IAA–AHR partagé chez l’homme.
Nouvelles pistes pour des thérapies cardiaques personnalisées
Dans l’ensemble, ce travail décrit un circuit reliant l’intestin et les artères : PSRC1 aide à préserver une barrière muqueuse saine et favorise Akkermansia, qui produit à partir du tryptophane alimentaire de l’IAA. L’IAA active l’AHR dans les macrophages, limitant leur mort et contribuant à maintenir les plaques artérielles plus petites et plus stables. Lorsque PSRC1 est perdu, cette chaîne s’affaiblit — Akkermansia décline, l’IAA chute, la signalisation AHR s’estompe et les macrophages meurent plus facilement, élargissant le noyau dangereux des plaques. 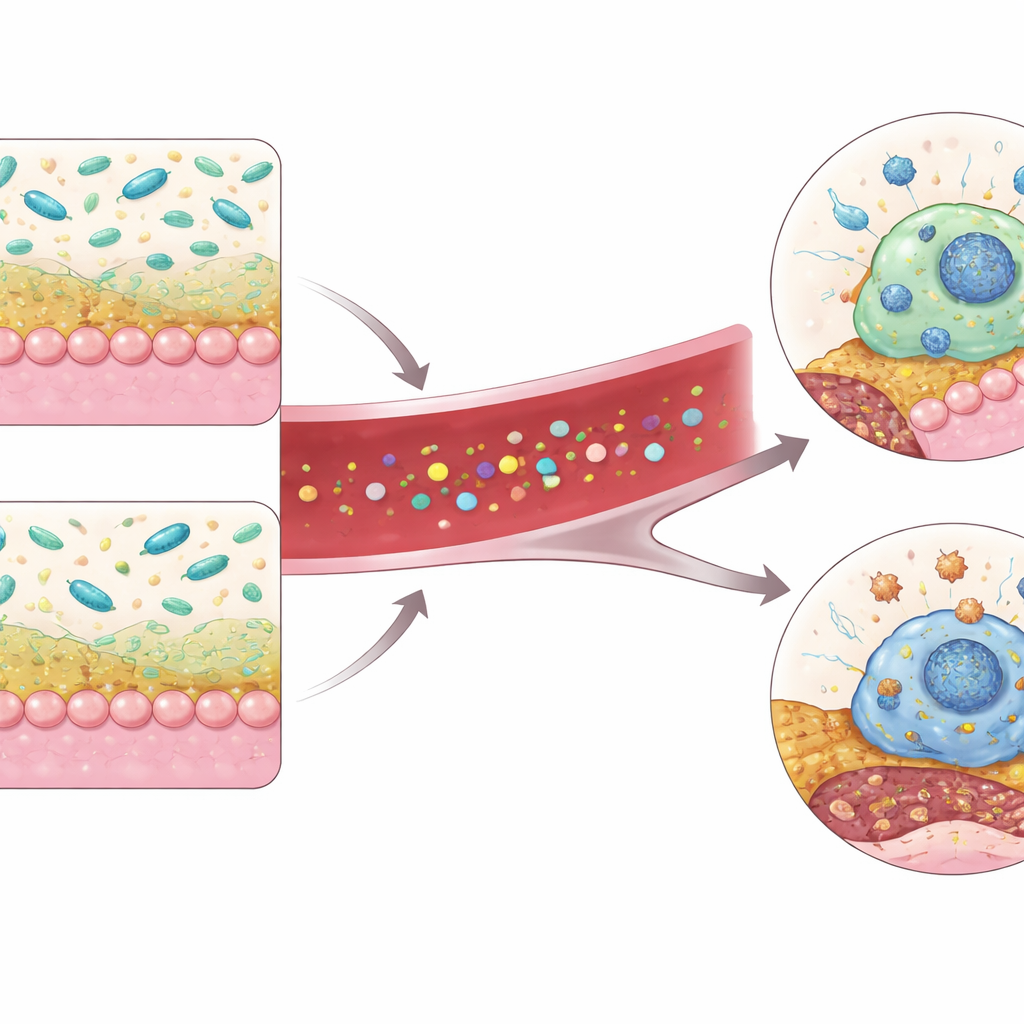
Citation: Wu, Q., Hu, K., Wang, Q. et al. Proline/serine-rich coiled-coil 1 alleviates atherosclerosis via remodeling tryptophan metabolism mediated by Akkermansia muciniphila. Exp Mol Med 58, 848–863 (2026). https://doi.org/10.1038/s12276-026-01668-5
Mots-clés: athérosclérose, microbiote intestinal, métabolisme du tryptophane, Akkermansia muciniphila, acide indole-3-acétique