Clear Sky Science · ru
Proline/serine-rich coiled-coil 1 ослабляет атеросклероз посредством ремоделирования метаболизма триптофана, опосредованного Akkermansia muciniphila
Как кишечные микробы и скрытый ген формируют здоровье сердца
Атеросклероз — медленное засорение и рубцевание артерий — обычно приписывают высокому уровню холестерина и воспалению. Это исследование выявляет неожиданный новый фактор: малоизученный человеческий ген PSRC1, который защищает артерии в сотрудничестве с микробом, живущим в слизи, и молекулой, образующейся из пищевого белка. Вместе они образуют цепочку событий от толстой кишки до иммунных клеток в стенках артерий и могут открыть путь к точечным методам лечения для людей с высоким риском сердечных заболеваний.
Ген, охраняющий артерии
Исследователи сосредоточились на PSRC1 — гене, ранее отмеченном в крупных генетических исследованиях как связанный с ишемической болезнью сердца. Предыдущие работы на мышах указывали, что потеря PSRC1 усугубляет атеросклероз, отчасти нарушая состав микробиоты кишечника. В этой работе команда подтвердила, что мыши без PSRC1 развивали более крупные, более хрупкие бляшки в артериях, несмотря на ту же самую диету с высоким содержанием жиров, что и контрольные животные. В их артериальных стенках присутствовали большие жировые отложения, расширенные некротические зоны внутри бляшек и меньше коллагена — все признаки опасных, склонных к разрыву поражений, которые могут вызвать инфаркты и инсульты.
Когда слизистая стенка и ключевой микроб исчезают
Чтобы понять, как ген хозяина может влиять на микробы в кишечнике, ученые изучили кишечник мышей, лишенных PSRC1. Они обнаружили, что защитный слой слизи, покрывающий толстую кишку, стал тоньше: уменьшилось число бокаловидных клеток, вырабатывающих слизь, и ослабли межклеточные контакты эпителия. Поврежденный барьер способствует утрате полезных бактерий. Особенно сильно истощилась одна бактерия — Akkermansia muciniphila, которая обычно питается слизью и при этом помогает поддерживать её целостность. Поскольку Akkermansia ассоциируется с защитой от ожирения, воспаления и атеросклероза, её исчезновение предложило правдоподобную связь между потерей PSRC1 и ухудшением состояния артерий. 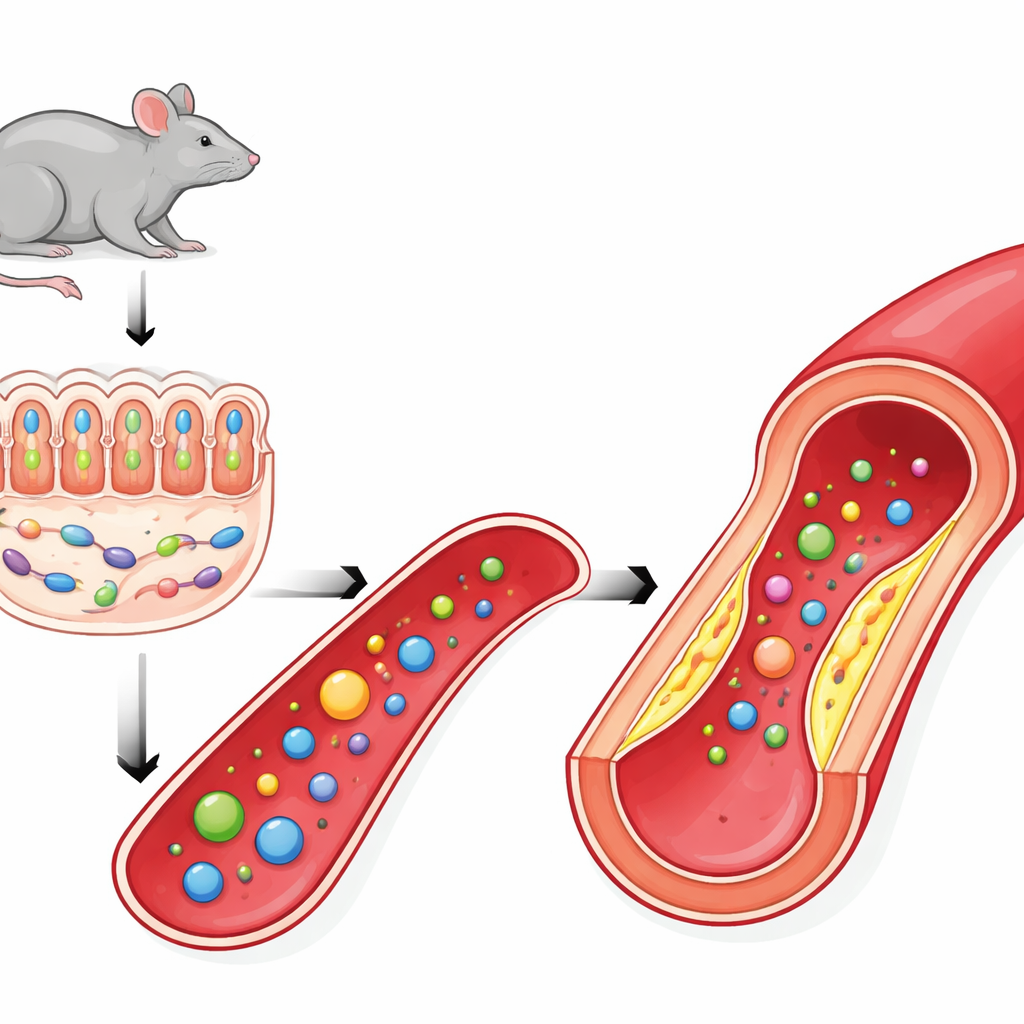
От пищевого белка к защитному сигналу
Далее команда сосредоточилась на триптофане — незаменимой аминокислоте из пищи, которую кишечные бактерии могут превращать в различные сигнальные молекулы. У мышей, лишенных PSRC1, в крови снизились уровни нескольких производных триптофана, особенно индол-3-уксусной кислоты (IAA) — продукта, известного своим способностью ослаблять воспаление и окислительный стресс в экспериментальных моделях. IAA способен активировать сенсор внутри иммунных клеток — рецептор арилуглеводородов (AHR), который, в свою очередь, регулирует гены, помогающие сдерживать воспаление и клеточную гибель. У мутантных мышей активность AHR и связанные с ним маркеры были снижены в печени, толстой кишке и, что важно, в макрофагах, находящихся в бляшках — иммунных клетках, поглощающих липиды и которые могут либо стабилизировать, либо дестабилизировать бляшки в зависимости от своего состояния.
Жизненная поддержка микроба и молекулы для иммунных клеток
Чтобы проверить, могут ли восстановление Akkermansia или IAA вернуть систему в рабочее состояние, исследователи лечили мышей без PSRC1 живыми или нагретыми (инактивированными) культурами Akkermansia после очистки их собственной микробной среды антибиотиками. Только живые бактерии заметно уменьшили размер бляшек, улучшили их структуру и повысили уровень IAA в крови, одновременно восстанавливая активность AHR в макрофагах. Прямое введение IAA также снизило тяжесть бляшек и сделало их более стабильными: уменьшилось число гибнущих макрофагов, а мышечная ткань и коллаген в бляшках увеличились. В клеточных культурах повышение уровня PSRC1 в макрофагах увеличивало содержание белка AHR за счёт замедления его разрушения через деубиквитинирующий фермент UCHL3, тогда как подавление PSRC1 делало клетки более уязвимыми к гибели под стрессом. Добавление IAA нейтрализовало этот про-смертный сигнал, но только при активном AHR, что указывает на то, что защитный эффект IAA реализуется через этот рецептор.
Подсказки от пациентов
Исследователи также проанализировали образцы крови у людей, проходивших обследование сердца. По сравнению с людьми без значимых коронарных стенозов, у пациентов с болезнью коронарных артерий уровень циркулирующего IAA и экспрессия PSRC1 и одного из AHR-ответных генов в их иммунных клетках крови были ниже. Статистический анализ показал, что более высокая экспрессия PSRC1 сопровождалась более высоким уровнем IAA и усиленной AHR-сигнализацией, что отзеркаливает результаты на мышах и поддерживает идею наличия общей оси PSRC1–Akkermansia–IAA–AHR у людей.
Новые пути к персонализированной терапии сердца
В совокупности работа рисует цепочку «кишечник — артерия»: PSRC1 помогает поддерживать здоровый слизистый барьер и способствует обитанию Akkermansia, которая, в свою очередь, производит IAA из пищевого триптофана. IAA активирует AHR в макрофагах, ограничивая их гибель и способствуя тому, чтобы артериальные бляшки были меньше и стабильнее. При потере PSRC1 эта цепочка ослабевает — Akkermansia уменьшается, IAA падает, AHR-сигнализация снижается, и макрофаги гибнут легче, расширяя опасное некротическое ядро бляшек. 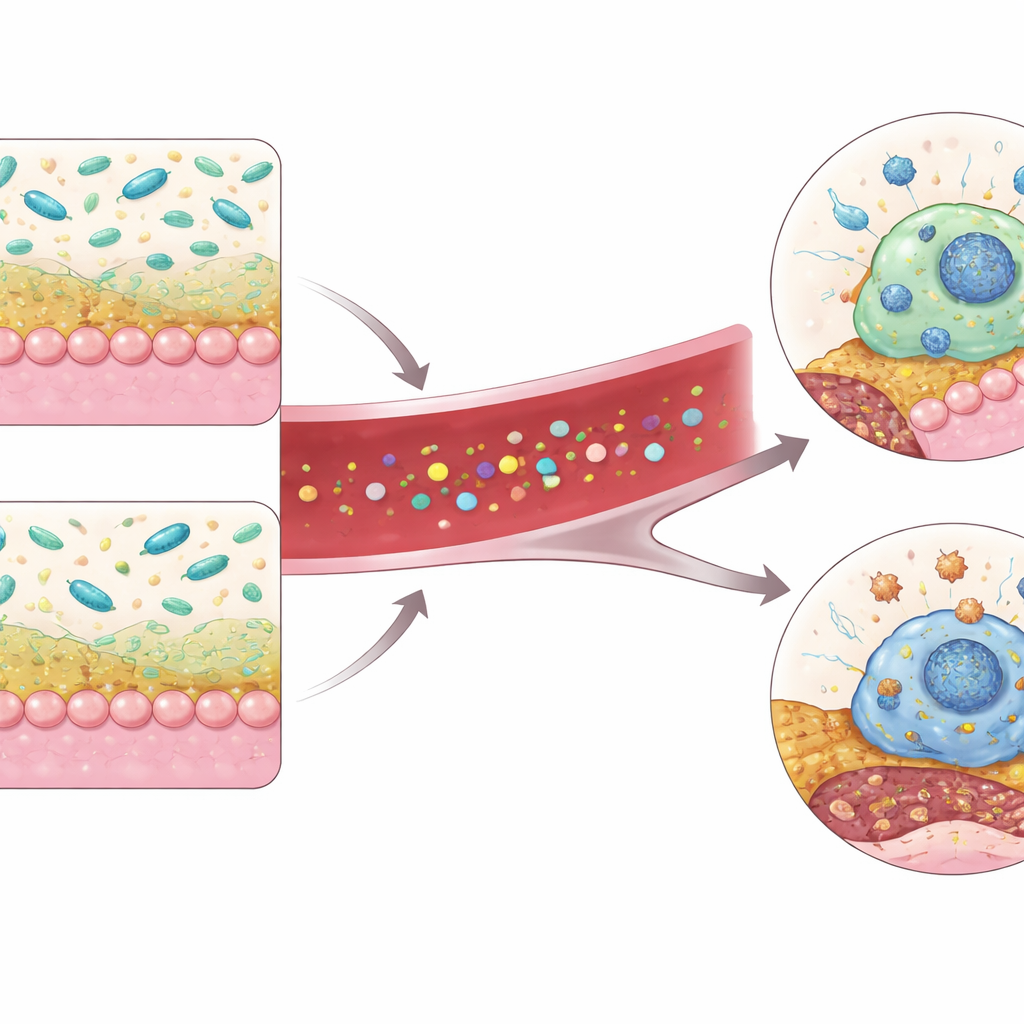
Цитирование: Wu, Q., Hu, K., Wang, Q. et al. Proline/serine-rich coiled-coil 1 alleviates atherosclerosis via remodeling tryptophan metabolism mediated by Akkermansia muciniphila. Exp Mol Med 58, 848–863 (2026). https://doi.org/10.1038/s12276-026-01668-5
Ключевые слова: атеросклероз, микробиом кишечника, метаболизм триптофана, Akkermansia muciniphila, индол-3-уксусная кислота