Clear Sky Science · zh
依赖 HMGCS2 的 β-OHB/H3K9bhb 改善阿尔茨海默病中的突触可塑性与认知
为何能量分子对记忆至关重要
阿尔茨海默病最为人所知的是记忆丧失和脑组织损伤,但这项研究关注疾病中不那么熟悉的一面:大脑的燃料与基因开关如何相互作用。研究人员探索了一种天然的燃料分子(通常可通过生酮饮食或禁食提升)如何改变包装 DNA 的组蛋白上的化学标记,从而帮助修复神经细胞之间支撑学习和记忆的微小连接。他们的工作指向一种基于代谢的新策略,用以支持阿尔茨海默病患者的大脑功能。
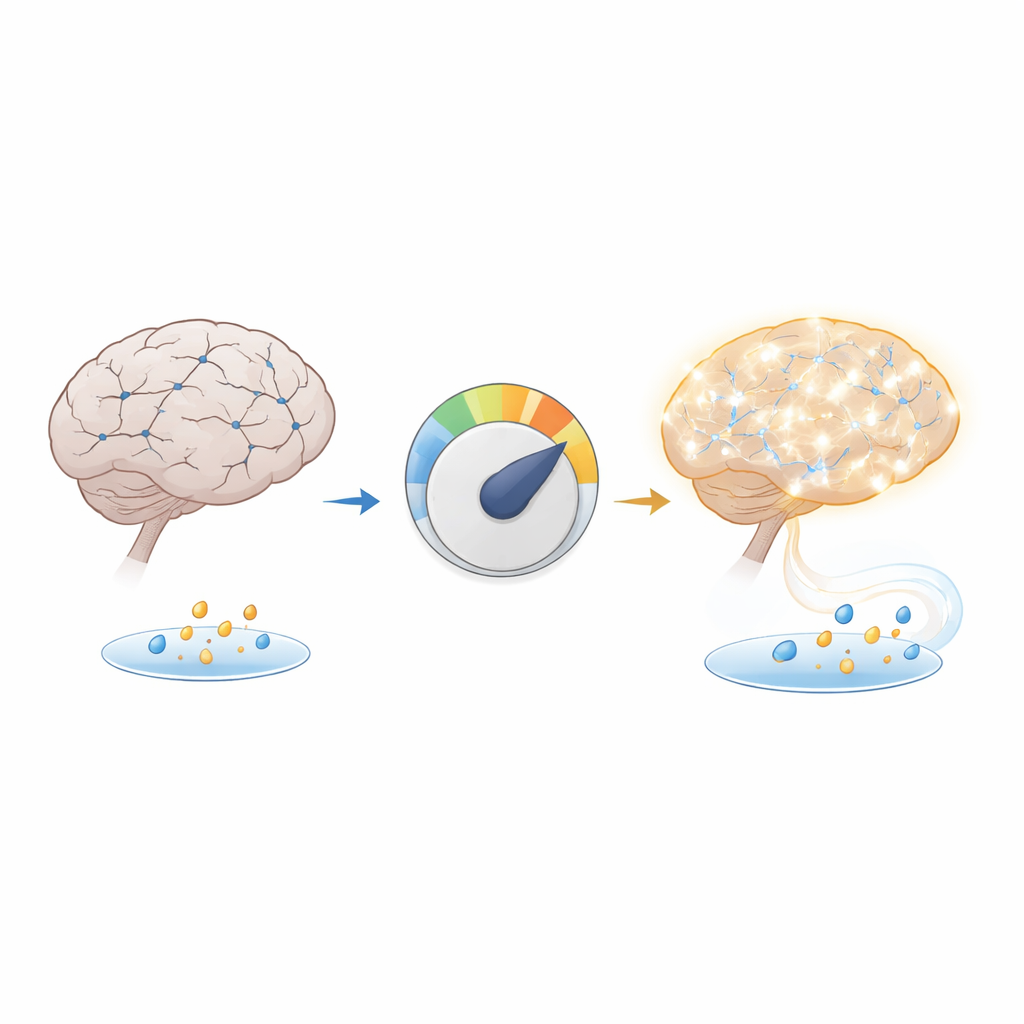
阿尔茨海默大脑中的一个隐藏短缺
团队将注意力集中在 β-羟基丁酸(β-hydroxybutyrate)——一种在机体燃烧脂肪时产生的小分子——以及与之相关的组蛋白化学标记 H3K9bhb。该标记倾向于“打开”某些 DNA 区域,使附近基因得以表达。研究人员在一种广泛使用的阿尔茨海默小鼠模型和阿尔茨海默患者的大脑组织中检测到,β-羟基丁酸和 H3K9bhb 水平均降低,尤以海马体(关键记忆中枢)为甚。血液中该分子的水平看似正常,提示问题并非全身性的燃料短缺,而是大脑内制造或利用该燃料的特定障碍。
为基因开关供能以保护神经连线
随后,研究者对中年阿尔茨海默小鼠连续数月补充 β-羟基丁酸。此处理提高了脑内该分子的水平并增强了 H3K9bhb 标记,主要出现在神经元而非支持细胞上。通过基因组范围和靶向分析,他们显示这些标记在参与轴突引导(传递信号的长纤维)以及构建和维持突触的基因启动区更为丰富。那些在阿尔茨海默小鼠中被抑制的基因重新被激活。显微镜观察证实,健康轴突和突触的标志物增加,神经元分枝和微小棘突(新连接的结构基础)增多。
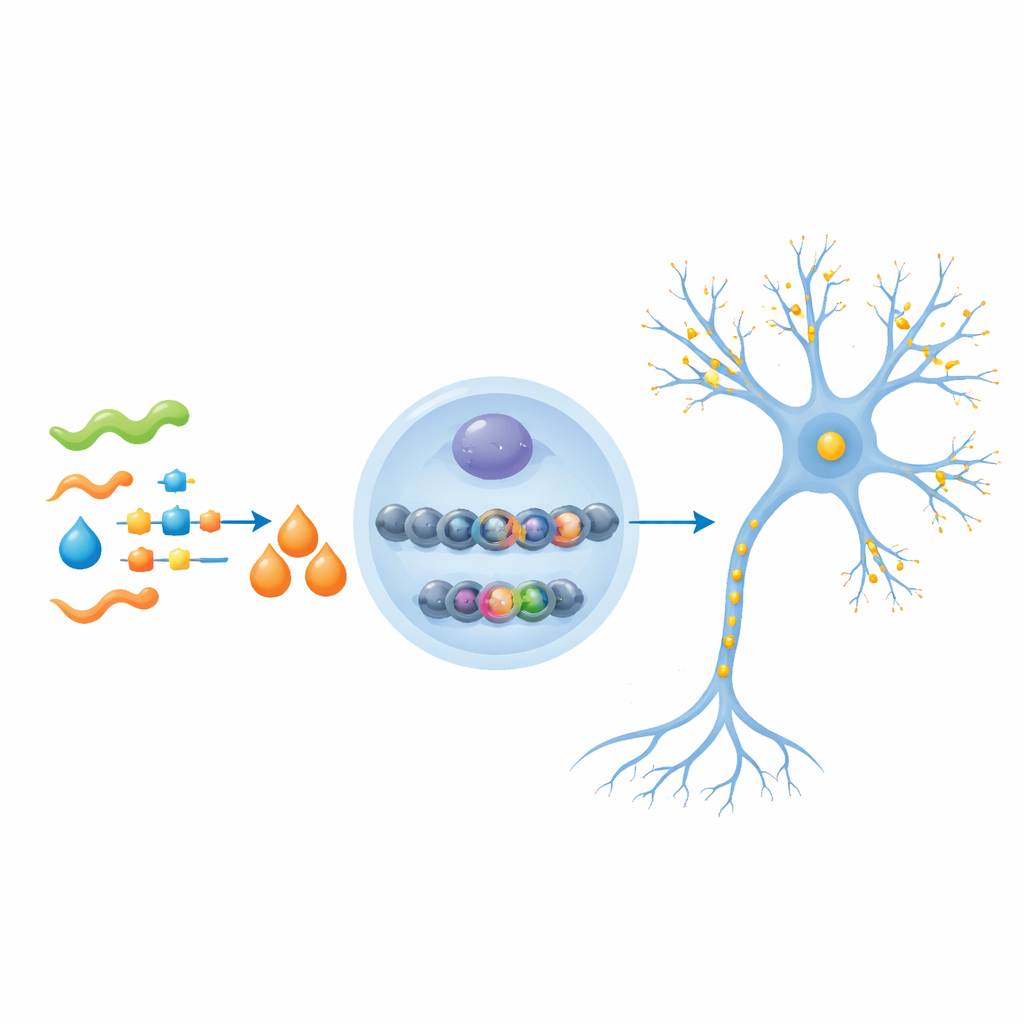
从更强的突触到更敏锐的记忆
因为神经元间的通讯在很大程度上依赖特定受体蛋白,团队重点考察了 NMDA 受体家族和一种名为 Syn1 的突触蛋白。在阿尔茨海默小鼠中,这些蛋白及其基因活性均被抑制,相应的 DNA 区域也携带较少的 H3K9bhb 标记。β-羟基丁酸治疗恢复了这些化学标记以及这些关键突触成分的表达。行为学测试得出类似结论:经治疗的小鼠更快学会在水迷宫中找到隐蔽平台,数日后记忆更持久,能区分新旧物体,并在基于恐惧的记忆任务中表现更强。重要的是,它们的游泳能力和整体运动未见变化,表明改善为认知层面的而非运动能力的改变。
设定燃料水平的大脑酶
研究接着询问为何 β-羟基丁酸会减少。该分子由细胞内一小组酶合成,其中一项关键酶为 HMGCS2。通过分析公开的人类数据集、小鼠大脑、暴露于阿尔茨海默相关蛋白片段的培养脑细胞以及来自阿尔茨海默小鼠的原代神经元,研究者发现 HMGCS2 持续下降。他们追溯到转录因子 PPARα 的下降,后者通常促进 HMGCS2 基因。当他们在神经元或阿尔茨海默小鼠大脑中人为增加 HMGCS2 时,β-羟基丁酸和 H3K9bhb 水平上升,突触相关基因重新激活,突触结构改善,多项记忆行为表现向健康小鼠靠拢。
围绕大脑燃料与基因控制重塑治疗思路
综合来看,研究勾勒出一条事件链:阿尔茨海默大脑中 HMGCS2 降低导致 β-羟基丁酸生成减少,相关基因上的 H3K9bhb 标记减少,突触减弱并引发认知衰退。恢复 β-羟基丁酸水平——无论是直接补充还是通过提升 HMGCS2——可重建这些化学标记,恢复对轴突与突触重要基因的表达,并改善小鼠的学习与记忆。对非专业读者而言,这一信息表明阿尔茨海默不仅关乎斑块与缠结,还涉及大脑如何管理能量与控制关键基因的可及性。针对这一“燃料到基因”通路,或可作为现有方法的补充,并激发通过从内部稳定大脑连线的新治疗思路。
引用: Yu, H., Wang, F., Yuan, Jq. et al. HMGCS2-dependent β-OHB/H3K9bhb ameliorates synaptic plasticity and cognition in Alzheimer’s disease. Exp Mol Med 58, 813–831 (2026). https://doi.org/10.1038/s12276-026-01664-9
关键词: 阿尔茨海默病, 生酮代谢, 突触可塑性, 表观遗传调控, β-羟基丁酸