Clear Sky Science · de
HMGCS2‑abhängiges β‑OHB/H3K9bhb verbessert synaptische Plastizität und Kognition bei Alzheimer‑Krankheit
Warum Energiemoleküle für das Gedächtnis wichtig sind
Die Alzheimer‑Krankheit ist vor allem für Gedächtnisverlust und geschädigtes Hirngewebe bekannt, doch diese Studie beleuchtet eine weniger bekannte Seite der Erkrankung: wie Hirn‑Treibstoff und Gen‑Schalter zusammenwirken. Die Forschenden untersuchen, wie ein natürliches Treibstoffmolekül, das durch ketogene Diäten oder Fasten erhöht werden kann, chemische Markierungen an DNA‑verpackenden Proteinen verändert und dadurch die winzigen Verbindungen zwischen Nervenzellen, die Lernen und Erinnerung ermöglichen, wiederherstellen hilft. Ihre Arbeit weist auf eine neue, am Stoffwechsel orientierte Strategie zur Unterstützung der Gehirnfunktion bei Alzheimer‑Krankheit hin.
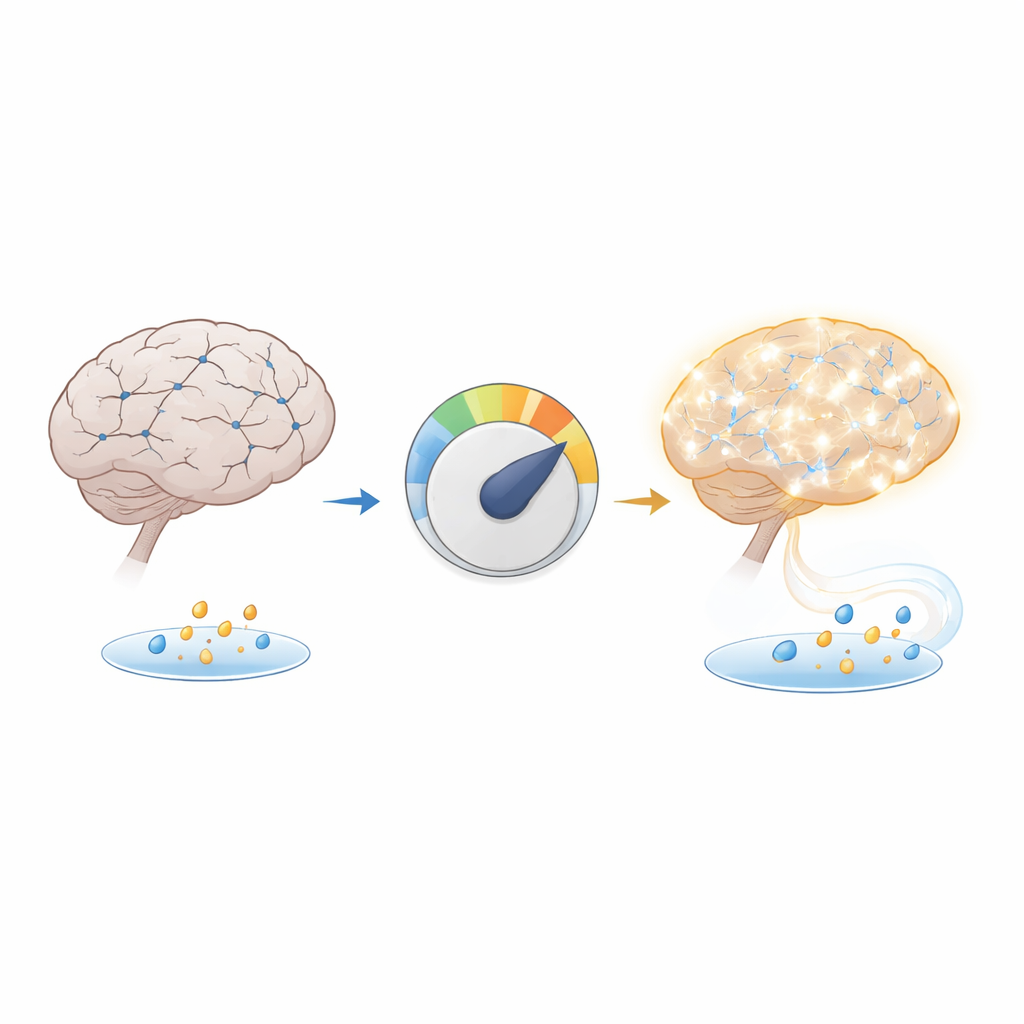
Ein versteckter Mangel im Alzheimer‑Gehirn
Das Team konzentrierte sich auf β‑Hydroxybutyrat, ein kleines Molekül, das bei der Fettverbrennung entsteht, und auf eine damit verwandte chemische Markierung an Histonproteinen, die die DNA organisieren. Diese Markierung, H3K9bhb genannt, sorgt dafür, dass Abschnitte der DNA „aufgeklappt“ werden, sodass nahegelegene Gene aktiv werden können. Beim Vergleich von Hirngewebe eines weit verbreiteten Alzheimer‑Mausmodells und von Menschen mit Alzheimer stellten die Wissenschaftler fest, dass die Konzentrationen von β‑Hydroxybutyrat und H3K9bhb vermindert waren, besonders im Hippocampus, einem wichtigen Gedächtniszentrum. Die Blutwerte des Moleküls wirkten normal, was darauf hindeutet, dass das Problem nicht ein allgemeiner Treibstoffmangel im ganzen Körper ist, sondern ein spezifisches Versagen, dieses Treibstoffmolekül im Gehirn zu produzieren oder zu nutzen.
Gene schalten mit Treibstoff zum Schutz der Nervenverbindungen
Als Nächstes verabreichten die Forschenden β‑Hydroxybutyrat über mehrere Monate an mittelalte Alzheimer‑Mäuse. Diese Behandlung erhöhte den Gehalt des Moleküls im Gehirn und stärkte die H3K9bhb‑Marken, überwiegend in Neuronen statt in Stützzellen. Mithilfe genomweiter und gezielter Analysen zeigten sie, dass diese Markierungen vermehrt an den Startregionen von Genen auftraten, die an der Führung von Axonen (den langen Fasern, die Signale weiterleiten) sowie am Aufbau und Betrieb von Synapsen beteiligt sind. Diese Gene, die bei den Alzheimer‑Mäusen zuvor herunterreguliert waren, wurden wieder aktiver. Mikroskopische Untersuchungen bestätigten, dass Marker gesunder Axone und Synapsen zunahmen und dass Nervenzellen mehr Verzweigungen und kleine Dornen (Spines) ausbildeten, die die strukturelle Grundlage neuer Verbindungen bilden.
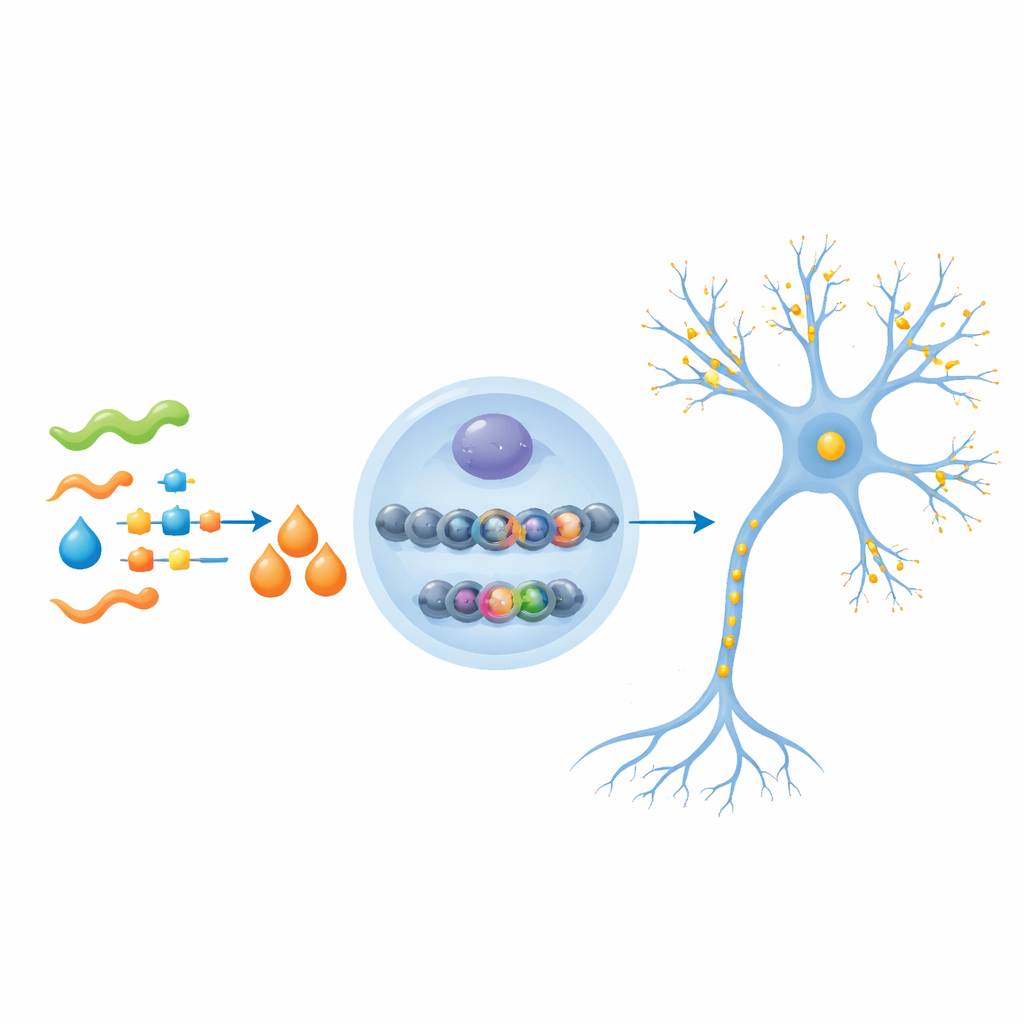
Von stärkeren Synapsen zu schärferem Gedächtnis
Da die Kommunikation zwischen Neuronen stark von bestimmten Rezeptorproteinen abhängt, untersuchte das Team insbesondere die NMDA‑Rezeptorfamilie und ein synaptisches Protein namens Syn1. Bei den Alzheimer‑Mäusen waren diese Proteine und ihre Genaktivität reduziert, und die entsprechenden DNA‑Regionen trugen weniger H3K9bhb‑Marken. Die Behandlung mit β‑Hydroxybutyrat stellte sowohl die chemischen Markierungen als auch die Expression dieser wichtigen synaptischen Komponenten wieder her. Verhaltenstests ergaben ein ähnliches Bild: Behandelte Mäuse lernten die Lage einer versteckten Plattform in einem Wasserlabyrinth schneller, erinnerten sich Tage später besser daran, unterschieden neue Objekte von vertrauten und zeigten stärkere angstbezogene Gedächtnisleistungen. Wichtig war, dass sich ihre Schwimmfähigkeit und die allgemeine Beweglichkeit nicht veränderten, was darauf hindeutet, dass die Verbesserungen kognitiver und nicht physischer Natur waren.
Das Hirnenzym, das den Treibstoffpegel bestimmt
Die Studie fragte dann, warum β‑Hydroxybutyrat überhaupt reduziert ist. Das Molekül wird in Zellen von einer kleinen Enzymgruppe hergestellt, darunter ein Enzym namens HMGCS2, das einen entscheidenden Schritt kontrolliert. Durch die Analyse öffentlicher Human‑Datensätze, von Mausgehirnen, kultivierten Hirnzellen, die Alzheimer‑verwandten Proteinfragmenten ausgesetzt wurden, und Primärneuronen aus Alzheimer‑Mäusen fanden die Forschenden, dass HMGCS2 konstant vermindert war. Sie führten dies auf einen Rückgang eines Transkriptionsfaktors, PPARα, zurück, der normalerweise das HMGCS2‑Gen hochreguliert. Als sie HMGCS2 künstlich in Neuronen oder im Gehirn von Alzheimer‑Mäusen erhöhten, stiegen β‑Hydroxybutyrat und H3K9bhb, synapsenbezogene Gene wurden wieder aktiviert, synaptische Strukturen verbesserten sich und die Gedächtnisleistung in mehreren Aufgaben näherte sich der gesunder Mäuse an.
Behandlung neu denken: Hirntreibstoff und Genkontrolle
In der Zusammenfassung skizzieren die Ergebnisse eine Ereigniskette: Vermindertes HMGCS2 in Alzheimer‑Gehirnen führt zu geringerer β‑Hydroxybutyrat‑Produktion, weniger H3K9bhb‑Marken auf Genen, die Synapsen stützen, schwächeren Synapsen und kognitivem Abbau. Die Wiederherstellung der β‑Hydroxybutyrat‑Spiegel — entweder direkt oder durch Anheben von HMGCS2 — baut diese chemischen Markierungen wieder auf, belebt die Genaktivität, die für Axone und Synapsen wichtig ist, und verbessert Lernen und Gedächtnis bei Mäusen. Für die interessierte Laienperspektive lautet die Botschaft, dass Alzheimer nicht nur Plaques und Verfilzungen betrifft, sondern auch die Art und Weise, wie das Gehirn seine Energie verwaltet und den Zugang zu kritischen Genen steuert. Die gezielte Beeinflussung dieses „Treibstoff‑zu‑Gen“-Wegs könnte bestehende Ansätze ergänzen und neue Behandlungsstrategien inspirieren, die das Gehirn von innen heraus stabilisieren.
Zitation: Yu, H., Wang, F., Yuan, Jq. et al. HMGCS2-dependent β-OHB/H3K9bhb ameliorates synaptic plasticity and cognition in Alzheimer’s disease. Exp Mol Med 58, 813–831 (2026). https://doi.org/10.1038/s12276-026-01664-9
Schlüsselwörter: Alzheimer‑Krankheit, ketogener Stoffwechsel, synaptische Plastizität, epigenetische Regulation, Beta‑Hydroxybutyrat