Clear Sky Science · es
La β-OHB/H3K9bhb dependiente de HMGCS2 mejora la plasticidad sináptica y la cognición en la enfermedad de Alzheimer
Por qué las moléculas energéticas importan para la memoria
La enfermedad de Alzheimer es más conocida por la pérdida de memoria y el deterioro del tejido cerebral, pero este estudio examina un aspecto menos familiar de la enfermedad: cómo interactúan el combustible del cerebro y los interruptores génicos. Los investigadores exploran cómo una molécula de combustible natural, cuya presencia suele incrementarse con dietas cetogénicas o el ayuno, puede cambiar etiquetas químicas en las proteínas que empaquetan el ADN y, a su vez, ayudar a restaurar las diminutas conexiones entre las neuronas que sustentan el aprendizaje y la memoria. Su trabajo apunta a una nueva estrategia basada en el metabolismo para apoyar la función cerebral en la enfermedad de Alzheimer.
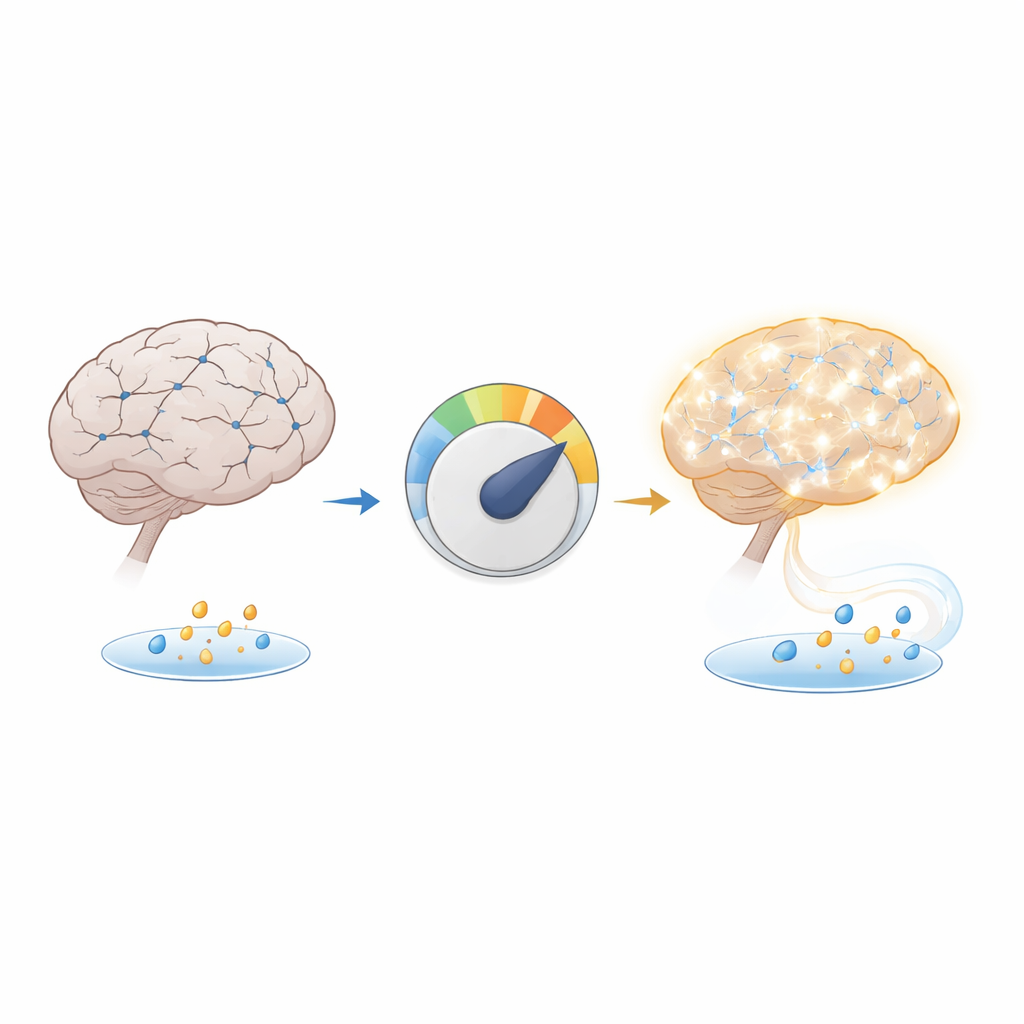
Una escasez oculta en el cerebro con Alzheimer
El equipo se centró en el β-hidroxibutirato, una pequeña molécula producida cuando el organismo quema grasa, y en una etiqueta química relacionada colocada en las histonas, proteínas que ayudan a organizar el ADN. Esta etiqueta, llamada H3K9bhb, tiende a "abrir" tramos de ADN para que los genes próximos puedan activarse. Al examinar tejido cerebral de un modelo de ratón ampliamente usado para el Alzheimer y de personas que padecieron la enfermedad, los científicos encontraron que los niveles de β-hidroxibutirato y de H3K9bhb estaban ambos reducidos, especialmente en el hipocampo, un centro clave de la memoria. Los niveles sanguíneos de la molécula parecían normales, lo que sugiere que el problema no es una carencia de combustible a nivel corporal, sino un fallo específico en producir o utilizar este combustible dentro del cerebro.
Alimentar los interruptores génicos para proteger el cableado neuronal
A continuación, los investigadores administraron β-hidroxibutirato a ratones con Alzheimer de mediana edad durante varios meses. Este tratamiento elevó el nivel de la molécula en el cerebro y aumentó las marcas H3K9bhb, principalmente en neuronas más que en células de soporte. Mediante análisis genómicos y dirigidos, mostraron que estas marcas se volvieron más abundantes en las regiones iniciales de genes implicados en la orientación de los axones (las fibras largas que conducen señales) y en la formación y funcionamiento de las sinapsis. Esos genes, previamente reprimidos en los ratones con Alzheimer, se activaron de nuevo. La microscopía confirmó que aumentaron marcadores de axones y sinapsis saludables y que las neuronas desarrollaron más ramas y pequeñas espinas, la base estructural de nuevas conexiones.
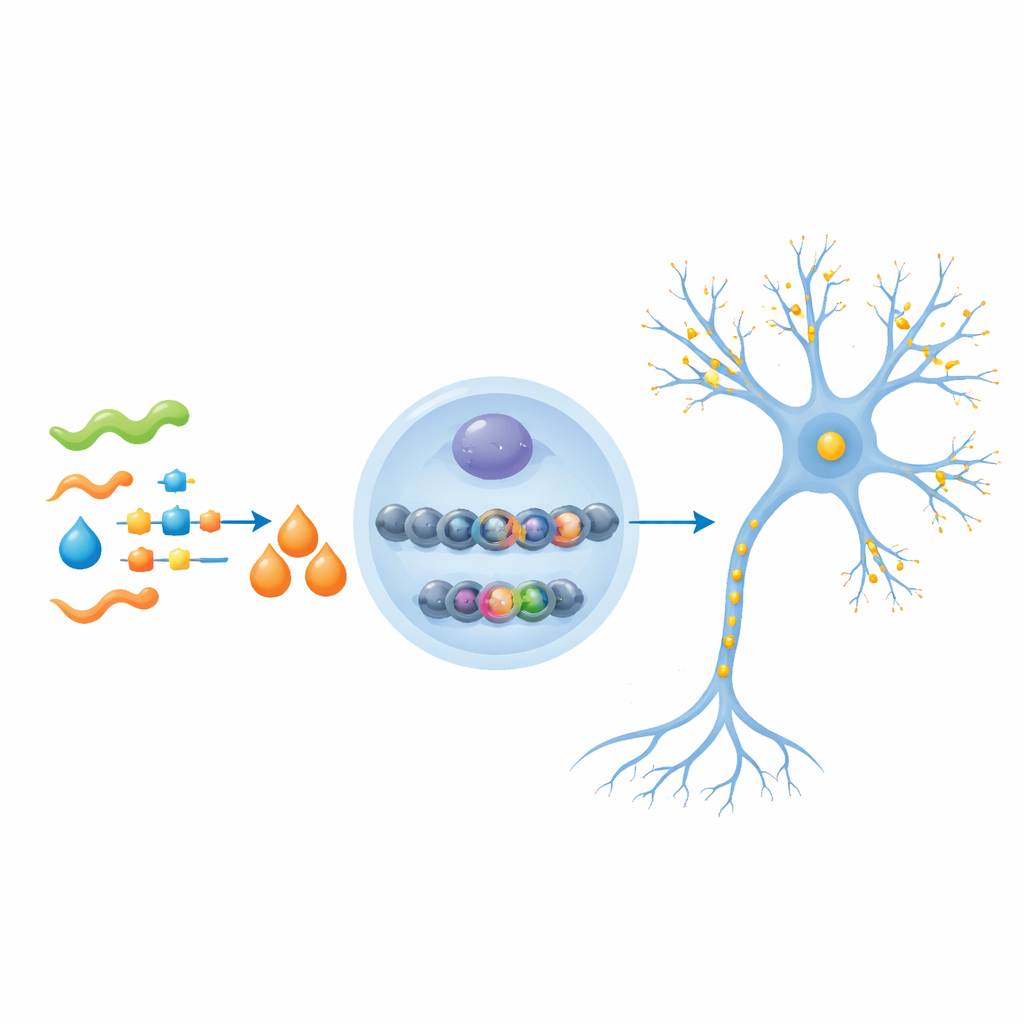
De sinapsis más fuertes a una memoria más aguda
Puesto que la comunicación entre neuronas depende en gran medida de ciertos receptores proteicos, el equipo examinó de cerca la familia de receptores NMDA y una proteína sináptica llamada Syn1. En los ratones con Alzheimer, estas proteínas y su actividad génica estaban disminuidas, y las regiones de ADN correspondientes presentaban menos marcas H3K9bhb. El tratamiento con β-hidroxibutirato restauró tanto las etiquetas químicas como la expresión de estos componentes sinápticos clave. Las pruebas comportamentales contaron una historia similar: los ratones tratados aprendieron más rápido la ubicación de una plataforma escondida en un laberinto acuático, la recordaron mejor días después, distinguieron objetos nuevos de los familiares y mostraron una memoria basada en el miedo más fuerte. Es importante que su capacidad de nadar y el movimiento general no cambiaron, lo que indica que las mejoras fueron cognitivas y no físicas.
La enzima cerebral que regula el nivel de combustible
El estudio preguntó después por qué el β-hidroxibutirato es bajo en primer lugar. La molécula se sintetiza en las células mediante un pequeño conjunto de enzimas, incluida una llamada HMGCS2 que controla un paso clave. Al analizar conjuntos de datos humanos públicos, cerebros de ratón, células cerebrales en cultivo expuestas a fragmentos proteicos relacionados con el Alzheimer y neuronas primarias de ratones con Alzheimer, los investigadores hallaron que HMGCS2 estaba consistentemente reducido. Rastrearon esto hasta una caída en un factor de transcripción, PPARα, que normalmente incrementa el gen HMGCS2. Cuando aumentaron artificialmente HMGCS2 en neuronas o en los cerebros de ratones con Alzheimer, subieron los niveles de β-hidroxibutirato y de H3K9bhb, se reactivaron genes relacionados con las sinapsis, mejoraron las estructuras sinápticas y el rendimiento en varias tareas de memoria se acercó al de ratones sanos.
Reformular el tratamiento en torno al combustible cerebral y el control génico
En conjunto, los hallazgos delinean una cadena de eventos: la reducción de HMGCS2 en cerebros con Alzheimer conduce a una menor producción de β-hidroxibutirato, menos marcas H3K9bhb en genes que sostienen las sinapsis, sinapsis más débiles y deterioro cognitivo. Restaurar los niveles de β-hidroxibutirato —ya sea directamente o mediante el aumento de HMGCS2— reconstruye estas marcas químicas, revive la actividad génica importante para axones y sinapsis y mejora el aprendizaje y la memoria en ratones. Para un observador no especialista, el mensaje es que el Alzheimer no solo trata de placas y ovillos, sino también de cómo el cerebro gestiona su energía y controla el acceso a genes críticos. Apuntalar esta vía "combustible-a-genes" podría complementar los enfoques existentes e inspirar nuevos tratamientos que funcionen estabilizando el cableado cerebral desde dentro.
Cita: Yu, H., Wang, F., Yuan, Jq. et al. HMGCS2-dependent β-OHB/H3K9bhb ameliorates synaptic plasticity and cognition in Alzheimer’s disease. Exp Mol Med 58, 813–831 (2026). https://doi.org/10.1038/s12276-026-01664-9
Palabras clave: Enfermedad de Alzheimer, metabolismo cetogénico, plasticidad sináptica, regulación epigenética, beta-hidroxibutirato