Clear Sky Science · fr
β-OHB/H3K9bhb dépendant de HMGCS2 améliore la plasticité synaptique et la cognition dans la maladie d’Alzheimer
Pourquoi les molécules énergétiques comptent pour la mémoire
La maladie d’Alzheimer est surtout connue pour la perte de mémoire et l’encombrement des tissus cérébraux, mais cette étude examine un aspect moins familier : la façon dont le carburant du cerveau et les interrupteurs génétiques interagissent. Les chercheurs explorent comment une molécule énergétique naturelle, souvent augmentée par les régimes cétogènes ou le jeûne, peut modifier les marques chimiques sur les protéines qui emballent l’ADN et, par ricochet, aider à restaurer les toutes petites connexions entre les neurones qui sous-tendent l’apprentissage et la mémoire. Leur travail pointe vers une nouvelle stratégie, basée sur le métabolisme, pour soutenir la fonction cérébrale dans la maladie d’Alzheimer.
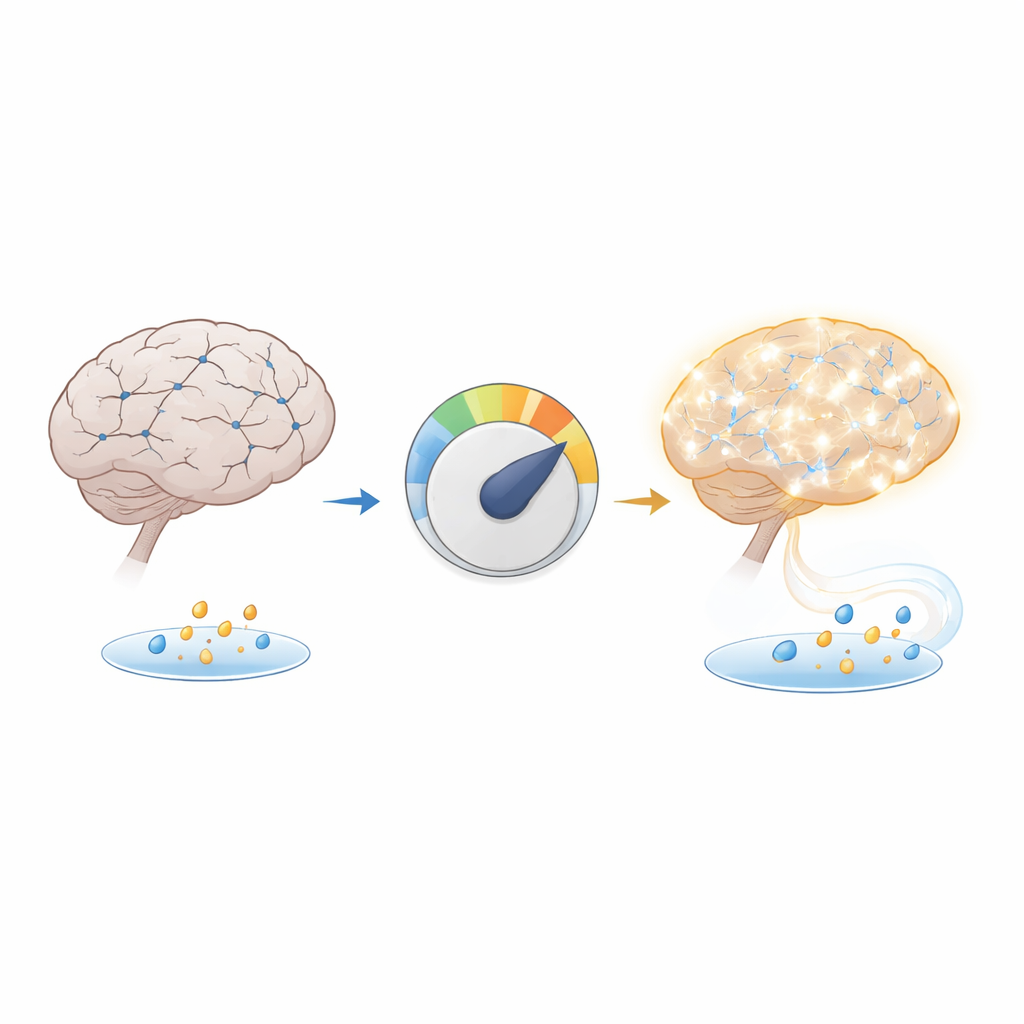
Une pénurie cachée dans le cerveau Alzheimer
L’équipe s’est concentrée sur le β-hydroxybutyrate, une petite molécule produite lorsque l’organisme brûle des graisses, et sur une marque chimique associée placée sur les histones, qui contribuent à organiser l’ADN. Cette marque, appelée H3K9bhb, a tendance à « ouvrir » des portions d’ADN pour permettre l’activation des gènes voisins. En examinant des tissus cérébraux d’un modèle murin largement utilisé de la maladie d’Alzheimer et de personnes atteintes, les scientifiques ont constaté que les niveaux de β-hydroxybutyrate et de H3K9bhb étaient tous deux réduits, en particulier dans l’hippocampe, un centre clé de la mémoire. Les taux sanguins de la molécule semblaient normaux, ce qui suggère que le problème n’est pas une pénurie de carburant au niveau de l’organisme, mais un défaut spécifique de production ou d’utilisation de ce carburant à l’intérieur du cerveau.
Alimenter les interrupteurs génétiques pour protéger le câblage nerveux
Ensuite, les chercheurs ont administré du β-hydroxybutyrate à des souris Alzheimer d’âge moyen pendant plusieurs mois. Ce traitement a élevé le niveau de la molécule dans le cerveau et augmenté les marques H3K9bhb, principalement dans les neurones plutôt que dans les cellules de soutien. Par des analyses génomiques globales et ciblées, ils ont montré que ces marques étaient devenues plus abondantes sur les régions de démarrage des gènes impliqués dans l’orientation des axones (les longs prolongements qui véhiculent les signaux) et dans la construction et le fonctionnement des synapses. Ces gènes, auparavant réprimés chez les souris Alzheimer, sont redevenus plus actifs. La microscopie a confirmé une augmentation des marqueurs d’axones et de synapses sains et que les neurones développaient davantage de branches et de petites épines, base structurelle de nouvelles connexions.
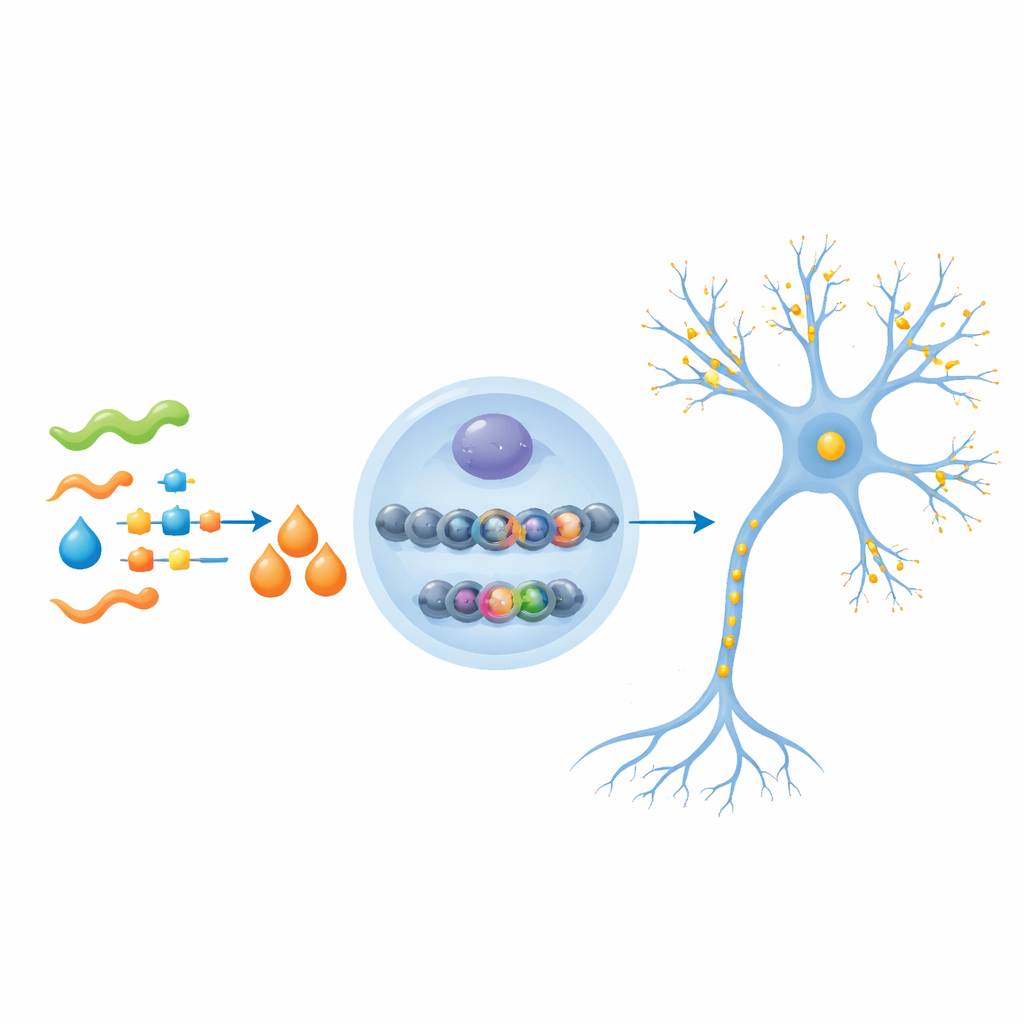
De synapses plus fortes à une mémoire plus nette
Parce que la communication entre neurones dépend fortement de certains récepteurs, l’équipe s’est penchée sur la famille des récepteurs NMDA et sur une protéine synaptique appelée Syn1. Chez les souris Alzheimer, ces protéines et l’activité de leurs gènes étaient diminuées, et les régions d’ADN correspondantes portaient moins de marques H3K9bhb. Le traitement par le β-hydroxybutyrate a restauré à la fois les marques chimiques et l’expression de ces composants synaptiques clés. Les tests comportementaux ont raconté une histoire comparable : les souris traitées ont appris plus rapidement l’emplacement d’une plate-forme cachée dans un labyrinthe aquatique, s’en sont mieux souvenues quelques jours plus tard, ont distingué de nouveaux objets d’objets familiers et ont montré une mémoire de peur renforcée. Il est important de noter que leur capacité de nage et leurs mouvements généraux n’étaient pas modifiés, indiquant que les améliorations étaient d’ordre cognitif et non physique.
L’enzyme cérébrale qui règle le niveau de carburant
L’étude a ensuite cherché pourquoi le β-hydroxybutyrate est bas en premier lieu. La molécule est synthétisée dans les cellules par un petit nombre d’enzymes, dont une appelée HMGCS2 qui contrôle une étape clé. En analysant des jeux de données humains publics, des cerveaux de souris, des cellules cérébrales en culture exposées à des fragments protéiques liés à Alzheimer et des neurones primaires de souris Alzheimer, les chercheurs ont constaté que HMGCS2 était systématiquement réduit. Ils ont retracé cette baisse jusqu’à une diminution d’un facteur de transcription, PPARα, qui stimule normalement le gène HMGCS2. Lorsqu’ils ont artificiellement augmenté HMGCS2 dans des neurones ou dans le cerveau de souris Alzheimer, le β-hydroxybutyrate et H3K9bhb ont augmenté, les gènes liés aux synapses se sont rallumés, les structures synaptiques se sont améliorées et les performances mnésiques sur plusieurs tâches se sont rapprochées de celles des souris saines.
Repenser le traitement autour du carburant cérébral et du contrôle des gènes
Pris ensemble, les résultats décrivent une chaîne d’événements : la réduction de HMGCS2 dans les cerveaux Alzheimer conduit à une moindre production de β-hydroxybutyrate, à moins de marques H3K9bhb sur les gènes soutenant les synapses, à des synapses affaiblies et au déclin cognitif. Restaurer les niveaux de β-hydroxybutyrate — soit directement, soit en augmentant HMGCS2 — reconstruit ces marques chimiques, ravive l’activité des gènes importants pour les axones et les synapses, et améliore l’apprentissage et la mémoire chez la souris. Pour un observateur non spécialiste, le message est que la maladie d’Alzheimer ne se résume pas aux plaques et aux enchevêtrements, mais aussi à la manière dont le cerveau gère son énergie et contrôle l’accès à des gènes cruciaux. Cibler cette voie « carburant-vers-gènes » pourrait compléter les approches existantes et inspirer de nouveaux traitements visant à stabiliser le câblage cérébral de l’intérieur.
Citation: Yu, H., Wang, F., Yuan, Jq. et al. HMGCS2-dependent β-OHB/H3K9bhb ameliorates synaptic plasticity and cognition in Alzheimer’s disease. Exp Mol Med 58, 813–831 (2026). https://doi.org/10.1038/s12276-026-01664-9
Mots-clés: maladie d’Alzheimer, métabolisme cétogène, plasticité synaptique, régulation épigénétique, beta-hydroxybutyrate