Clear Sky Science · nl
HMGCS2-afhankelijke β-OHB/H3K9bhb verbetert synaptische plasticiteit en cognitie bij de ziekte van Alzheimer
Waarom energiemoleculen belangrijk zijn voor geheugen
De ziekte van Alzheimer staat vooral bekend om geheugenverlies en aangetast hersenweefsel, maar deze studie belicht een minder bekende kant van de aandoening: hoe de brandstof van de hersenen en genregelaars op elkaar inwerken. De onderzoekers onderzoeken hoe een natuurlijk brandstofmolecuul, dat vaak verhoogd wordt door ketogene diëten of vasten, chemische labels op DNA-verpakkende eiwitten kan omkeren en daarmee kan helpen de kleine verbindingen tussen zenuwcellen die ten grondslag liggen aan leren en geheugen te herstellen. Hun werk wijst op een nieuwe, op het metabolisme gebaseerde strategie om de hersenfunctie bij de ziekte van Alzheimer te ondersteunen.
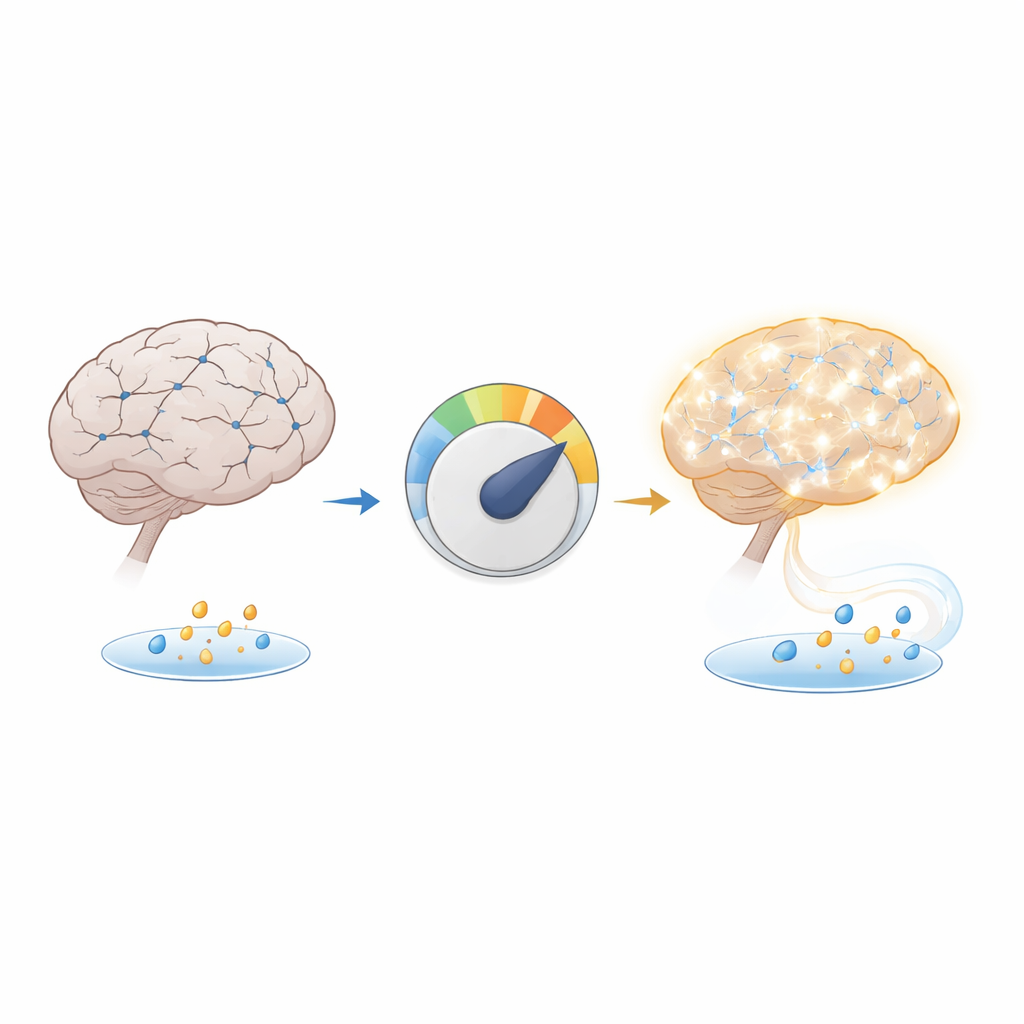
Een verborgen tekort in de Alzheimer-hersenen
Het team richtte zich op β-hydroxyboterzuur, een klein molecuul dat wordt geproduceerd wanneer het lichaam vet verbrandt, en op een verwant chemisch label dat op histoneiwitten wordt geplaatst, die helpen bij de organisatie van DNA. Dit label, H3K9bhb genoemd, heeft de neiging om stukken DNA "open te zetten" zodat nabijgelegen genen aan kunnen gaan. Bij onderzoek van hersenweefsel van een veelgebruikt muismodel voor Alzheimer en van mensen met Alzheimer vonden de wetenschappers dat de niveaus van β-hydroxyboterzuur en H3K9bhb beide verlaagd waren, vooral in de hippocampus, een belangrijk geheugencentrum. De bloedwaarden van het molecuul leken normaal, wat suggereert dat het probleem niet een tekort aan brandstof in het hele lichaam is, maar een specifieke fout in de productie of het gebruik van deze brandstof binnenin de hersenen.
Brandstof voor genregelaars om zenuwbedrading te beschermen
Vervolgens gaven de onderzoekers β-hydroxyboterzuur aan Alzheimer-muizen van middelbare leeftijd gedurende enkele maanden. Deze behandeling verhoogde het niveau van het molecuul in de hersenen en versterkte H3K9bhb-markeringen, voornamelijk in neuronen in plaats van ondersteunende cellen. Met genoomwijde en gerichte analyses lieten ze zien dat deze markeringen talrijker werden op de startgebieden van genen die betrokken zijn bij het geleiden van axonen (de lange vezels die signalen dragen) en bij het bouwen en laten functioneren van synapsen. Die genen, eerder afgezwakt in de Alzheimer-muizen, werden opnieuw actiever. Microscopen bevestigden dat markers voor gezonde axonen en synapsen toenamen en dat zenuwcellen meer vertakkingen en kleine uitsteeksels ontwikkelden — de structurele basis voor nieuwe verbindingen.
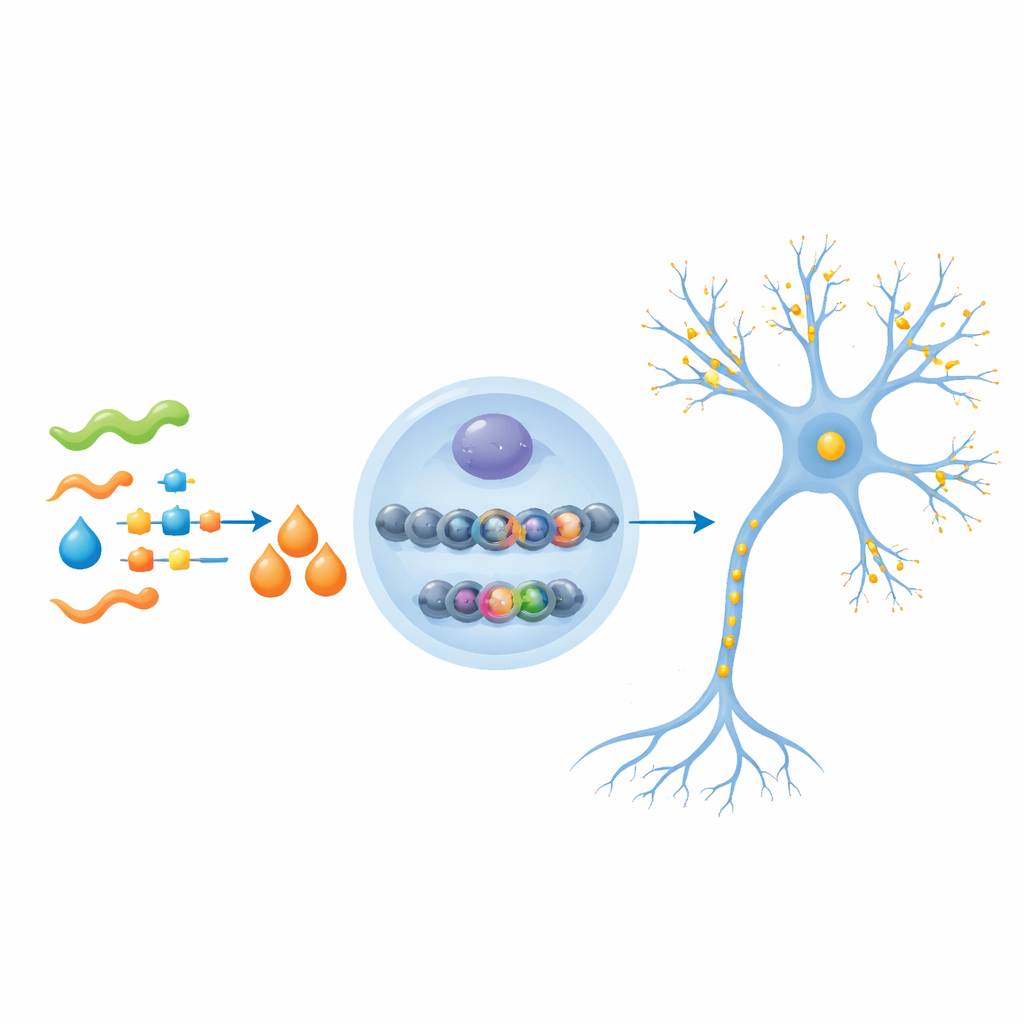
Van sterkere synapsen naar scherper geheugen
Aangezien communicatie tussen neuronen sterk afhankelijk is van bepaalde receptor-eiwitten, onderzochten de onderzoekers de NMDA-receptorfamilie en een synaptisch eiwit genaamd Syn1 nauwkeurig. Bij de Alzheimer-muizen waren deze eiwitten en hun genactiviteit onderdrukt, en droegen de overeenkomstige DNA-regio’s minder H3K9bhb-markeringen. Behandeling met β-hydroxyboterzuur herstelde zowel de chemische labels als de expressie van deze belangrijke synaptische componenten. Gedragstests vertelden hetzelfde verhaal: behandelde muizen leerden sneller de locatie van een verborgen platform in een waterlabyrint, onthielden het beter dagen later, konden nieuwe objecten onderscheiden van bekende, en toonden sterkere angstgebaseerde herinneringen. Belangrijk was dat hun zwemvermogen en algehele beweging ongewijzigd waren, wat aangeeft dat de verbeteringen cognitief en niet fysiek waren.
Het hersenenzym dat het brandstofniveau bepaalt
De studie vroeg zich vervolgens af waarom β-hydroxyboterzuur aanvankelijk laag is. Het molecuul wordt in cellen gemaakt door een klein aantal enzymen, waaronder een die HMGCS2 heet en een sleutelstap beheerst. Door openbare menselijke datasets, muizenhersenen, gekweekte hersencellen die werden blootgesteld aan Alzheimer-gerelateerde proteïnefragmenten, en primaire neuronen van Alzheimer-muizen te analyseren, vonden de onderzoekers dat HMGCS2 consequent verlaagd was. Ze traceerden dit terug naar een daling in een transcriptiefactor, PPARα, die normaal gesproken het HMGCS2-gen stimuleert. Wanneer ze kunstmatig HMGCS2 verhoogden in neuronen of in de hersenen van Alzheimer-muizen, stegen β-hydroxyboterzuur en H3K9bhb, werden synapsgerelateerde genen weer actief, verbeterden synaptische structuren, en benaderde het geheugenpresteren in meerdere taken dat van gezonde muizen.
Behandeling herdenken rond hersenbrandstof en gencontrole
Gezamenlijk schetsen de bevindingen een keten van gebeurtenissen: verlaagde HMGCS2 in Alzheimer-hersenen leidt tot minder productie van β-hydroxyboterzuur, minder H3K9bhb-markeringen op genen die synapsen ondersteunen, zwakkere synapsen en cognitieve achteruitgang. Het herstellen van β-hydroxyboterzuurniveaus — direct of door HMGCS2 te verhogen — herbouwt deze chemische labels, herleeft genactiviteit die belangrijk is voor axonen en synapsen, en verbetert leren en geheugen bij muizen. Voor een niet-specialist is de boodschap dat Alzheimer niet alleen gaat over plaques en kluwens, maar ook over hoe de hersenen hun energie beheren en de toegang tot cruciale genen regelen. Het richten op deze “brandstof-naar-gen” route zou bestaande benaderingen kunnen aanvullen en nieuwe behandelingen kunnen inspireren die werken door de bedrading van de hersenen van binnenuit te stabiliseren.
Bronvermelding: Yu, H., Wang, F., Yuan, Jq. et al. HMGCS2-dependent β-OHB/H3K9bhb ameliorates synaptic plasticity and cognition in Alzheimer’s disease. Exp Mol Med 58, 813–831 (2026). https://doi.org/10.1038/s12276-026-01664-9
Trefwoorden: Ziekte van Alzheimer, ketogeen metabolisme, synaptische plasticiteit, epigenetische regulatie, beta-hydroxyboterzuur