Clear Sky Science · zh
局部输送OSK因子实现部分细胞重编程,以减轻骨关节炎和软骨纤维化
这对疼痛关节为何重要
膝关节骨关节炎是导致疼痛和残疾的主要原因之一,但现有治疗大多只是缓解症状,而不能修复受损的软骨。这项研究探索了再生医学中的一个大胆设想:用三种称为OSK的生物开关温和“重置”衰老的关节细胞,并将其直接递送到膝关节。研究表明,这种方法不仅可能减缓关节损伤,还能逆转部分导致日常活动困难的瘢痕和僵硬。
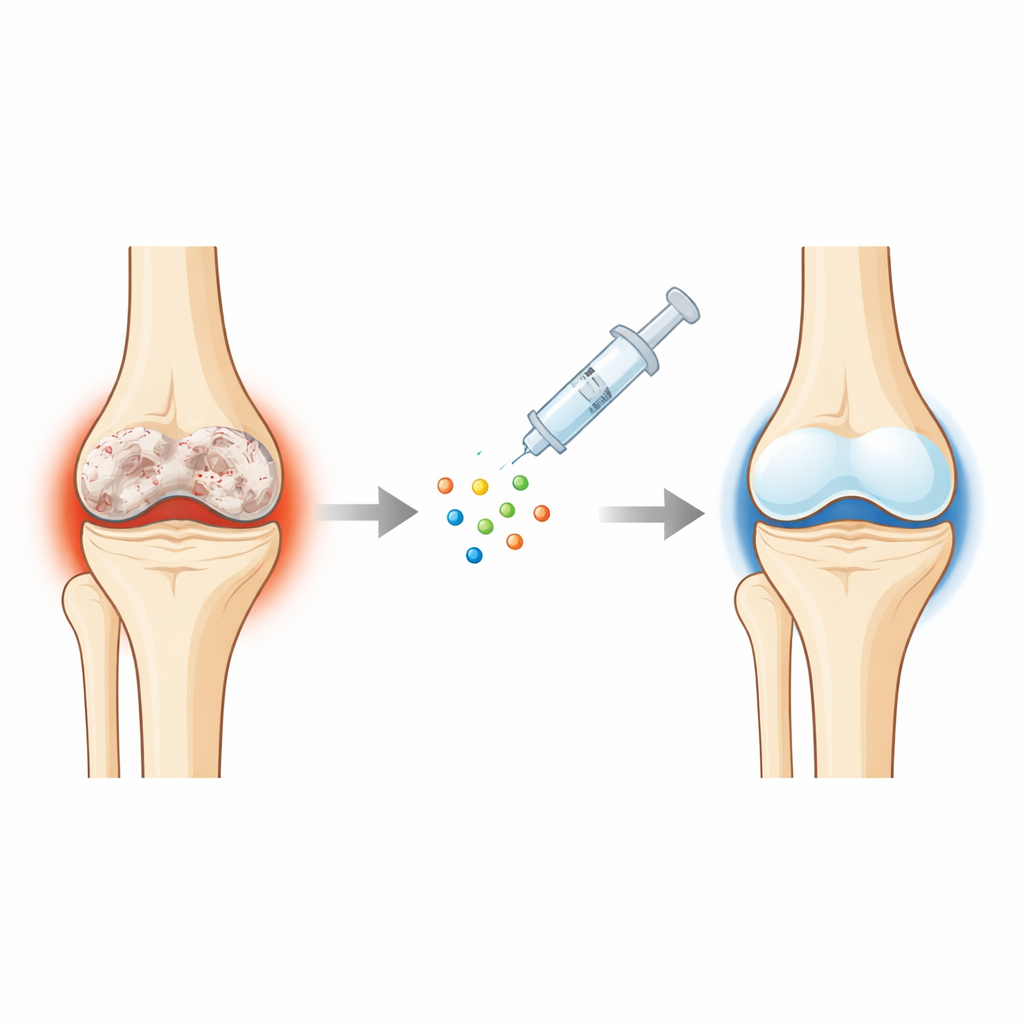
深入了解受损的软骨
在骨关节炎中,覆盖在骨端的光滑、白色软骨会逐步破坏。下方的骨组织增厚,表面变得粗糙,原本弹性的层被纤维样瘢痕组织取代。维持软骨的细胞——软骨细胞——在年龄、压力和炎症的驱动下进入有害状态:它们使周围环境发炎、更易死亡,并开始表现得更像成骨细胞。由于软骨血供少、修复细胞稀少,一旦这一过程启动就很难逆转,患者因此出现疼痛、肿胀和活动受限。
温和地倒转细胞时钟
科学家发现某些基因开关可以将细胞的“内部年龄”倒转,但过度推动可能把正常组织变成易发肿瘤的干细胞。为避免这种风险,作者只使用了三种因子——Oct4、Sox2 和 Klf4,合称OSK——省略了第四种更危险的成分。他们将OSK装入一种无害的病毒载体并直接注入小鼠膝关节。在体外培养的软骨细胞中,暴露于OSK后细胞保持了正常身份,同时变得更有韧性:它们产生更少的炎症分子、更能抵抗细胞死亡,并且在类似疾病的严酷条件下不太容易向成骨样细胞转变。
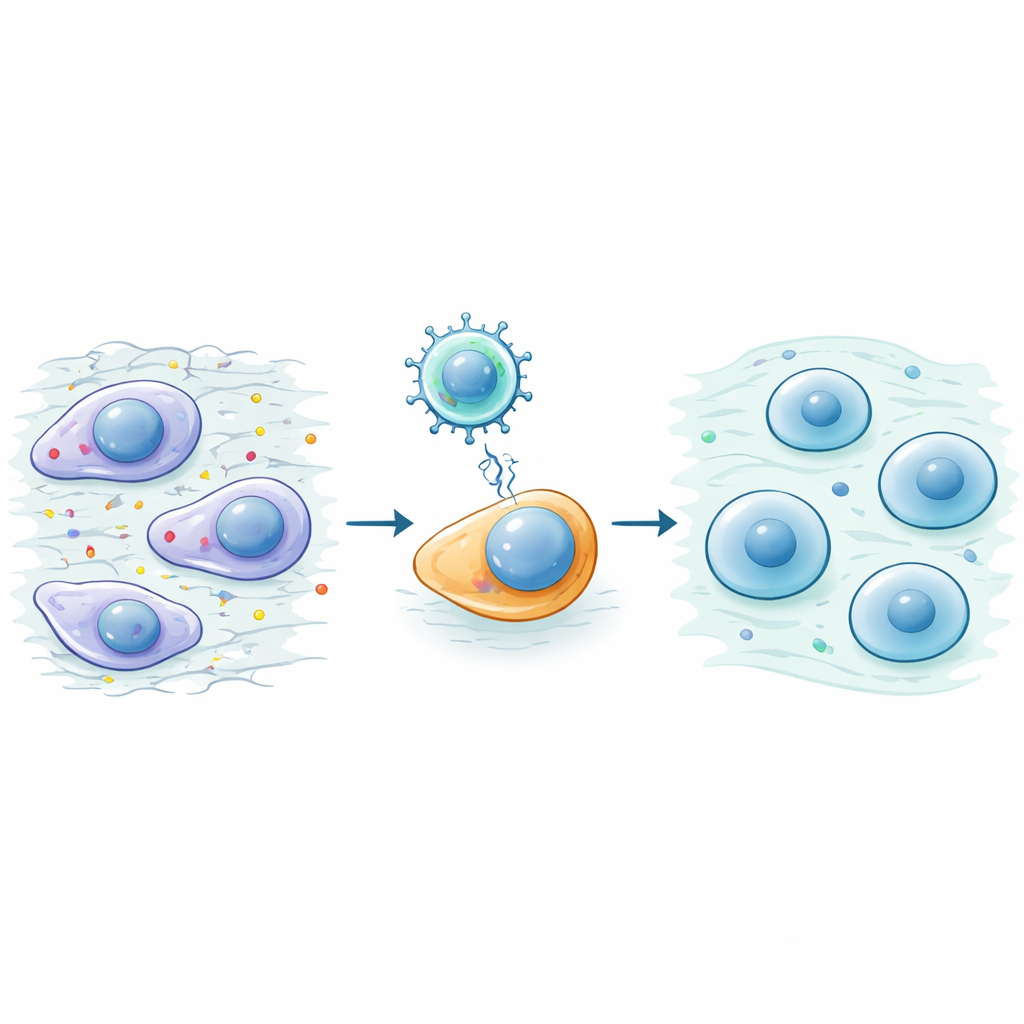
保护并重建受损关节
研究团队随后在两种由外科损伤诱导的标准小鼠膝关节骨关节炎模型中测试了OSK。接受OSK处理的老鼠活动更好、握力更强,触碰足部时的疼痛反应更轻。膝关节扫描显示关节表面更平滑,下软骨处的异常骨增生较少。显微镜下,OSK处理的关节保留了更多原本的、玻璃样的“透明软骨”,而僵硬的纤维软骨斑块较少。构建软骨的有益成分得以保留,而显示分解和疤痕形成的破坏性及“过度表达”标志被抑制。值得注意的是,OSK即便在疾病后期给药也有效,能将已形成的纤维软骨推动回更接近正常的透明样状态。
重置衰老软骨的表观遗传密码
除了结构改善和缓解疼痛,研究者还探寻OSK是否改变了关节组织中更深层次的分子衰老迹象。他们关注DNA甲基化,这是一种作用如表观遗传时钟的DNA化学标记系统。在骨关节炎软骨中,这个时钟走得更快:衰老标志上升,控制炎症和组织质量的基因出现失调。通过对全基因组甲基化谱的分析,团队发现OSK处理的软骨在表观上比其实际年龄显得“更年轻”,且与未处理的病变组织有显著差异。该疗法降低了一种与软骨衰老相关的DNA甲基转移酶的表达,同时提升了另一种帮助擦除甲基标记的酶TET2。当故意阻断TET2时,OSK的许多保护性效应消失,突显该酶为关键中介者。
这对未来护理的可能意义
综合来看,研究结果表明,将OSK因子以精细调控的方式输送到膝关节,可以在不将细胞转变为失控干细胞的情况下,部分重编程衰老、病变的软骨细胞。在小鼠中,这种方法缓解疼痛、保护关节结构,甚至能将瘢痕样纤维软骨转回更接近原本具有缓冲功能的形态——这些变化与可测量的“更年轻”表观遗传状态一致。尽管还需在更大动物和人体中测试安全性、剂量及长期效果,但这项研究为未来骨关节炎治疗提供了早期前景:不再仅仅缓解症状,而是重写关节组织的衰老密码。
引用: Liu, YW., Zou, JT., Gong, JS. et al. Local delivery of OSK factors enables partial cellular reprogramming to mitigate osteoarthritis and cartilage fibrosis. Exp Mol Med 58, 782–797 (2026). https://doi.org/10.1038/s12276-026-01662-x
关键词: 骨关节炎, 软骨再生, 细胞重编程, 表观遗传学, 基因疗法