Clear Sky Science · sv
Lokal leverans av OSK‑faktorer möjliggör partiell cellulär omprogrammering för att mildra artros och broskfibros
Varför detta spelar roll för värkande leder
Knäartros är en ledande orsak till smärta och funktionsnedsättning, men dagens behandlingar dämpar oftast symtomen snarare än återställer det skadade brosket. Denna studie undersöker en djärv idé från regenerativ medicin: att varsamt ”återställa” åldrande ledceller med tre biologiska reglage kallade OSK‑faktorer, levererade direkt in i knät. Arbetet tyder på att det kan vara möjligt att inte bara bromsa ledskador, utan också vända viss ärrbildning och stelhet som gör vardagsrörelser svåra.
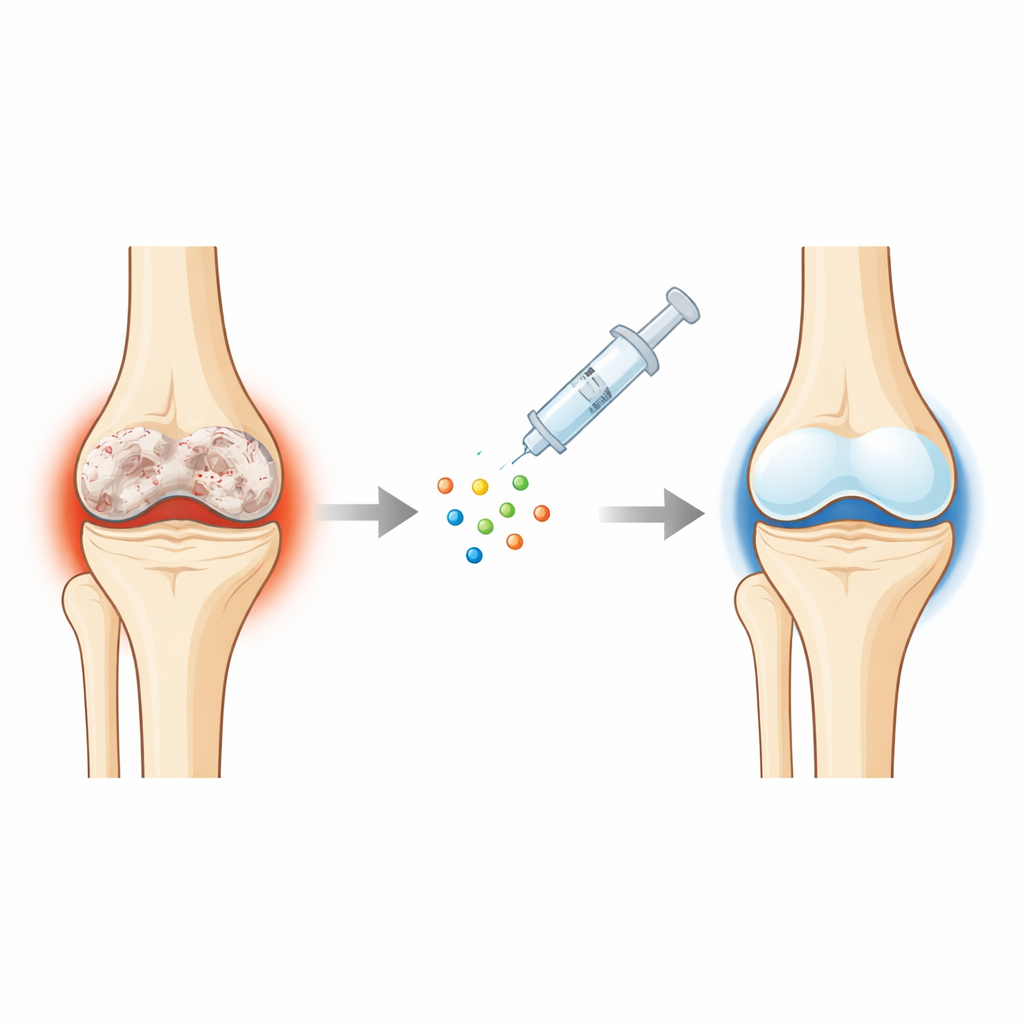
En närmare titt på utslitet brosk
Vid artros bryts det jämna, vita brosket som dämpar benändarna gradvis ner. Underliggande ben förtjockas, ytan blir grov och fibröst ärrliknande vävnad ersätter det ursprungliga fjädrande skiktet. De celler som upprätthåller brosk, kondrocyter, drivs av ålder, belastning och inflammation in i ett skadligt tillstånd: de orsakar inflammation i omgivningen, dör lättare och börjar bete sig mer som benbildande celler. Eftersom brosk har låg blodtillförsel och få reparationsceller är det svårt att vända denna process när den väl startat, vilket lämnar patienter med smärta, svullnad och nedsatt rörlighet.
Att varsamt vrida tillbaka den cellulära klockan
Forskare har funnit att vissa genetiska reglage kan spola tillbaka en cells inre ”ålder”, men att trycka för hårt kan förvandla normala vävnader till tumörbenägna stamceller. För att undvika denna risk använde författarna endast tre faktorer—Oct4, Sox2 och Klf4, tillsammans kallade OSK—och utelämnade en fjärde, mer riskfylld komponent. De förpackade OSK i en ofarlig viral bärare och injicerade den direkt i musknän. I odlingsskålar behöll broskceller som exponerades för OSK sin normala identitet samtidigt som de blev mer motståndskraftiga: de producerade färre inflammatoriska molekyler, motstod celldöd och var mindre benägna att omvandlas till benliknande celler även under hårda, sjukdomsliknande förhållanden.
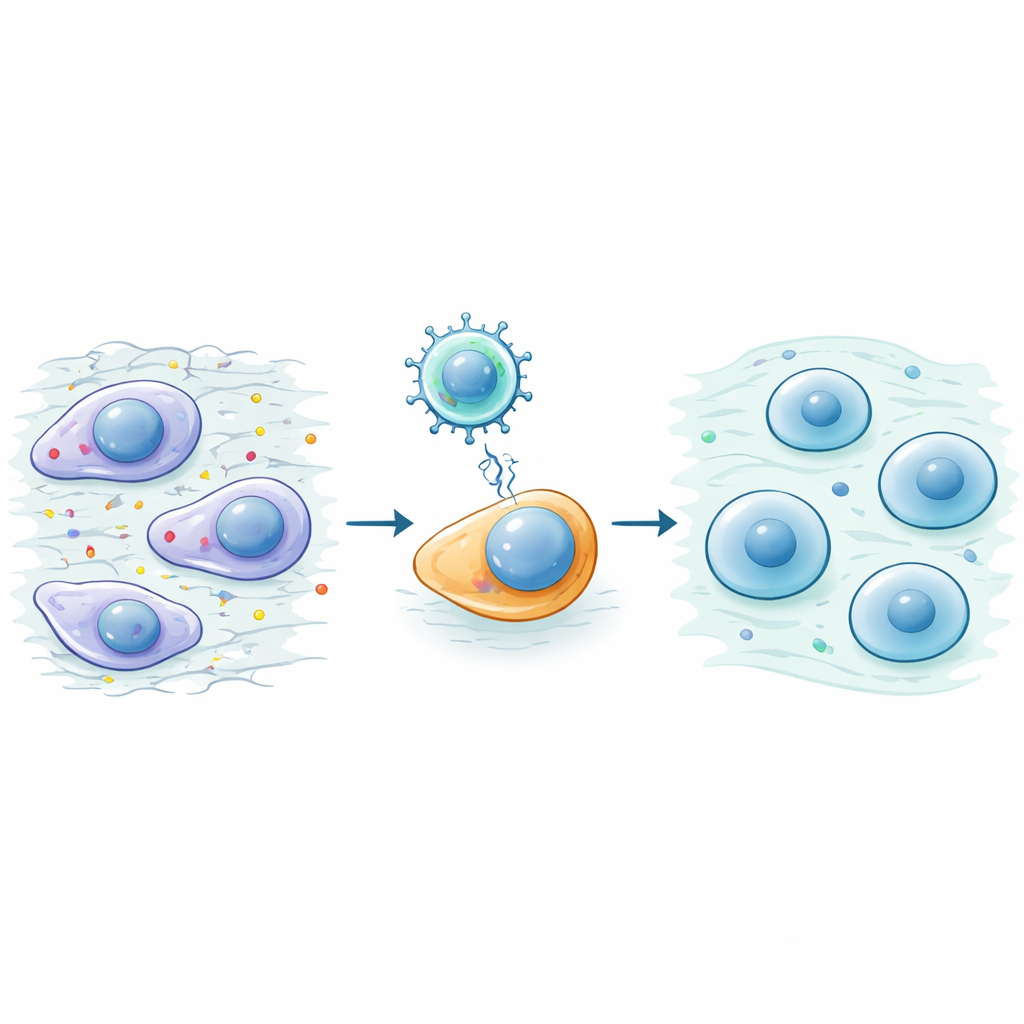
Skydda och återbygga skadade leder
Forskarna testade sedan OSK i två standardmodeller för knäartros hos mus, framkallade genom kirurgisk skada. Möss som fick OSK‑behandling rörde sig bättre, hade starkare grepp och visade mindre smärta vid beröring av tassarna. Skanningar av deras knän visade jämnare ledytor och mindre onormal benförtjockning under brosket. Under mikroskopet behöll OSK‑behandlade leder mer av det ursprungliga, glasartade ”hyalina” brosket och färre områden med stelt fibrobrok. Hjälpsamma byggstenar för brosk bevarades, medan destruktiva och överväxta markörer för nedbrytning och ärrbildning minskade. Anmärkningsvärt är att OSK också fungerade när det gavs senare i sjukdomsförloppet, och påverkade redan bildad fibrobrok mot ett mer normalt, hyalinlikt tillstånd.
Återställa broskets epigenetiska kod
Bortom struktur och smärtlindring frågade forskarna om OSK förändrar djupare molekylära tecken på åldrande i ledvävnaden. De fokuserade på DNA‑metylering, ett kemiskt märkningssystem på DNA som fungerar som en epigenetisk klocka. I artrotiskt brosk går denna klocka fortare: åldersmarkörer stiger och gener som styr inflammation och vävnadskvalitet är felreglerade. Genom att profilera metylering över genomet fann teamet att OSK‑behandlat brosk såg ”yngre” ut än väntat för sin ålder och skilde sig markant från obehandlad sjuk vävnad. Terapin dämpade uttrycket av ett DNA‑metylerande enzym kopplat till broskåldrande och ökade ett annat enzym, TET2, som hjälper till att ta bort metyleringsmärken. När TET2 medvetet blockerades försvann många av OSK:s skyddande effekter, vilket lyfter fram detta enzym som en nyckelmedlare.
Vad detta kan innebära för framtida vård
Tillsammans tyder fynden på att noggrant avvägd leverans av OSK‑faktorer in i knät kan delvis omprogrammera åldrande, sjuka broskceller utan att förvandla dem till okontrollerade stamceller. Hos möss lindrar denna metod smärta, skyddar ledstrukturen och omvandlar till och med ärrliknande fibrobrok tillbaka mot dess ursprungliga, dämpande form—förändringar som överensstämmer med ett mätbart ”yngre” epigenetiskt tillstånd. Även om mycket arbete återstår för att testa säkerhet, dosering och långtidseffekter i större djur och människor, ger denna studie en tidig inblick i en framtid där artrosbehandling inte bara syftar till att dämpa symptom, utan att skriva om den åldrande koden i ledvävnaderna själva.
Citering: Liu, YW., Zou, JT., Gong, JS. et al. Local delivery of OSK factors enables partial cellular reprogramming to mitigate osteoarthritis and cartilage fibrosis. Exp Mol Med 58, 782–797 (2026). https://doi.org/10.1038/s12276-026-01662-x
Nyckelord: artros, broskregenerering, cellulär omprogrammering, epigenetik, genterapi