Clear Sky Science · de
Die lokale Verabreichung von OSK-Faktoren ermöglicht partielle zelluläre Reprogrammierung zur Minderung von Arthrose und Knorpelfibrose
Warum das für schmerzende Gelenke wichtig ist
Die Kniearthrose ist eine führende Ursache für Schmerzen und Behinderung, doch die heutigen Behandlungen überdecken meist nur die Symptome, anstatt beschädigten Knorpel wiederherzustellen. Diese Studie untersucht eine mutige Idee der regenerativen Medizin: das behutsame „Zurücksetzen“ der Zellen im alternden Gelenk mithilfe von drei biologischen Schaltern, den sogenannten OSK-Faktoren, die direkt ins Knie verabreicht werden. Die Arbeit deutet darauf hin, dass es möglich sein könnte, nicht nur das Fortschreiten der Gelenkschädigung zu verlangsamen, sondern auch einige Narbenbildungen und Steifigkeit umzukehren, die alltägliche Bewegungen erschweren.
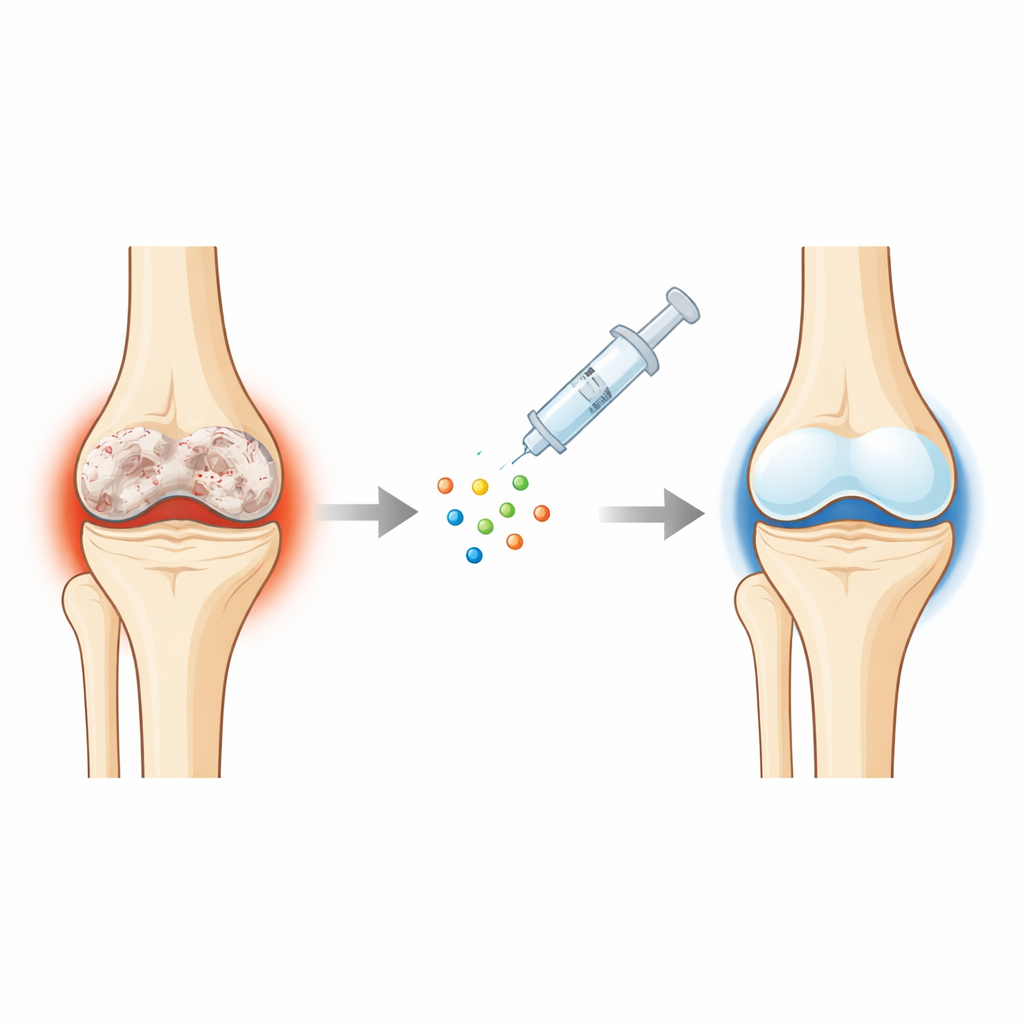
Ein genauerer Blick auf verschlissenen Knorpel
Bei Arthrose bricht der glatte, weiße Knorpel, der die Enden der Knochen polstert, allmählich ab. Der darunterliegende Knochen verdickt sich, die Oberfläche wird rau und faseriges, narbenähnliches Gewebe ersetzt die ursprüngliche elastische Schicht. Die Zellen, die den Knorpel erhalten — die Chondrozyten — werden durch Alter, Belastung und Entzündung in einen schädlichen Zustand gedrängt: Sie fördern lokale Entzündungen, sterben leichter ab und beginnen sich mehr wie knochenbildende Zellen zu verhalten. Da Knorpel nur geringe Durchblutung und wenige Reparaturzellen hat, ist dieser Prozess, einmal eingesetzt, sehr schwer umkehrbar, was Patienten Schmerzen, Schwellungen und eingeschränkte Mobilität beschert.
Das Zellalter behutsam zurückdrehen
Wissenschaftler haben herausgefunden, dass bestimmte Gen-Schalter das innere „Alter“ einer Zelle zurückspulen können, doch zu starkes Eingreifen kann normales Gewebe in tumoranfällige Stammzellen verwandeln. Um dieses Risiko zu vermeiden, verwendeten die Autor:innen nur drei Faktoren — Oct4, Sox2 und Klf4, zusammen OSK genannt — und ließen eine vierte, riskantere Komponente weg. Sie verpackten OSK in einen harmlosen viralen Träger und injizierten ihn direkt in die Kniegelenke von Mäusen. In Zellkulturen behielten Knorpelzellen, die OSK ausgesetzt waren, ihre normale Identität, wurden dabei aber widerstandsfähiger: Sie produzierten weniger entzündungsfördernde Moleküle, widerstanden dem Zelltod besser und neigten weniger dazu, sich unter krankheitsähnlichen Bedingungen in knochenähnliche Zellen zu verwandeln.
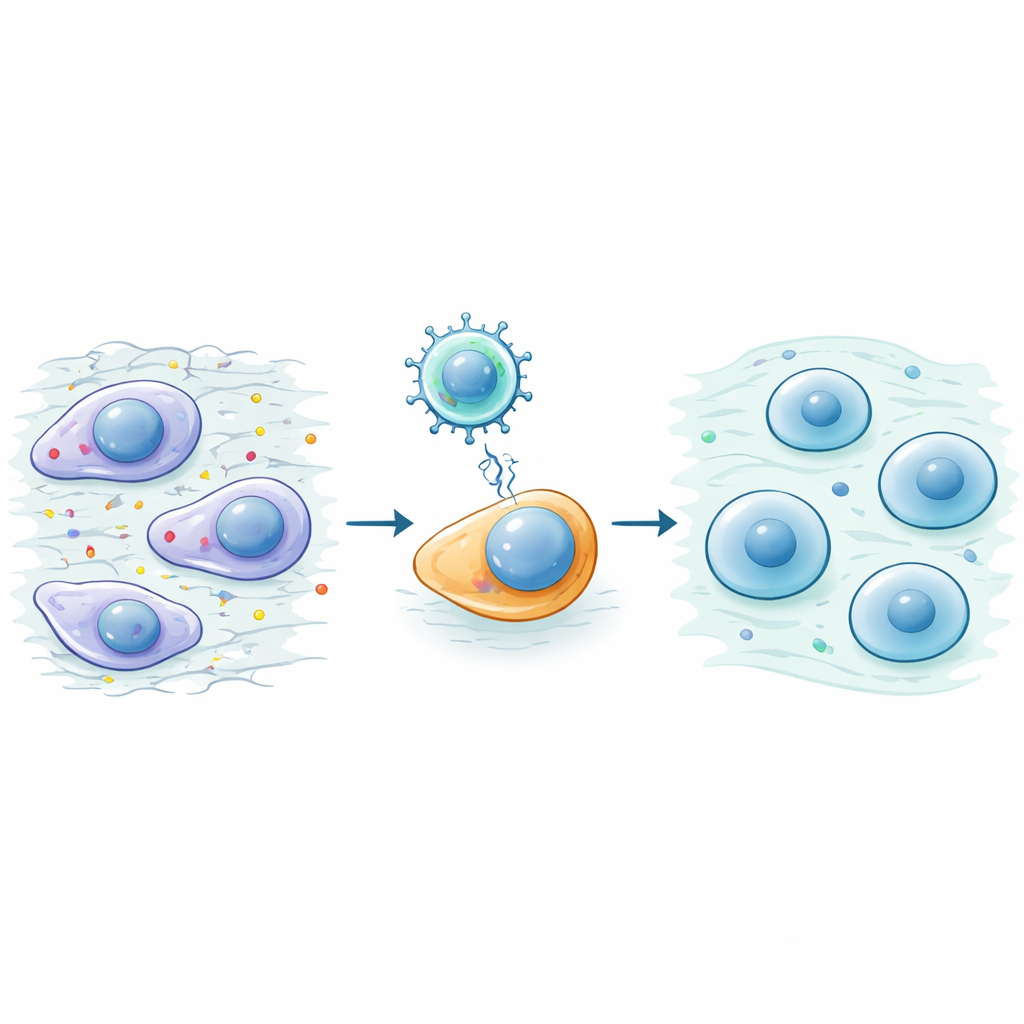
Schutz und Wiederaufbau beschädigter Gelenke
Das Team testete OSK anschließend in zwei etablierten Mausmodellen der Kniearthrose, die durch chirurgische Verletzung erzeugt wurden. Mäuse, die die OSK-Behandlung erhielten, bewegten sich besser, griffen kräftiger zu und zeigten weniger Schmerzreaktionen bei Berührung ihrer Pfoten. Auf Scans ihrer Knie zeigten sich glattere Gelenkflächen und weniger abnorme Knochenverdickung unter dem Knorpel. Unter dem Mikroskop behielten OSK-behandelte Gelenke mehr des ursprünglichen, gläsernen „hyalinen“ Knorpels und wiesen weniger Stellen mit steifer Fibroknorpelbildung auf. Nützliche Bausteine des Knorpels blieben erhalten, während zerstörerische und „überwachsene“ Marker für Abbau und Vernarbung reduziert wurden. Bemerkenswert ist, dass OSK auch bei später Gabe in der Erkrankung wirkte und bereits gebildeten Fibroknorpel in Richtung eines normaleren, hyalinähnlichen Zustands zurückzudrängen schien.
Das epigenetische Muster des alternden Knorpels zurücksetzen
Über Struktur und Schmerzlinderung hinaus fragten die Forscher:innen, ob OSK die tieferen molekularen Zeichen des Alterns im Gelenkgewebe verändert. Sie konzentrierten sich auf DNA-Methylierung, ein chemisches Markierungssystem auf der DNA, das wie eine epigenetische Uhr wirkt. Bei arthrotischem Knorpel läuft diese Uhr schneller: Altersmarker steigen, und Gene, die Entzündung und Gewebequalität steuern, sind fehlreguliert. Durch die Profilerstellung der Methylierung über das gesamte Genom fanden die Forscher:innen, dass OSK-behandelter Knorpel „jünger“ aussah als für sein Alter zu erwarten und sich deutlich vom unbehandelten, erkrankten Gewebe unterschied. Die Therapie dämpfte die Expression eines DNA-methylierenden Enzyms, das mit Knorpelalterung in Verbindung steht, und förderte ein anderes Enzym, TET2, das hilft, Methylierungsmarken zu entfernen. Als TET2 gezielt blockiert wurde, verschwanden viele der schützenden Effekte von OSK, was dieses Enzym als wichtigen Vermittler hervorhebt.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt deuten die Befunde darauf hin, dass eine sorgfältig abgestimmte Verabreichung der OSK-Faktoren ins Knie alternde, erkrankte Knorpelzellen teilweise reprogrammieren kann, ohne sie in unkontrollierbare Stammzellen zu verwandeln. Bei Mäusen lindert dieser Ansatz Schmerzen, schützt die Gelenkstruktur und wandelt sogar narbenartigen Fibroknorpel wieder in eine ursprünglichere, polsternde Form um — Veränderungen, die mit einem messbar „jüngeren“ epigenetischen Zustand übereinstimmen. Zwar bleibt viel Arbeit, um Sicherheit, Dosierung und Langzeitwirkungen in größeren Tieren und beim Menschen zu prüfen, doch die Studie bietet einen frühen Blick auf eine Zukunft, in der Arthrosebehandlung nicht nur Symptome lindert, sondern den Alterungscode der Gelenkgewebe selbst neu schreibt.
Zitation: Liu, YW., Zou, JT., Gong, JS. et al. Local delivery of OSK factors enables partial cellular reprogramming to mitigate osteoarthritis and cartilage fibrosis. Exp Mol Med 58, 782–797 (2026). https://doi.org/10.1038/s12276-026-01662-x
Schlüsselwörter: Arthrose, Knorpelregeneration, zelluläre Reprogrammierung, Epigenetik, Gentherapie