Clear Sky Science · nl
Lokale toediening van OSK-factoren maakt gedeeltelijke cellulaire herprogrammering mogelijk om artrose en kraakbeenfibrose te verminderen
Waarom dit belangrijk is voor pijnlijke gewrichten
Artrose van de knie is een belangrijke oorzaak van pijn en invaliditeit, maar de huidige behandelingen maskeren meestal symptomen in plaats van beschadigd kraakbeen te herstellen. Deze studie onderzoekt een gedurfde gedachte uit de regeneratieve geneeskunde: het voorzichtig "resetten" van verouderende gewrichtscellen met drie biologische schakelaars, de zogenaamde OSK-factoren, rechtstreeks in de knie toegediend. Het werk suggereert dat het mogelijk zou kunnen zijn niet alleen om gewrichtsschade te vertragen, maar ook om sommige littekens en stijfheid terug te draaien die alledaagse bewegingen bemoeilijken.
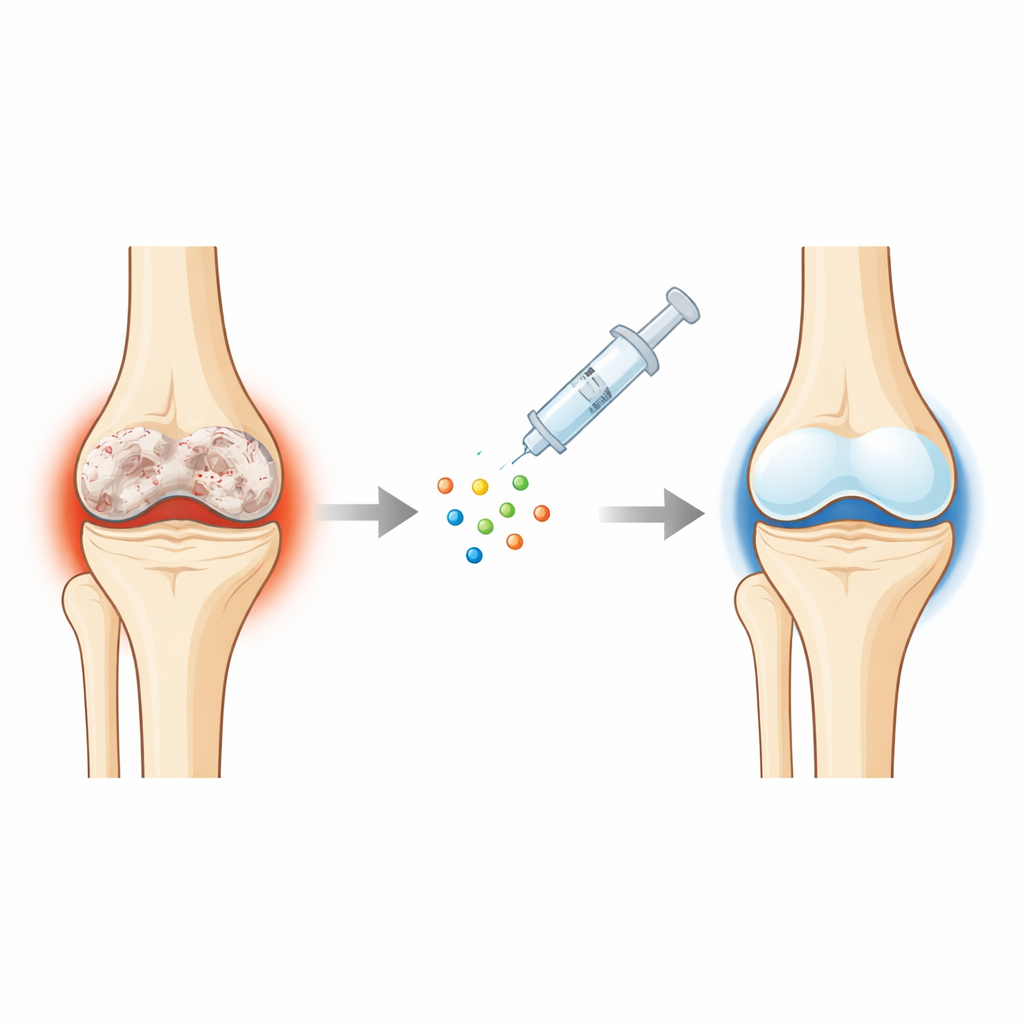
Een nadere blik op versleten kraakbeen
Bij artrose gaat het gladde, witte kraakbeen dat de uiteinden van botten dempt geleidelijk achteruit. Het onderliggende bot verdikt, het oppervlak wordt ruw en vezelig, littekenachtig weefsel vervangt de oorspronkelijke veerkrachtige laag. De cellen die kraakbeen onderhouden, chondrocyten, worden door leeftijd, stress en ontsteking in een schadelijke staat gedrukt: ze veroorzaken ontsteking in hun omgeving, sterven gemakkelijker af en beginnen zich meer te gedragen als botvormende cellen. Omdat kraakbeen weinig bloedtoevoer en weinig herstellende cellen heeft, is het, zodra dit proces begint, zeer moeilijk om te keren, wat patiënten achterlaat met pijn, zwelling en verlies van mobiliteit.
Het celklokje voorzichtig terugdraaien
Wetenschappers hebben ontdekt dat bepaalde genschakelaars de interne "leeftijd" van een cel kunnen terugdraaien, maar te ver gaan kan normale weefsels veranderen in tumorgevoelige stamcellen. Om dit gevaar te vermijden gebruikten de auteurs slechts drie factoren—Oct4, Sox2 en Klf4, samen bekend als OSK—en lieten ze een vierde, risicovollere component weg. Ze verpakten OSK in een onschadelijke virusdrager en injecteerden deze direct in de kniegewrichten van muizen. In laboratoriumschalen behielden kraakbeencellen die aan OSK werden blootgesteld hun normale identiteit terwijl ze veerkrachtiger werden: ze produceerden minder ontstekingsmoleculen, weerstonden celdood beter en waren minder geneigd om onder zware, ziekteachtige omstandigheden in botachtige cellen te veranderen.
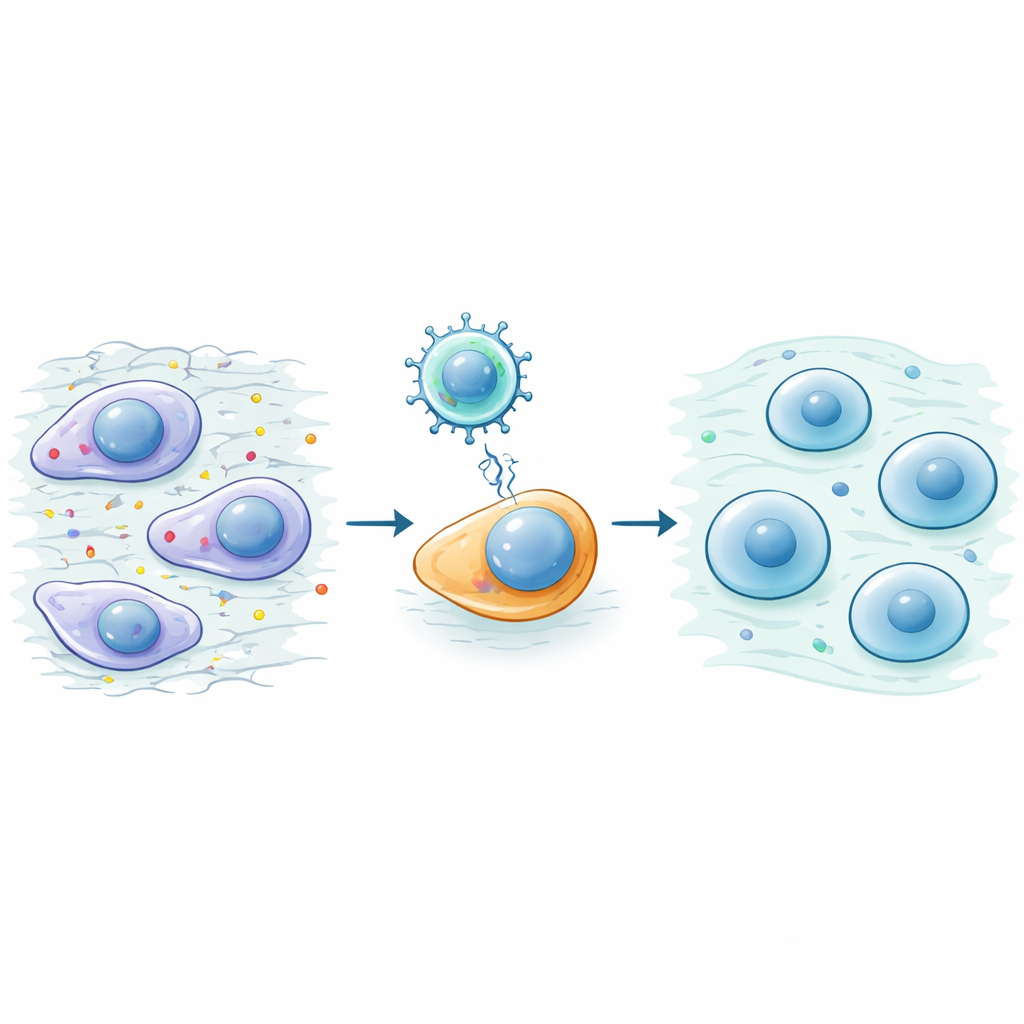
Beschermen en herbouwen van beschadigde gewrichten
Het team testte OSK vervolgens in twee standaard muismodellen van knieartrose die door chirurgisch letsel werden veroorzaakt. Muizen die de OSK-behandeling kregen bewogen beter, hadden een sterker grijpen en vertoonden minder pijn bij aanraking van hun poten. Scans van hun knieën toonden gladdere gewrichtsoppervlakken en minder abnormale botverdikking onder het kraakbeen. Onder de microscoop behielden OSK-behandelde gewrichten meer van het oorspronkelijke, glanzende "hyaliene" kraakbeen en minder plekken met stijf fibrocartilage. Nuttige bouwstenen van kraakbeen bleven behouden, terwijl destructieve en "overgroeide" merkers die afbraak en littekenvorming signaleren verminderd waren. Opmerkelijk genoeg werkte OSK ook wanneer het later in de ziekte werd toegediend, en duwde het al gevormde fibrocartilage in de richting van een meer normale, hyaline-achtige toestand.
Het epigenetische code van verouderend kraakbeen resetten
Buiten structuur en pijnverlichting vroeg het team zich af of OSK de diepere moleculaire tekenen van veroudering in gewrichtsweefsel verandert. Ze richtten zich op DNA-methylering, een chemisch etiketteringssysteem op DNA dat fungeert als een epigenetische klok. In artrotisch kraakbeen loopt deze klok te snel: verouderingsmarkers stijgen en genen die ontsteking en weefselkwaliteit regelen zijn verkeerd gereguleerd. Door methylering over het hele genoom in kaart te brengen, vonden de onderzoekers dat OSK-behandeld kraakbeen er "jonger" uitzag dan verwacht voor zijn leeftijd en duidelijk verschilde van onbehandeld ziek weefsel. De therapie dempte de expressie van een DNA-methylerend enzym dat aan kraakbeenveroudering is gekoppeld en verhoogde een ander enzym, TET2, dat helpt methyleringsmerken te wissen. Toen TET2 opzettelijk werd geblokkeerd, verdwenen veel van de beschermende effecten van OSK, wat dit enzym als een belangrijke bemiddelaar benadrukt.
Wat dit kan betekenen voor toekomstige zorg
Gezamenlijk wijzen de bevindingen erop dat zorgvuldig afgestemde toediening van OSK-factoren in de knie verouderende, zieke kraakbeencellen gedeeltelijk kan herprogrammeren zonder ze te veranderen in ongecontroleerde stamcellen. Bij muizen verlichtte deze benadering pijn, beschermde de gewrichtsstructuur en zette het zelfs littekenachtig fibrocartilage terug in de richting van de oorspronkelijke, dempende vorm—veranderingen die overeenkomen met een meetbare "jongere" epigenetische toestand. Hoewel er nog veel werk resteert om veiligheid, dosering en langetermijneffecten bij grotere dieren en mensen te testen, biedt deze studie een vroege blik op een toekomst waarin de behandeling van artrose niet alleen gericht is op het verzachten van symptomen, maar op het herschrijven van de verouderingscode van gewrichtsweefsels zelf.
Bronvermelding: Liu, YW., Zou, JT., Gong, JS. et al. Local delivery of OSK factors enables partial cellular reprogramming to mitigate osteoarthritis and cartilage fibrosis. Exp Mol Med 58, 782–797 (2026). https://doi.org/10.1038/s12276-026-01662-x
Trefwoorden: artrose, kraakbeenregeneratie, cellulaire herprogrammering, epigenetica, gentherapie