Clear Sky Science · pl
Lokalne dostarczanie czynników OSK umożliwia częściowe przeprogramowanie komórek w celu złagodzenia choroby zwyrodnieniowej stawów i włóknienia chrząstki
Dlaczego to ważne przy bolących stawach
Choroba zwyrodnieniowa stawu kolanowego jest jedną z głównych przyczyn bólu i niepełnosprawności, a obecne terapie w przeważającej mierze maskują objawy zamiast odbudowywać uszkodzoną chrząstkę. Badanie to bada odważną koncepcję medycyny regeneracyjnej: delikatne „zresetowanie” komórek starzejącego się stawu przy użyciu trzech biologicznych przełączników zwanych czynnikami OSK, dostarczonych bezpośrednio do kolana. Wyniki sugerują, że być może możliwe jest nie tylko spowolnienie uszkodzeń stawu, lecz także odwrócenie części bliznowacenia i sztywności, które utrudniają codzienne poruszanie się.
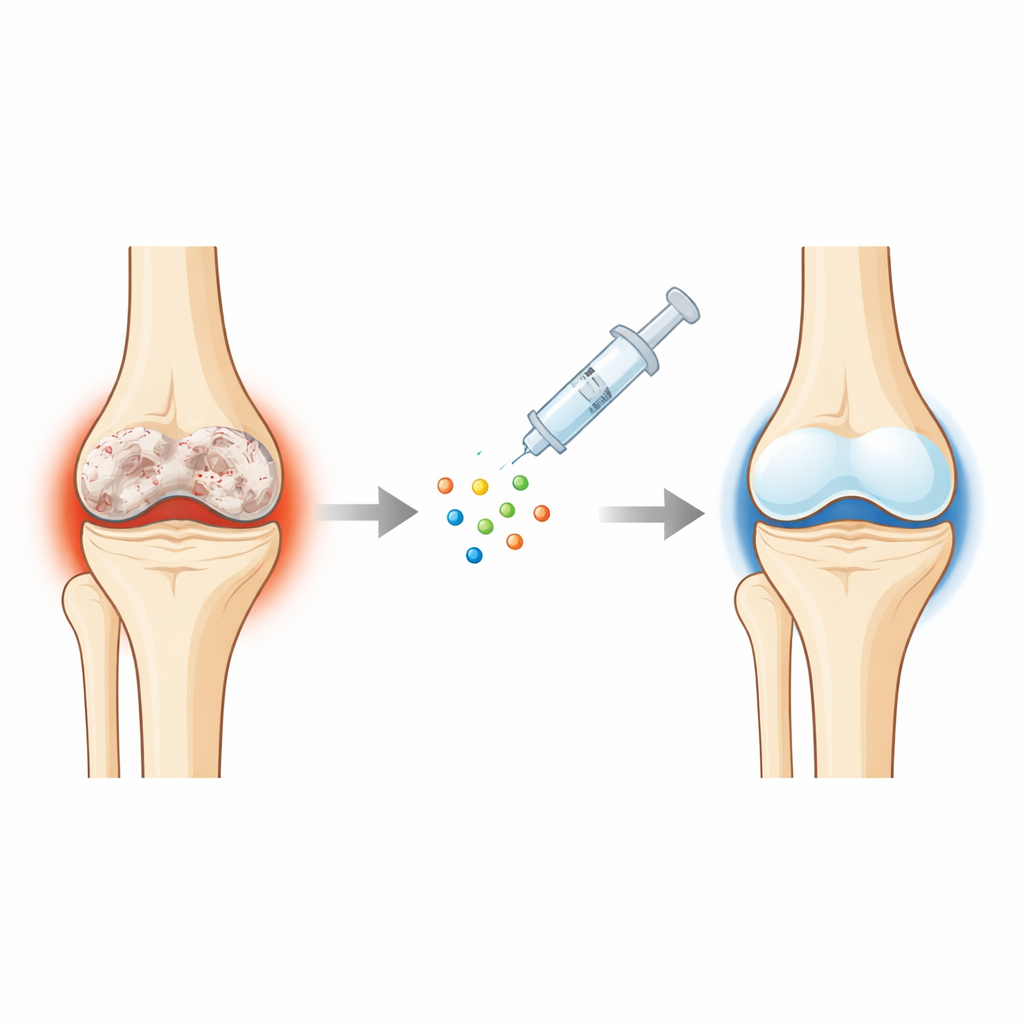
Bliższe spojrzenie na zużytą chrząstkę
W chorobie zwyrodnieniowej gładka, biała chrząstka amortyzująca końce kości stopniowo się rozkłada. Pod nią kość staje się grubsza, powierzchnia staje się chropowata, a elastyczną warstwę zastępuje włóknista tkanka przypominająca bliznę. Komórki utrzymujące chrząstkę, chondrocyty, pod wpływem wieku, przeciążenia i zapalenia przechodzą w szkodliwy stan: wywołują stan zapalny w otoczeniu, częściej ulegają śmierci i zaczynają zachowywać się bardziej jak komórki tworzące kość. Ponieważ chrząstka ma niewielkie unaczynienie i mało komórek naprawczych, gdy ten proces się rozpocznie, trudno go odwrócić, co pozostawia pacjentów z bólem, obrzękiem i utratą sprawności ruchowej.
Delikatne cofanie zegara komórkowego
Naukowcy odkryli, że pewne przełączniki genowe potrafią cofnąć wewnętrzny „wiek” komórki, ale zbyt silne działanie może przekształcić normalne tkanki w komórki macierzyste podatne na tworzenie nowotworów. Aby uniknąć tego ryzyka, autorzy użyli tylko trzech czynników — Oct4, Sox2 i Klf4, znanych łącznie jako OSK — pomijając czwarty, bardziej ryzykowny składnik. Zamknęli OSK w nieszkodliwym wektorze wirusowym i wstrzyknięli go bezpośrednio do stawów kolanowych myszy. W hodowlach komórkowych komórki chrząstki wystawione na działanie OSK zachowywały swoją tożsamość, jednocześnie stając się bardziej odporne: produkowały mniej związków prozapalnych, lepiej opierały się śmierci komórkowej i rzadziej przechodziły w komórki o cechach kostnych nawet w surowych, chorobowych warunkach.
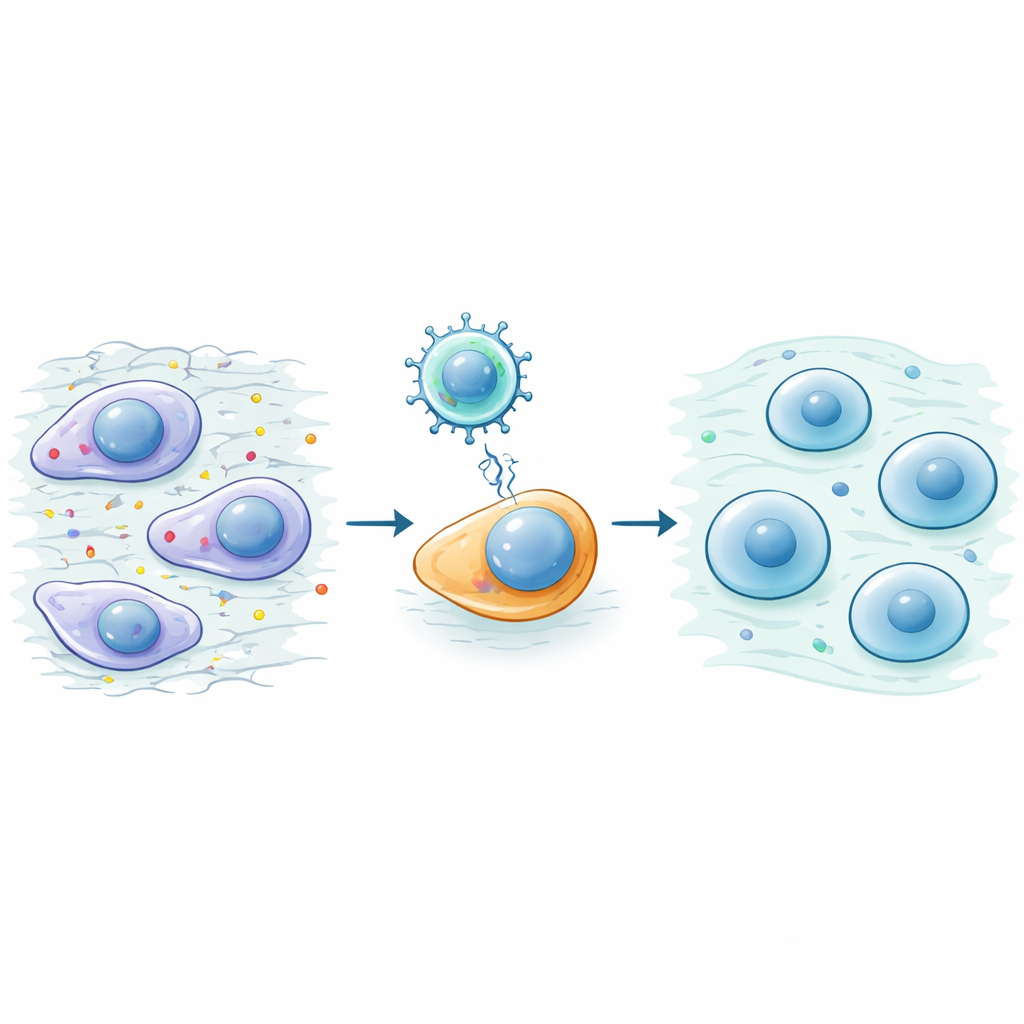
Ochrona i odbudowa uszkodzonych stawów
Zespół następnie przetestował OSK w dwóch standardowych modelach mysich zwyrodnień stawu kolanowego wywołanych urazem chirurgicznym. Myszy otrzymujące leczenie OSK poruszały się lepiej, miały mocniejszy chwyt i odczuwały mniejszy ból przy dotyku łap. Obrazowania kolan ujawniły gładsze powierzchnie stawowe i mniejsze nieprawidłowe pogrubienie kości pod chrząstką. Pod mikroskopem stawy leczone OSK zachowały więcej oryginalnej, szklistej chrząstki „hialinowej” i mniej obszarów twardej fibrochrząstki. Zachowane zostały korzystne składniki budulcowe chrząstki, podczas gdy markery związane z rozkładem i bliznowaceniem zostały zredukowane. Co istotne, OSK działał także przy późniejszym podaniu w przebiegu choroby, skłaniając już powstałą fibrochrząstkę ku bardziej normalnemu, przypominającemu hialinę stanowi.
Resetowanie epigenetycznego kodu starzejącej się chrząstki
Ponad strukturą i ulgą w bólu badacze sprawdzili, czy OSK zmienia głębsze molekularne oznaki starzenia w tkance stawowej. Skoncentrowali się na metylacji DNA, chemicznym znakowaniu DNA działającym jak epigenetyczny zegar. W chrząstce dotkniętej chorobą zwyrodnieniową ten zegar przyspiesza: wzrastają markery starzenia, a geny kontrolujące stan zapalny i jakość tkanki są nieprawidłowo regulowane. Poprzez profilowanie metylacji w całym genomie zespół stwierdził, że chrząstka leczona OSK wyglądała „młodziej” niż należałoby się spodziewać po jej wieku i wyraźnie różniła się od nieleczonej, chorej tkanki. Terapia osłabiła ekspresję enzymu metylującego DNA, powiązanego ze starzeniem chrząstki, i zwiększyła poziom innego enzymu, TET2, który pomaga usuwać znaki metylacyjne. Gdy TET2 został celowo zablokowany, wiele ochronnych efektów OSK zniknęło, wskazując na ten enzym jako kluczowego pośrednika.
Co to może oznaczać dla przyszłej opieki
Podsumowując, wyniki sugerują, że starannie dostrojone dostarczenie czynników OSK do kolana może częściowo przeprogramować starzejące się, chore komórki chrząstki bez przekształcania ich w niekontrolowane komórki macierzyste. U myszy takie podejście łagodzi ból, chroni strukturę stawu, a nawet przekształca włóknistą, bliznowatą chrząstkę z powrotem w bardziej pierwotną, amortyzującą formę — zmiany zgodne z mierzalnym „młodszym” stanem epigenetycznym. Choć przed nami jeszcze dużo pracy nad bezpieczeństwem, dawkowaniem i długoterminowymi skutkami u większych zwierząt i ludzi, badanie to daje wczesne spojrzenie na przyszłość, w której leczenie choroby zwyrodnieniowej stawów ma na celu nie tylko łagodzenie objawów, lecz także przepisanie kodu starzenia samych tkanek stawów.
Cytowanie: Liu, YW., Zou, JT., Gong, JS. et al. Local delivery of OSK factors enables partial cellular reprogramming to mitigate osteoarthritis and cartilage fibrosis. Exp Mol Med 58, 782–797 (2026). https://doi.org/10.1038/s12276-026-01662-x
Słowa kluczowe: choroba zwyrodnieniowa stawów, regeneracja chrząstki, przeprogramowanie komórkowe, epigenetyka, terapia genowa