Clear Sky Science · tr
HIV-1 proteaz inhibitörleri olarak koltuk kenarı ve zikzak grafen kuantum noktalarının karşılaştırmalı çalışması
HIV ile Mücadelede Küçük Bir Karbon Aracı
HIV’in kendini kopyalamasını engelleyen ilaçlar ölümcül bir enfeksiyonu yönetilebilir bir duruma dönüştürdü, ancak virüs mevcut ilaçlara karşı direnç geliştirebiliyor. Bu çalışma, grafen kuantum noktalarından — yalnızca birkaç milyarıncı metre genişliğinde ultra küçük karbon parçacıkları — inşa edilen yeni bir aday ilacı araştırıyor; bu parçacıkların HIV-1 proteazı adlı önemli bir viral enzime bağlanıp onu potansiyel olarak devre dışı bırakıp bırakamayacağını inceliyor.
Bu Karbon Noktalarını Özel Kılan Nedir
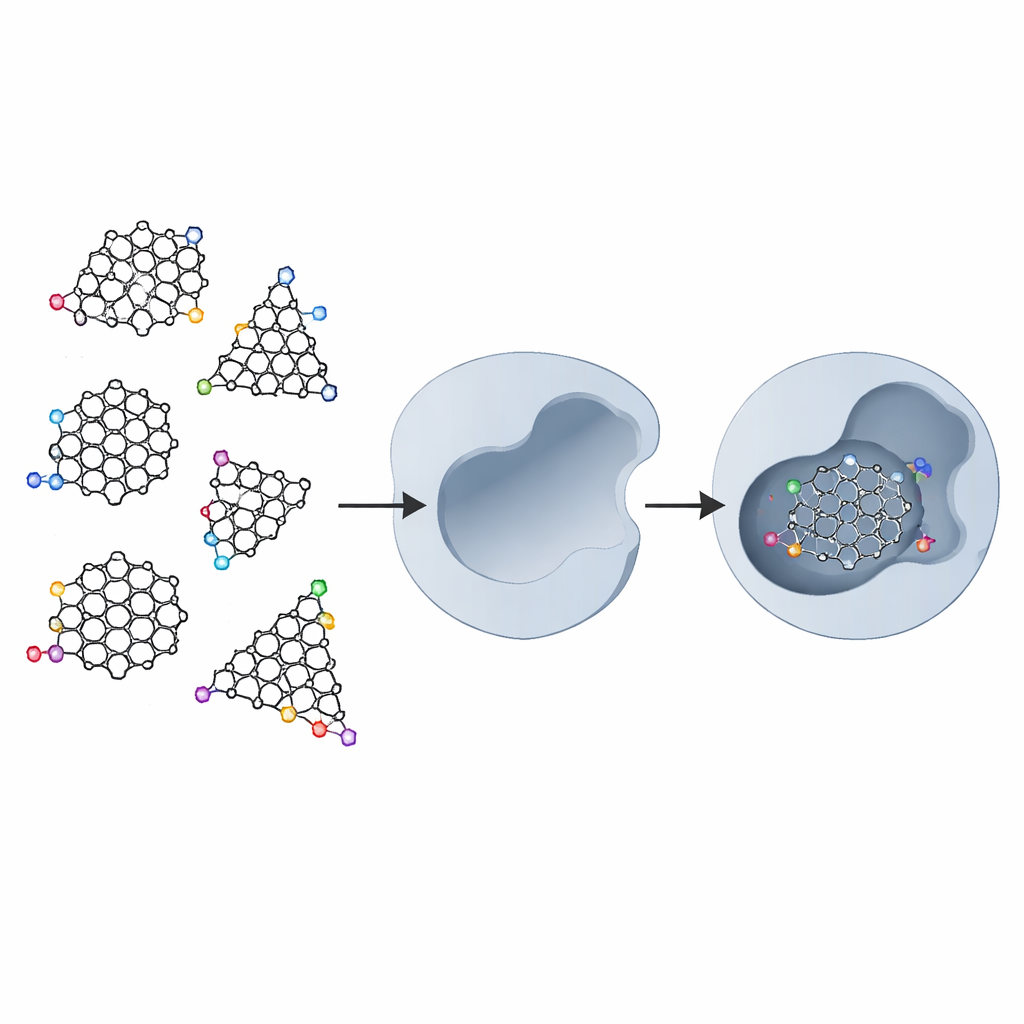
Grafen, tavuk tel örgüsü gibi düzenlenmiş karbon atomlarından oluşan bir tabakadır. Bu tabaka çok küçük parçalara, yani grafen kuantum noktalarına bölündüğünde, elektronlar çok sınırlı bir alana hapsolduğu ve parçaların kenarları kimyasal olarak aktif hale geldiği için yeni davranışlar kazanır. Noktalar üçgen veya altıgen şekillerde kesilebilir ve sınırlarında "armchair" (koltuk kenarı) veya "zigzag" atom dizilimleri gibi farklı desenler bulunabilir. Buna ek olarak, kimyagerler kenarlara su içinde çözünürlüğü ve biyomoleküllerle etkileşimi iyileştirmek için ekstra kimyasal gruplar bağlayabilir. Bu birleşik özellikler, grafen kuantum noktalarını sadece elektronik ve görüntüleme için değil, aynı zamanda tıp için de umut verici araçlar haline getiriyor.
Karbon Tabanlı Proteaz Engelleyiciler Tasarlamak
Araştırmacılar beş temel grafen kuantum noktası tipini inceledi: düz bir levha, armchair kenarlı üçgen ve altıgen parçalar ile zigzag kenarlı üçgen ve altıgen parçalar. Bunların her birini önce küçük bir halka (pirrolidin), bir benzen halkası ve son olarak iki hidroksimetilkarbonil (HMC) grubu ile "süslediler". HMC grupları, HIV-1 proteazın aktif bölgesinin merkezinde bulunan iki aspartik asit birimiyle hidrojen bağı oluşturabildikleri için seçildi. Gerçek enzimin çevresindeki aminoasitlerin çoğu suyu sevmeyen (hidrofobik) yapıdayken, bu iki aspartik asit suyu seven (hidrofilik) davranış sergiler ve dikkatle yerleştirilmiş kimyasal kancalar için doğal bir kenetlenme noktası yaratır.
Bilgisayarda Reaktivitenin Test Edilmesi
Islak laboratuvar yerine, ekip bu tasarım noktalarının nasıl davrandığını tahmin etmek için yüksek düzeyli kuantum kimyası hesaplamaları kullandı. Her yapıyı optimize ettiler ve toplam dipol momenti (yük dağılımının ne kadar düzensiz olduğunu ölçen bir değer) ve en yüksek dolu ile en düşük boş elektron durumları arasındaki enerji boşluğu gibi kimyasal reaktiviteyi gösteren nicelikleri hesapladılar. Büyük bir dipol momenti ile küçük bir boşluk genellikle bir molekülün etkileşime daha istekli olduğunu gösterir. Tüm tasarımlar arasında, pirrolidin ve HMC grupları bağlı zigzag kenarlı üçgen bir nokta öne çıktı; en yüksek polariteyi ve en küçük boşluğu sergiledi. Bilim insanları ayrıca elektron bulutunun her nokta üzerinde nasıl dağıldığını ve kaç elektronik durumun mevcut olduğunu incelediler ve belirli şekil ve kenar desenlerinin malzemeyi daha tepkisel kıldığını daha da doğruladılar.
Noktaların Enzimi Ne Kadar İyi Tutabildiğini Görmek
Bu kuantum noktalarının gerçekten HIV-1 proteaza kenetlenip kenetlenemeyeceğini anlamak için araştırmacılar, enzimin aktif bölgesini taklit eden iki aspartik asit birimiyle etkileşimlerini simüle ettiler. Moleküller arası atomların kuantum teorisi (QTAIM) adı verilen bir yöntem kullanarak bağların oluşabileceği elektron yoğunluğunun ince ayrıntılarını incelediler. Tüm modifiye edilmiş noktalar kararlı kompleksler oluşturdu, ancak HMC grupları bağlı zigzag üçgen tasarım özellikle güçlü etkileşimler sergiledi; bazı bağlantılar kısmen kovalent bir karakter aldı — geçici bir çekimden ziyade gerçek bir kimyasal bağa daha yakın. Bir diğer önemli faktör boyuttu: en iyi uyum sağlayan yapı, pirrolidin, benzen ve iki HMC grubu ile modifiye edilmiş saf bir levha temelinde yaklaşık 9.3 angström genişliğindeydi ve bu da gerçek proteaz aktif bölgesinin yaklaşık 10 angström genişliğindeki boşluğuyla güzelce eşleşiyordu.
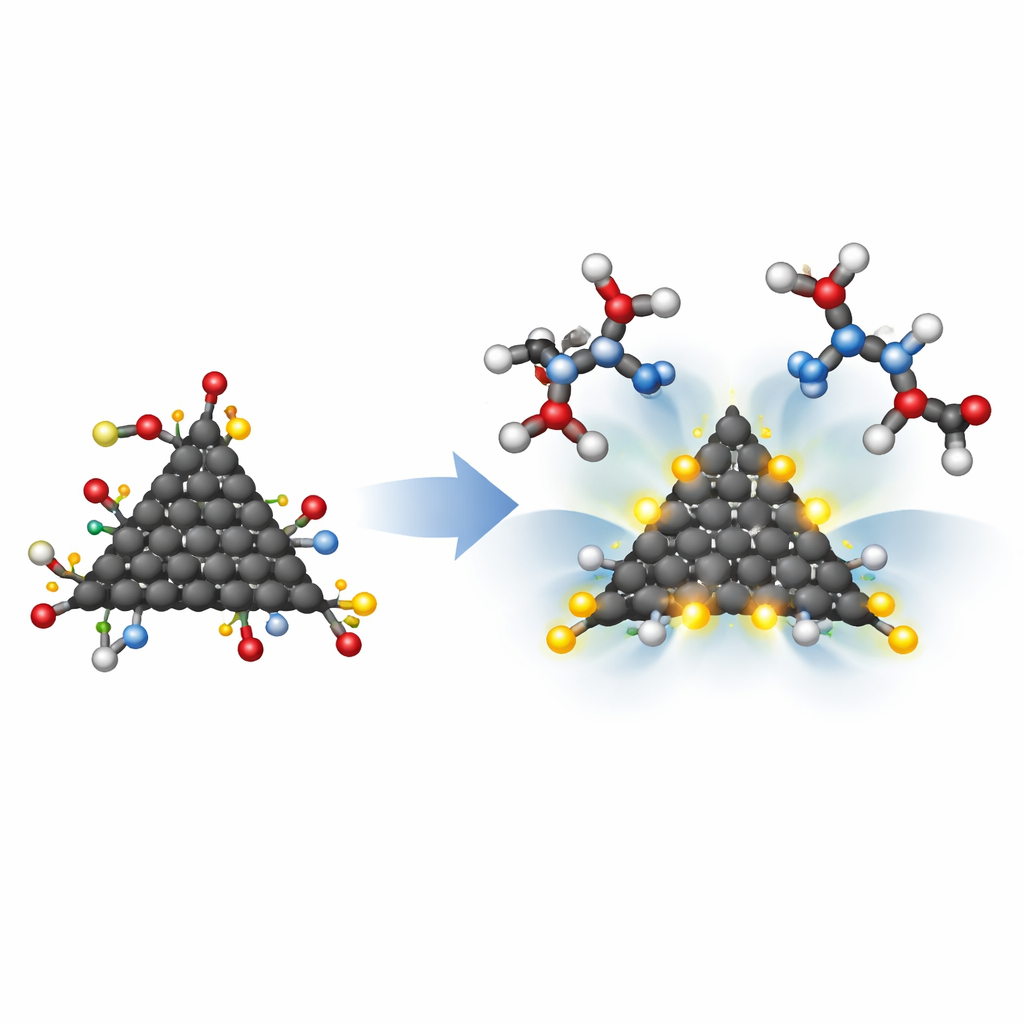
Gelecekteki HIV Tedavileri İçin Neden Önemli
Zeki nano-mühendislik ile ayrıntılı bilgisayar modellemesini birleştirerek bu çalışma, küçük karbon noktalarının hem HIV-1 proteaz cebine sığacak hem de anahtar aspartik asit kalıntılarına sağlam biçimde tutunacak şekilde tasarlanabileceğini gösteriyor. En umut verici versiyonlar, enzim boşluğuna girebilecek kadar küçük, güçlü hidrojen bağları kuracak kadar polar ve bağlandıktan sonra elektronik olarak kararlıydı. Bunlar hazır ilaçlar olmaktan ziyade erken, teorik sonuçlar olsa da, şekil, kenar deseni ve bağlanmış kimyasal grupların grafen kuantum noktalarının HIV-1 proteaz inhibitörü olarak davranma kapasitesini birlikte nasıl kontrol ettiğine dair bir yol haritası çiziyor. Bu yol haritası gelecekte karbon bazlı yeni bir antiviral materyal sınıfının tasarımını yönlendirebilir.
Atıf: Ibrahim, A., Elhaes, H. & Ibrahim, M.A. Comparative study of armchair and zigzag graphene quantum dots as HIV-1 protease inhibitors. Sci Rep 16, 14650 (2026). https://doi.org/10.1038/s41598-026-48709-7
Anahtar kelimeler: grafen kuantum noktaları, HIV-1 proteaz, nanotıp, hesaplamalı ilaç tasarımı, karbon nanomalzemeler