Clear Sky Science · fr
Étude comparative des points quantiques de graphène à bords « armchair » et « zigzag » en tant qu’inhibiteurs de la protéase du VIH-1
Un minuscule outil de carbone dans la lutte contre le VIH
Les médicaments qui empêchent le VIH de se répliquer ont transformé une infection mortelle en une maladie contrôlable, mais le virus peut encore évoluer et devenir résistant aux traitements existants. Cette étude explore un nouveau type de candidat-médicament constitué de points quantiques de graphène — des flocons de carbone ultra-petits, de quelques milliardièmes de mètre — pour évaluer s’ils peuvent se fixer sur une enzyme virale clé, la protéase du VIH-1, et potentiellement l’inhiber.
Ce qui rend ces points de carbone particuliers
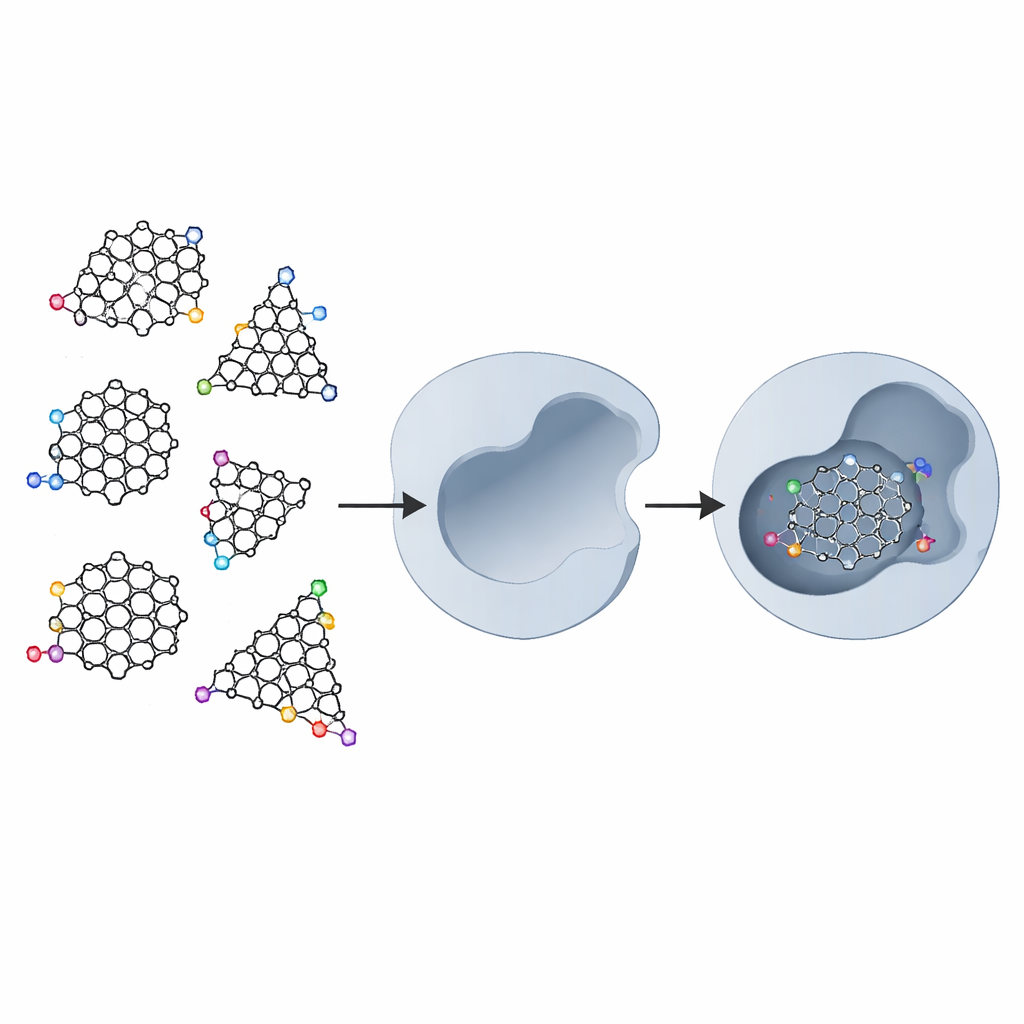
Le graphène est une feuille d’atomes de carbone disposés comme un grillage. Lorsqu’on découpe cette feuille en fragments très petits, appelés points quantiques de graphène, elle acquiert de nouveaux comportements parce que les électrons sont confinés dans un espace minuscule et parce que les bords des fragments deviennent chimiquement actifs. Les points peuvent être découpés en formes triangulaires ou hexagonales, et leurs bordures peuvent présenter différents agencements — configurations « armchair » ou « zigzag » des atomes. De plus, les chimistes peuvent fixer des groupes chimiques supplémentaires sur les bords pour améliorer leur solubilité dans l’eau et leurs interactions avec les molécules biologiques. Ces caractéristiques combinées font des points quantiques de graphène des outils prometteurs non seulement pour l’électronique et l’imagerie, mais aussi pour la médecine.
Conception d’inhibiteurs de protéase à base de carbone
Les chercheurs ont examiné cinq types de base de points quantiques de graphène : une feuille simple, des fragments triangulaires et hexagonaux à bords armchair, et des fragments triangulaires et hexagonaux à bords zigzag. Ils ont ensuite « décoré » chacun de ces modèles par un petit cycle (pyrrolidine), un anneau benzénique, et enfin deux groupes hydroxyméthylcarbonyl (HMC). Les groupes HMC ont été choisis parce qu’ils peuvent former des liaisons hydrogène avec deux unités d’acide aspartique situées au cœur du site actif de la protéase du VIH-1. Dans l’enzyme réelle, presque tous les acides aminés environnants sont hydrophobes, mais ces deux acides aspartiques sont hydrophiles, créant un site d’accostage naturel pour des crochets chimiques placés de façon précise.
Tester la réactivité sur ordinateur
Plutôt que d’effectuer des expériences en laboratoire humide, l’équipe a utilisé des calculs de chimie quantique de haut niveau pour prédire le comportement de ces points conçus. Ils ont optimisé chaque structure et calculé des grandeurs révélatrices de la réactivité chimique, telles que le moment dipolaire total (une mesure de la répartition asymétrique de la charge) et l’écart d’énergie entre les états électroniques occupés et inoccupés les plus élevés. Un moment dipolaire élevé combiné à un petit gap signifie généralement qu’une molécule est plus encline à interagir. Parmi tous les modèles, un point triangulaire à bords zigzag avec pyrrolidine et groupes HMC attachés s’est distingué, affichant la polarité la plus forte et le plus petit gap. Les scientifiques ont également étudié la répartition du nuage électronique sur chaque point et le nombre d’états électroniques disponibles, confirmant que certaines formes et certains motifs de bord rendent le matériau plus réactif.
Voir à quel point les points agrippent l’enzyme
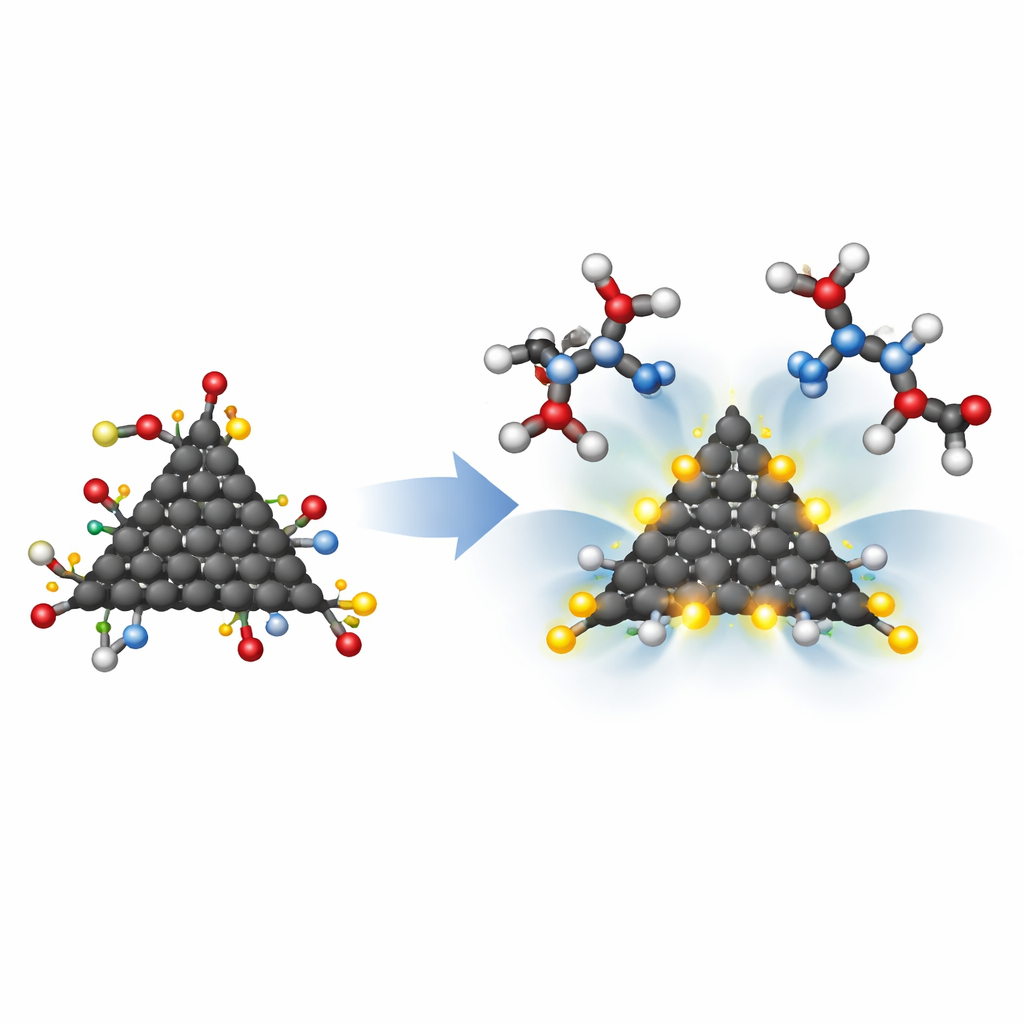
Pour comprendre si ces points quantiques pouvaient réellement se fixer sur la protéase du VIH-1, les chercheurs ont simulé leur interaction avec deux unités d’acide aspartique reproduisant le site actif de l’enzyme. En utilisant une méthode appelée théorie quantique des atomes dans les molécules, ils ont examiné les détails fins de la densité électronique là où des liaisons pourraient se former. Tous les points modifiés ont formé des complexes stables, mais la conception triangulaire à bords zigzag avec groupes HMC a montré des interactions particulièrement fortes, certaines prises présentant un caractère partiellement covalent — plus proche d’une vraie liaison chimique qu’une attraction passagère. Un autre facteur important est la taille : la structure s’ajustant le mieux, basée sur une feuille pristine modifiée par pyrrolidine, benzène et deux groupes HMC, mesurait environ 9,3 angströms de diamètre, correspondant bien à la cavité d’environ 10 angströms du site actif de la protéase réelle.
Pourquoi c’est important pour les futurs traitements du VIH
En combinant une nanoingénierie intelligente et une modélisation informatique détaillée, ce travail montre que de petits points de carbone peuvent être conçus pour s’insérer dans la poche de la protéase du VIH-1 et agripper fermement ses résidus clés d’acide aspartique. Les versions les plus prometteuses sont suffisamment petites pour pénétrer dans la cavité enzymatique, assez polaires et réactives pour former des liaisons hydrogène fortes, et électriquement stables une fois liées. Bien qu’il s’agisse de résultats théoriques préliminaires et non de médicaments prêts à l’emploi, ils tracent une feuille de route sur la façon dont la forme, le motif des bords et les groupes chimiques attachés aux points quantiques de graphène contrôlent conjointement leur capacité à agir comme inhibiteurs de la protéase du VIH-1. Cette feuille de route pourrait guider la conception d’une nouvelle classe de matériaux antiviraux à base de carbone à l’avenir.
Citation: Ibrahim, A., Elhaes, H. & Ibrahim, M.A. Comparative study of armchair and zigzag graphene quantum dots as HIV-1 protease inhibitors. Sci Rep 16, 14650 (2026). https://doi.org/10.1038/s41598-026-48709-7
Mots-clés: points quantiques de graphène, protéase du VIH-1, nanomédecine, conception de médicaments par calcul, nanomatériaux de carbone