Clear Sky Science · ru
Сравнительное исследование графеновых квантовых точек с «кресельной» и «зигзагообразной» кромкой как ингибиторов протеазы ВИЧ‑1
Крохотный углеродный инструмент в борьбе с ВИЧ
Лекарства, которые блокируют способность ВИЧ к размножению, превратили смертельную инфекцию в контролируемое состояние, но вирус всё ещё может эволюционировать и приобретать устойчивость к существующим препаратам. В этом исследовании рассматривается новый тип кандидата в лекарства, созданный из графеновых квантовых точек — ультра‑малых углеродных фрагментов размером в несколько миллиардных долей метра — чтобы выяснить, могут ли они прикрепляться к ключевому вирусному ферменту, протеазе ВИЧ‑1, и потенциально его блокировать.
Чем эти углеродные точки особенные
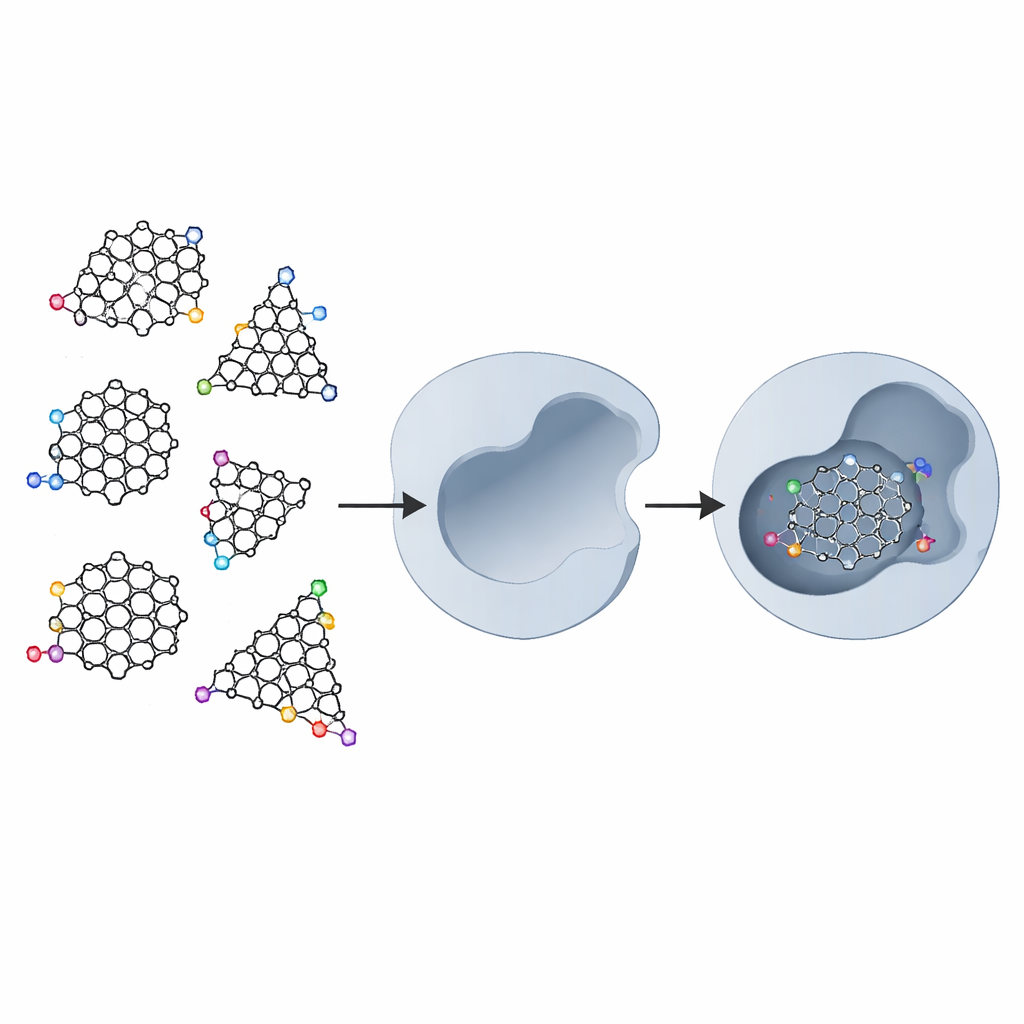
Графен — это лист углеродных атомов, устроенных как пчелиная сота. Когда такой лист разрезают на очень мелкие кусочки, называемые графеновыми квантовыми точками, у материала появляются новые свойства: электроны ограничены в малом объёме, а края фрагментов становятся химически активными. Точки можно вырезать в треугольной или шестиугольной форме, а их границы могут иметь разные узоры — «кресельную» (armchair) или «зигзагообразную» (zigzag) раскладку атомов. Кроме того, химики могут присоединять к краям дополнительные функциональные группы, чтобы улучшить растворимость в воде и взаимодействие с биомолекулами. В совокупности эти свойства делают графеновые квантовые точки перспективными не только для электроники и визуализации, но и для медицины.
Проектирование углеродных блокаторов протеазы
Исследователи рассмотрели пять базовых типов графеновых квантовых точек: незамещённый лист, треугольные и шестиугольные фрагменты с кресельными краями и треугольные и шестиугольные фрагменты с зигзагообразными краями. Затем каждую из этих конструкций «украшали» маленьким кольцом (пирролидином), бензольным кольцом и, наконец, двумя гидроксиметилкарбонильными (HMC) группами. HMC‑группы были выбраны потому, что они способны образовывать водородные связи с двумя остатками аспарагиновой кислоты, расположенными в центре активного участка протеазы ВИЧ‑1. В реальном ферменте почти все ближайшие аминокислоты гидрофобны, но эти две аспарагиновые кислоты гидрофильны, создавая естественную «стацию посадки» для аккуратно расположенных химических «крючков».
Тестирование реактивности на компьютере
Вместо работы в «мокрой» лаборатории команда использовала высокоуровневые вычисления квантовой химии, чтобы предсказать поведение этих дизайнерских точек. Они оптимизировали каждую структуру и рассчитали величины, указывающие на химическую реактивность, такие как полный дипольный момент (мера неравномерного распределения заряда) и энергетический разрыв между высшей занятой и низшей незанятой электронными состояниями. Большой дипольный момент в сочетании с малым разрывом обычно означает, что молекула готова к взаимодействию. Среди всех конструкций выделилась треугольная точка с зигзагообразной кромкой, модифицированная пирролидином и HMC‑группами: она показала наибольшую полярность и наименьший энергетический разрыв. Учёные также проанализировали распределение электронной плотности по каждой точке и число доступных электронных состояний, что дополнительно подтвердило: определённая форма и тип кромки делают материал более отзывчивым.
Оценка силы захвата фермента
Чтобы понять, смогут ли эти квантовые точки действительно сцепляться с протеазой ВИЧ‑1, исследователи смоделировали их взаимодействие с двумя остатками аспарагиновой кислоты, имитирующими активный сайт фермента. С помощью метода теории атомов в молекулах они изучили тонкие детали электронной плотности в местах возможного образования связей. Все модифицированные точки образовывали стабильные комплексы, но треугольная зигзагообразная конструкция с HMC‑группами проявила особенно сильные взаимодействия, причём некоторые контакты имели частично ковалентный характер — ближе к настоящей химической связи, чем к мимолётному притяжению. Другим важным фактором оказался размер: наиболее подходящая структура, основанная на цельном листе с присоединёнными пирролидином, бензолом и двумя HMC‑группами, имела размер около 9,3 ангстрема, что хорошо согласуется с примерно 10‑ангстремным объёмом каверны активного сайта настоящей протеазы.
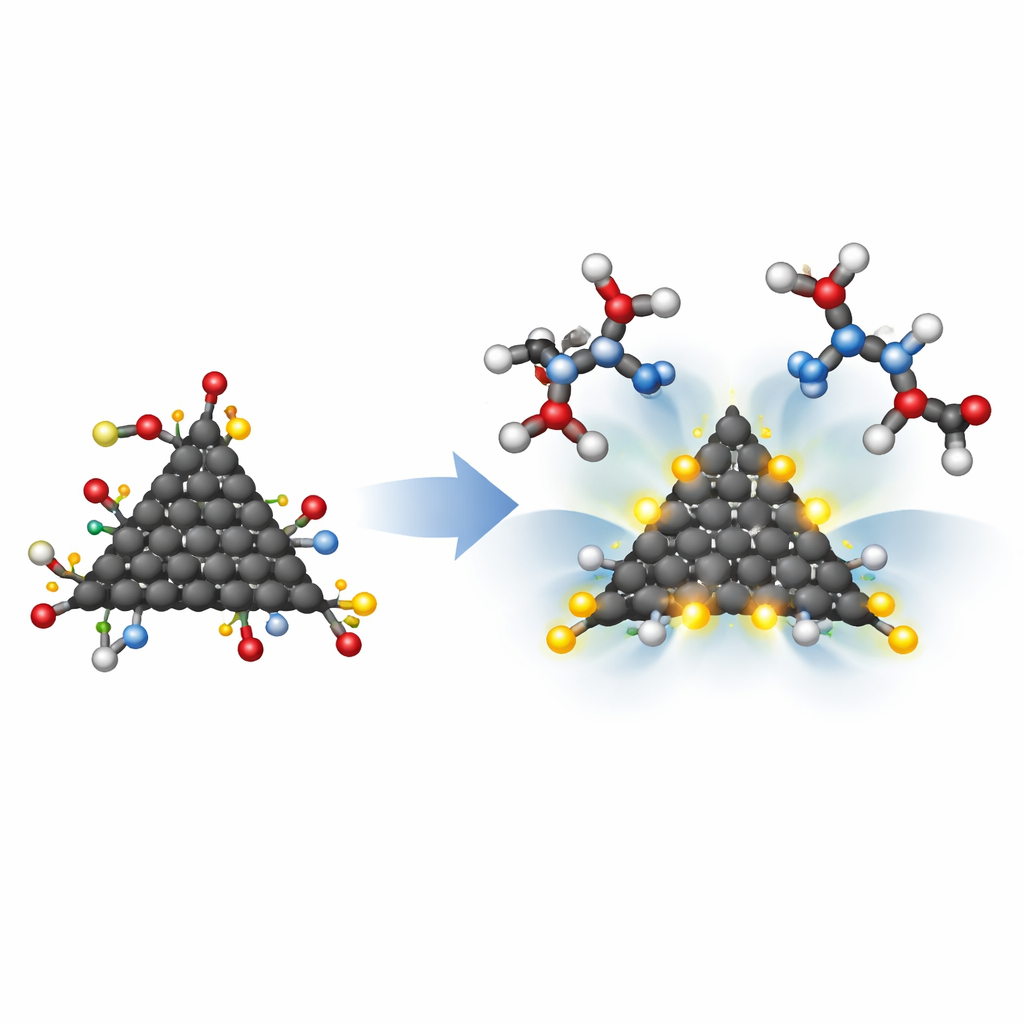
Почему это важно для будущих методов лечения ВИЧ
Сочетая продуманную нанотехнику и детальное компьютерное моделирование, эта работа показывает, что крошечные углеродные точки можно настроить так, чтобы они и поместились в карман протеазы ВИЧ‑1, и надёжно захватывали её ключевые остатки аспарагиновой кислоты. Наиболее перспективные варианты достаточно малы, чтобы проникать в полость фермента, полярны и реактивны для образования прочных водородных связей и электронно стабильны в связанном состоянии. Хотя это ранние теоретические результаты, а не готовые лекарства, они прокладывают дорожную карту: форма, тип кромки и присоединённые функциональные группы графеновых квантовых точек совместно определяют их способность выступать в роли ингибиторов протеазы ВИЧ‑1. Эта карта может направить разработку нового класса углеродных противовирусных материалов в будущем.
Цитирование: Ibrahim, A., Elhaes, H. & Ibrahim, M.A. Comparative study of armchair and zigzag graphene quantum dots as HIV-1 protease inhibitors. Sci Rep 16, 14650 (2026). https://doi.org/10.1038/s41598-026-48709-7
Ключевые слова: графеновые квантовые точки, протеаза ВИЧ‑1, наномедицина, компьютерное проектирование лекарств, углеродные наноматериалы