Clear Sky Science · nl
Vergelijkende studie van armchair- en zigzag-graphene-quantumdots als HIV-1-proteaseremmers
Een klein koolstofinstrument in de strijd tegen hiv
Geneesmiddelen die verhinderen dat hiv zich vermenigvuldigt hebben van een dodelijke infectie een behandelbare aandoening gemaakt, maar het virus kan nog steeds resistentie tegen bestaande middelen ontwikkelen. Deze studie onderzoekt een nieuw soort kandidaat-geneesmiddel opgebouwd uit graphene quantum dots — uiterst kleine koolstofvlokjes van slechts enkele miljardsten van een meter — om na te gaan of ze zich aan een sleutelenzym van het virus, de HIV-1-protease, kunnen hechten en dat mogelijk kunnen uitschakelen.
Wat deze koolstofdruppels speciaal maakt
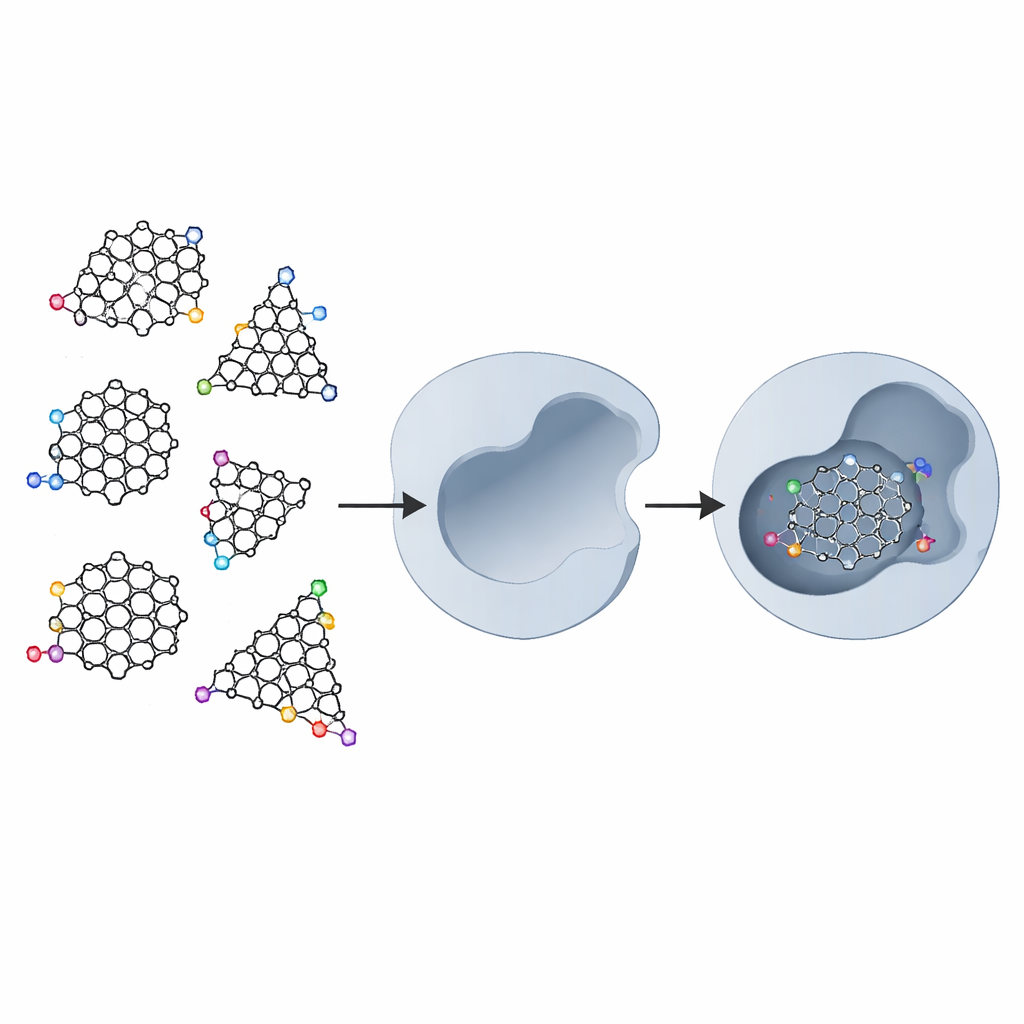
Graphene is een vel koolstofatomen gerangschikt als kippenrasters. Als dat vel in zeer kleine stukjes wordt gesneden — graphene quantum dots — ontstaan nieuwe eigenschappen doordat elektronen in zo’n krappe ruimte worden beperkt en omdat de randen van de stukjes chemisch actief worden. De dots kunnen in driehoekige of zeshoekige vormen worden gesneden en hun randen kunnen verschillende patronen hebben — “armchair” of “zigzag” atoomarrangementen. Daarnaast kunnen chemici extra chemische groepen aan de randen koppelen om de oplosbaarheid in water en de interactie met biologische moleculen te verbeteren. Deze gecombineerde eigenschappen maken graphene quantum dots veelbelovend, niet alleen voor elektronica en beeldvorming, maar ook voor toepassingen in de geneeskunde.
Ontwerpen van koolstofgebaseerde proteaseremmers
De onderzoekers bekeken vijf basistypen graphene quantum dots: een onbewerkt vel, driehoekige en zeshoekige stukjes met armchair-randen, en driehoekige en zeshoekige stukjes met zigzag-randen. Ze “decoreerden” elk van deze vervolgens met een klein ringetje (pyrrolidine), een benzeenring en tenslotte twee hydroxymethylcarbonyl (HMC)-groepen. De HMC-groepen werden gekozen omdat ze waterstofbruggen kunnen vormen met twee asparaginezuureenheden die in het hart van het actieve centrum van HIV-1-protease zitten. In het echte enzym zijn vrijwel alle nabije aminozuren waterafstotend (hydrofoob), maar deze twee asparaginezuren zijn waterminnend (hydrofoob), waardoor een natuurlijke dockingplaats ontstaat voor zorgvuldig geplaatste chemische haken.
Reactiviteit testen op de computer
In plaats van in een nat laboratorium te werken, gebruikte het team hoge-niveau kwantumchemische berekeningen om te voorspellen hoe deze ontworpen dots zich gedragen. Ze optimaliseerden elke structuur en berekenden grootheden die chemische reactiviteit aangeven, zoals het totale dipoolmoment (een maat voor hoe ongelijk lading verdeeld is) en de energiekloof tussen de hoogste bezette en laagste onbezet electronenbanen. Een groot dipoolmoment gecombineerd met een kleine kloof betekent doorgaans dat een molecuul gretiger is om te interageren. Onder alle ontwerpen viel een driehoekige dot met zigzag-rand en aangehechte pyrrolidine- en HMC-groepen op, met de hoogste polariteit en de kleinste kloof. De wetenschappers onderzochten ook hoe de elektronenwolk zich over elke dot verspreidt en hoeveel elektronische toestanden beschikbaar zijn, waarmee ze verder bevestigden dat bepaalde vormen en randpatronen het materiaal responsiever maken.
Beoordelen hoe goed de dots het enzym vastgrijpen
Om te begrijpen of deze quantum dots het HIV-1-protease echt stevig konden vastpakken, simuleerden de onderzoekers hun interactie met twee asparaginezuureenheden die het actieve centrum van het enzym nabootsen. Met een methode genaamd quantum theory of atoms in molecules onderzochten ze de fijne details van de elektrondichtheid waar bindingen zouden kunnen ontstaan. Alle gemodificeerde dots vormden stabiele complexen, maar het zigzag-driehoekontwerp met HMC-groepen toonde bijzonder sterke interacties, waarbij sommige contacten een deels covalente karakter aannamen — dichter bij een echte chemische binding dan bij een vluchtige aantrekking. Een andere belangrijke factor was grootte: de best passende structuur, gebaseerd op een onbewerkt vel aangepast met pyrrolidine, benzeen en twee HMC-groepen, had een diameter van circa 9,3 ångström, wat goed overeenkomt met de ongeveer 10 ångström brede holte van het echte actieve centrum van de protease.
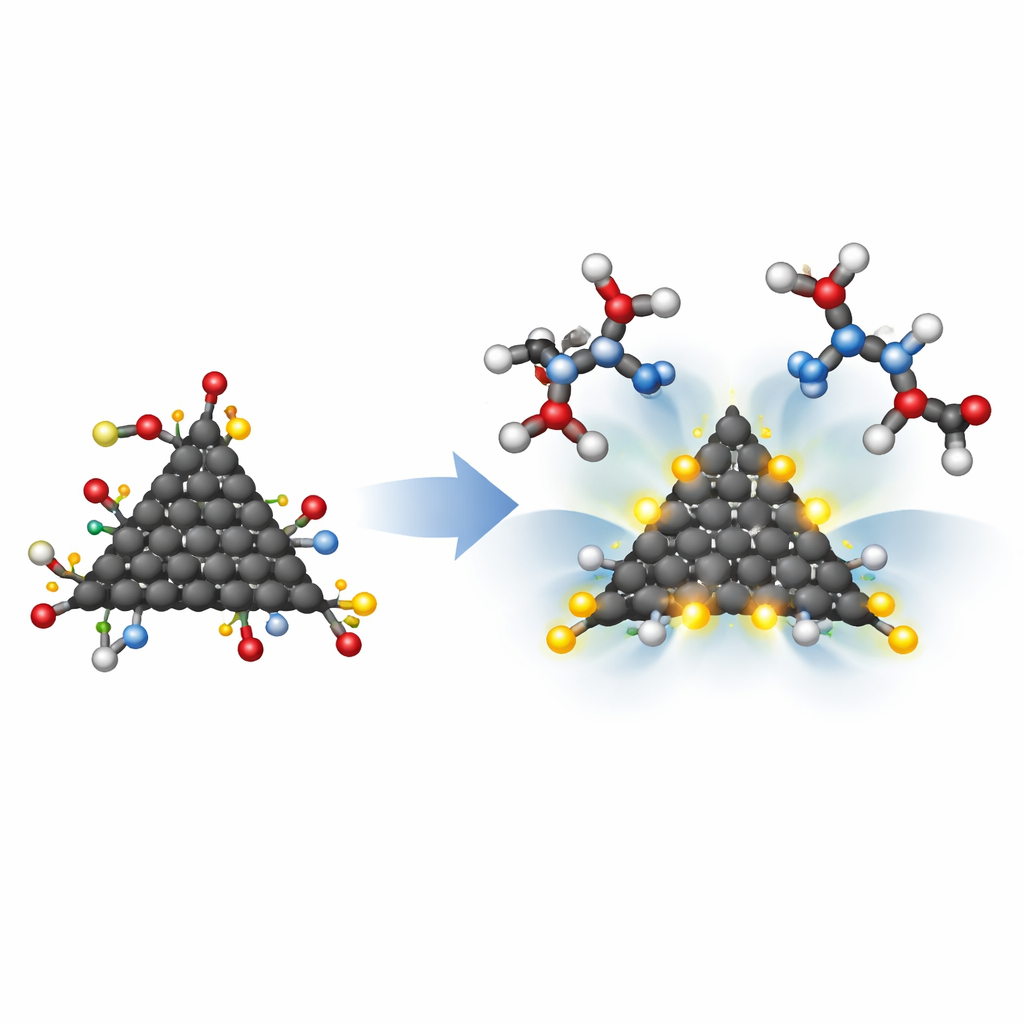
Waarom dit van belang is voor toekomstige hiv-behandelingen
Door slimme nano-engineering te combineren met gedetailleerde computermodellering toont dit werk aan dat kleine koolstofdruppels kunnen worden afgestemd om zowel in de HIV-1-proteasepocket te passen als zijn sleutel-asparaginezuurresiduen stevig vast te grijpen. De meest veelbelovende versies zijn klein genoeg om de enzymholte binnen te dringen, polair en reactief genoeg om sterke waterstofbruggen te vormen, en elektronisch stabiel zodra ze gebonden zijn. Hoewel het vroege, theoretische resultaten zijn en geen kant-en-klare geneesmiddelen, geven ze wel een routekaart voor hoe vorm, randpatroon en aangehechte chemische groepen van graphene quantum dots gezamenlijk hun vermogen bepalen om als HIV-1-proteaseremmers te fungeren. Die routekaart kan in de toekomst het ontwerp sturen van een nieuwe klasse koolstofgebaseerde antivirale materialen.
Bronvermelding: Ibrahim, A., Elhaes, H. & Ibrahim, M.A. Comparative study of armchair and zigzag graphene quantum dots as HIV-1 protease inhibitors. Sci Rep 16, 14650 (2026). https://doi.org/10.1038/s41598-026-48709-7
Trefwoorden: graphene quantum dots, HIV-1 protease, nanomedicine, computational drug design, carbon nanomaterials