Clear Sky Science · tr
Yakınsama analizi ve optimal kontrol içeren kesirli uzay‑zamansal Hahnfeldt tümör modeli
Kanserin “hafızasının” önemi
Kanser bir saksı bitkisi gibi basitçe büyümez. Tümörler şekil değiştirir, doku içinde yayılır ve geçmiş ilaç uygulamalarını ile bağışıklık saldırılarını “hatırlar”. Birçok standart matematiksel kanser modeli büyümeyi basit, hafızasız bir süreç olarak ele alır; bu da gerçek hastalarda görülen yavaş nüksleri, uyku dönemlerini ve düzensiz yayılımı kaçırabilir. Bu makale, tümörlerin hafızasını ve mekânsal özelliklerini doğrudan matematiğe dahil eden yeni bir yaklaşım sunarak kanserlerin nasıl büyüdüğünü ve kombinasyon tedavilerinin uzun vadede onları nasıl kontrol altında tutabileceğini daha iyi tahmin etmeyi amaçlıyor.
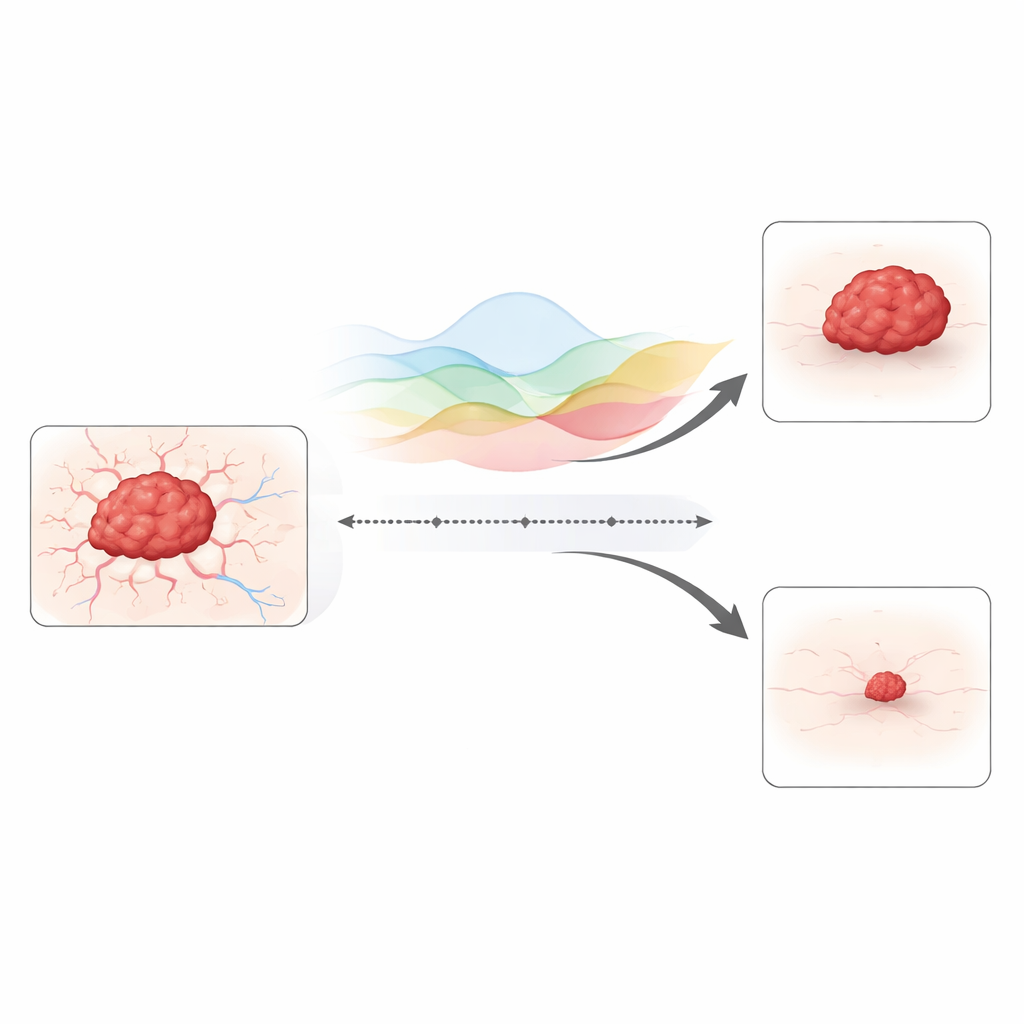
Tümör büyümesine hafıza eklemek
Çalışma, tümörün boyutunu onu besleyen kan damarlarıyla ilişkilendiren iyi bilinen bir modele dayanıyor. Klasik versiyonda değişimler zaman içinde adım adım ve geçmişten bağımsız olarak gerçekleşir. Burada yazar, bu basit zaman adımlarını “kesirli” bir zaman operatörü ile değiştiriyor; bu, bugünkü davranışın önceki tüm durumlara bağlı olmasına izin veren matematiksel bir araçtır. Biyolojik açıdan bu, dokuda kalan ilaç artıklarını, kan damarlarında uzun süreli hasarı ve tedaviden sonra aktif kalan bağışıklık hücrelerini yakalar. Model ayrıca tümör hücrelerinin ve damarların uzay içinde nasıl hareket edip yayıldığını takip ederek, düzgün bir hücre küresi yerine düzensiz, parmak benzeri invazyonları temsil edebilir.
Matematiği biyolojik olarak gerçekçi tutmak
Her yararlı kanser modeli negatif hücre sayıları veya sınırsız büyüme gibi imkânsız sonuçlardan kaçınmalıdır. Makale, makul başlangıç koşullarıyla bu çerçevedeki hem tümör hücrelerinin hem de kan damarlarının negatif olmadığını ve biyolojik olarak makul bir aralık içinde kaldığını kanıtlar. Yazar daha sonra alttaki denklemleri bilgisayarda çözmek için öngörücü‑düzeltici (predictor–corrector) yöntemi gibi belirli bir sayısal şemayı analiz eder. Hata sınırları ve kararlılık koşullarını belirleyerek, model uzun menzilli hafıza ve uzaysal yayılım içerse bile bu yönteme dayanan simülasyonların yalnızca görsel olarak ikna edici değil, matematiksel olarak da güvenilir olduğunu gösterir.
Simülasyonların ortaya koydukları
Bu çerçeveyi kullanarak makale, geleneksel hafızasız dinamikleri kesirli, hafıza‑zengin karşıtlarıyla karşılaştırır. “Hafıza gücü” yüksek olduğunda (klasik duruma yakın), tümörler hızla büyür ve sonra dengeye ulaşır; tedavi durduktan sonra hızlı şekilde geri sıçrama eğilimindedirler. Hafıza etkisi arttırıldıkça (kesirli türev mertebesi düştükçe) büyüme yavaşlar, tedaviye yanıtlar gecikir ve tümör uzun dönemli neredeyse uyku halinde kalabilir. Model ayrıca kanser hücreleri ve destekleyici damarlar doku içinde difüze olurken düzensiz invazyon cepheleri üretir; bu desen, görüntüleme ve patoloji çalışmalarında gerçek tümörlerde görülenlere daha yakındır.
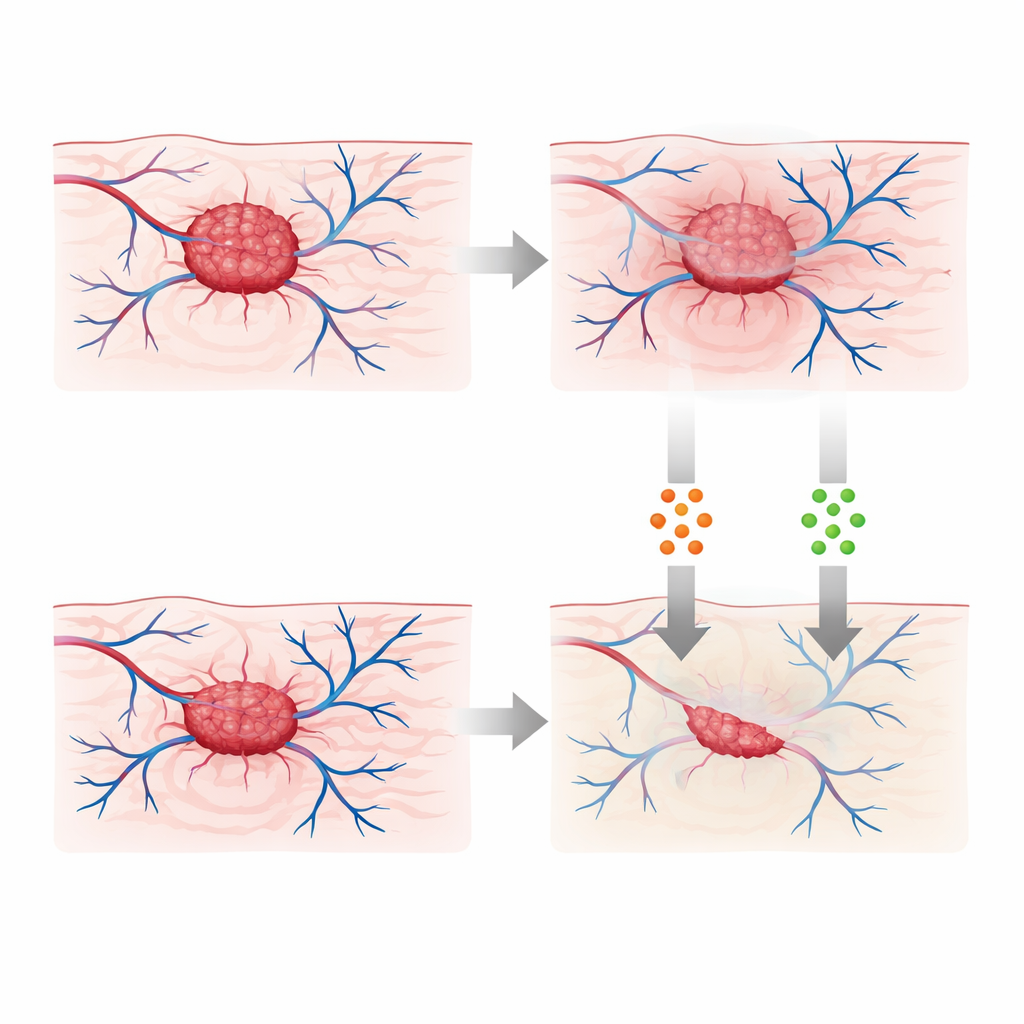
Daha akıllı kombinasyon terapileri tasarlamak
Çalışma pasif öngörülemenin ötesine geçip bu hafızayı tedavileri planlamak için nasıl kullanabileceğimizi araştırır. İki kontrol düğmesi tanıtarak kemoterapi ve immünoterapiyi temsil eder ve optimalizasyon problemi formüle eder: ilaç yükünü sınırlarken tümörü azaltmak. Standart kontrol teorisinin kesirli bir versiyonunu kullanarak, yazar sistemin hafızası olduğunda bu tedavilerin zaman içinde nasıl değişmesi gerektiğine dair kurallar türetir. Kemoterapi tek başına, immünoterapi tek başına ve kombine bir program olmak üzere üç senaryonun simülasyonları, kombinasyonun en derin ve en kalıcı tümör baskılanmasını sağladığını gösterir. Kesirli bağlamda, doku ve bağışıklık yanıtındaki biyolojik hafızayı yansıtarak tedavi durduktan sonra bile faydalar sürer.
Geleceğin kanser bakımına katkıları
Basitçe söylemek gerekirse makale, bir tümörün hafızasını ve yamalı yayılımını ciddiye almanın geleceği hakkında düşünme biçimimizi değiştirdiğini gösteriyor. Hafızayı dikkate alan modeller doğal olarak yavaş nüksleri, uzun sessiz dönemleri ve düzensiz invazyonu yeniden üretir—klinikte sık görülen ama daha basit denklemlerin kaçırdığı özellikler. Ayrıca dikkatle zamanlanmış kemoterapi ve immünoterapi kombinasyonlarının bu hafıza etkilerinden yararlanarak tümörleri daha uzun süre baskılı tutabileceğini, sürekli yüksek doz tedavi gerektirmeden bunu başarabileceğini öne sürer. Bu çalışma kuramsal düzeyde kalsa da, tedavi fikirlerini denemek için daha sadık bir matematiksel “oyun alanı” sunar ve her hastanın tümörünün nasıl büyüdüğünü, yayıldığını ve hatırladığını dikkate alan gerçekten kişiselleştirilmiş programlara rehberlik edebilir.
Atıf: Can, E. Fractional spatiotemporal Hahnfeldt tumor model with convergence analysis and optimal control. Sci Rep 16, 12549 (2026). https://doi.org/10.1038/s41598-026-41810-x
Anahtar kelimeler: tümör büyüme modellemesi, kesirli hesap, kemo‑immünoterapi, uzay‑zamansal kanser dinamiği, optimal tedavi kontrolü