Clear Sky Science · nl
Fractioneel spatiotemporaal Hahnfeldt-tumormodel met convergentieanalyse en optimaal bestuur
Waarom het „geheugen” van kanker ertoe doet
Kanker groeit niet simpelweg als een plant in een pot. Tumoren veranderen van vorm, verspreiden zich door weefsel en onthouden eerdere medicatie en immuunaanvallen. Veel standaard wiskundige modellen van kanker beschouwen groei als een eenvoudig, geheugenloos proces, wat trage terugvallen, perioden van dormantie en ongelijkmatige verspreiding bij echte patiënten kan missen. Dit artikel introduceert een nieuwe manier om tumoren te beschrijven die geheugen en ruimte rechtstreeks in de wiskunde opneemt, met als doel beter te voorspellen hoe kankers groeien en hoe combinatietherapieën ze op lange termijn onder controle kunnen houden.
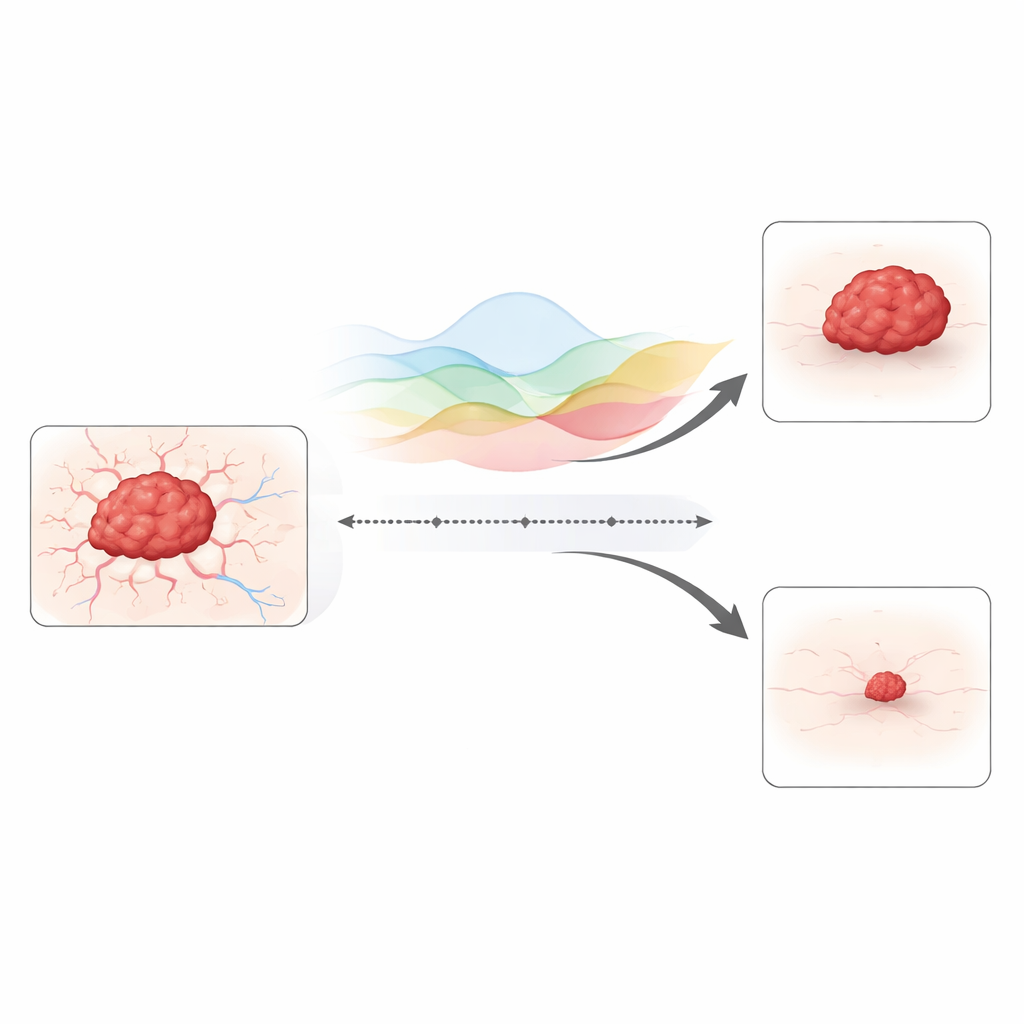
Geheugen toevoegen aan tumorgroei
De studie bouwt voort op een bekend model dat de omvang van een tumor koppelt aan de bloedvaten die haar voeden. In de klassieke versie vinden veranderingen stap voor stap in de tijd plaats, zonder afhankelijkheid van het verre verleden. Hier vervangt de auteur die eenvoudige tijdstappen door een „fractionele” tijdoperator, een wiskundig instrument waarmee het gedrag van vandaag afhankelijk kan zijn van alles wat eerder gebeurde. Biologisch gezien vangt dit achterblijvende medicijnresten in weefsel, langdurige schade aan bloedvaten en immuuncellen die na behandeling actief blijven. Het model houdt ook bij hoe kankercellen en bloedvaten zich door de ruimte verplaatsen en verspreiden, zodat het ongelijkmatige, vingerachtige invasies kan weergeven in plaats van een gladde, uniforme celsamenklontering.
De wiskunde biologisch realistisch houden
Elk nuttig kankermodel moet onmogelijke uitkomsten vermijden, zoals negatieve celaantallen of onbeperkte groei. Het artikel bewijst dat, met redelijke beginvoorwaarden, zowel tumorcellen als bloedvaten in dit kader niet-negatief blijven en binnen een biologisch plausibel bereik blijven. De auteur analyseert vervolgens een specifiek numeriek schema — een predictor–correctormethode — voor het oplossen van de onderliggende vergelijkingen op een computer. Door grenzen te stellen aan de fout en voorwaarden voor stabiliteit vast te leggen, toont het werk aan dat op deze methode gebaseerde simulaties niet alleen visueel overtuigend maar ook wiskundig betrouwbaar zijn, zelfs wanneer het model langafstandgeheugen en ruimtelijke verspreiding bevat.
Wat de simulaties onthullen
Met dit raamwerk vergelijkt het artikel traditionele, geheugenloze dynamieken met hun fractionele, geheugenvollere tegenhangers. Wanneer de „geheugenkracht” groot is (dicht bij het klassieke geval), groeien tumoren snel en vlakken ze vervolgens af, en hebben ze de neiging snel te herstellen nadat de behandeling stopt. Naarmate het geheugeneffect toeneemt (wat overeenkomt met een lagere fractionele orde), vertraagt de groei, worden reacties op therapie uitgesteld en kan de tumor lange perioden van bijna-dormantie ingaan. Het model produceert ook onregelmatige invasiefronten doordat kankercellen en ondersteunende bloedvaten door weefsel diffunderen, een patroon dat dichter bij wat beeldvorming en pathologie in echte tumoren laten zien ligt.
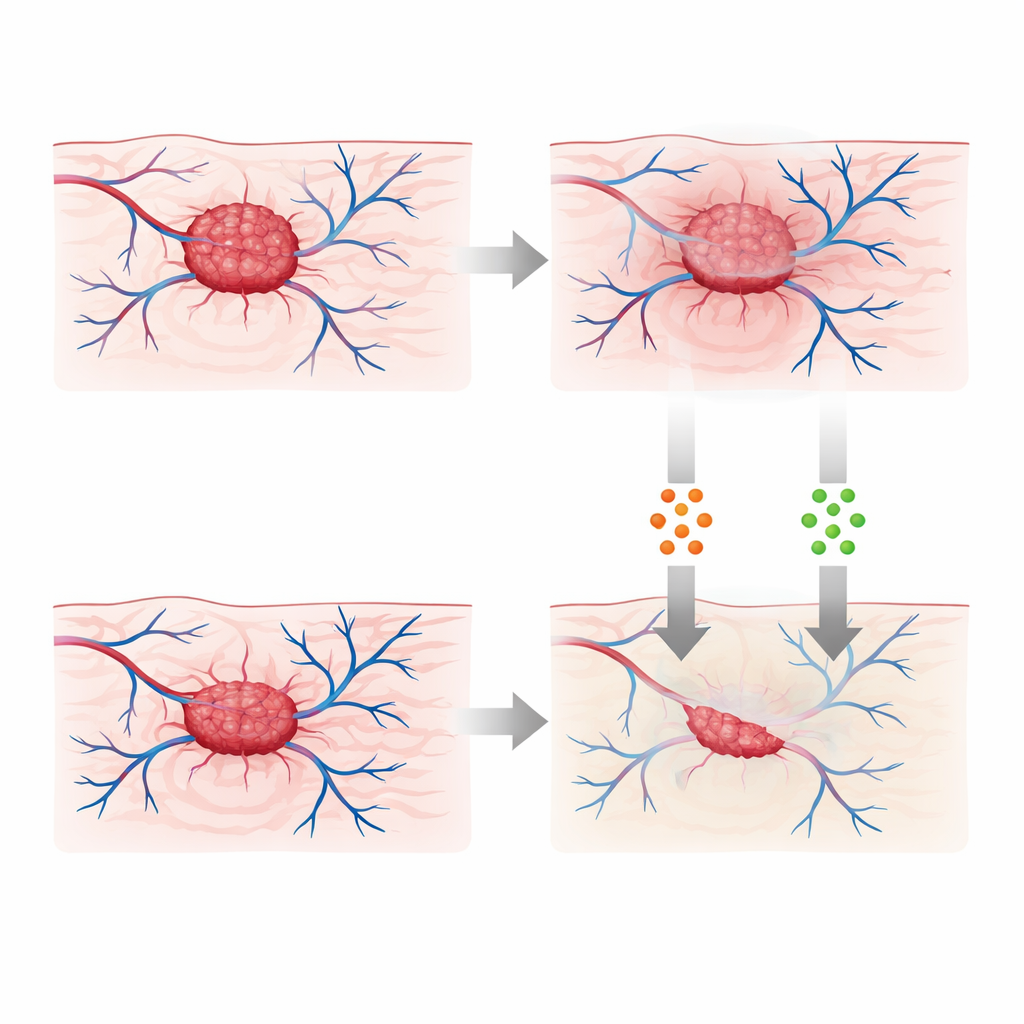
Het ontwerpen van slimmer gecombineerde therapieën
De studie gaat verder dan passieve voorspelling en onderzoekt hoe dit geheugen kan worden gebruikt om behandelingen te plannen. Het introduceert twee regelknoppen die chemotherapie en immunotherapie vertegenwoordigen en formuleert een optimalisatieprobleem: de tumor reduceren terwijl de geneesmiddellast beperkt blijft. Met een fractionele variant van standaard regeltheorie leidt de auteur regels af voor hoe deze behandelingen in de tijd zouden moeten variëren wanneer het systeem geheugen heeft. Simulaties van drie scenario’s — alleen chemotherapie, alleen immunotherapie en een gecombineerd schema — geven aan dat de combinatie leidt tot de diepste en meest blijvende tumordemping. In de fractionele setting blijven de voordelen van de behandeling aanhouden, zelfs nadat medicijnen zijn gestopt, wat het biologische geheugen in zowel weefsel als immuunrespons weerspiegelt.
Wat dit betekent voor de toekomstige kankerzorg
Simpel gezegd toont het artikel aan dat het serieus nemen van het geheugen en de ongelijkmatige verspreiding van een tumor verandert hoe we over haar toekomst denken. Geheugenbewuste modellen reproduceren vanzelf trage terugvallen, lange stille fasen en ongelijkmatige invasie — kenmerken die vaak in de kliniek worden gezien maar door eenvoudigere vergelijkingen worden gemist. Ze suggereren ook dat zorgvuldig getimede combinaties van chemo- en immunotherapie deze geheugeneffecten kunnen benutten om tumoren langer onderdrukt te houden, zonder constant hoge doseringen. Hoewel dit werk theoretisch blijft, biedt het een meer getrouwe wiskundige „zandbak” om behandelideeën te testen en zou het kunnen helpen bij het sturen van echt gepersonaliseerde schema’s die respect tonen voor hoe de tumor van elke patiënt groeit, zich verspreidt en onthoudt.
Bronvermelding: Can, E. Fractional spatiotemporal Hahnfeldt tumor model with convergence analysis and optimal control. Sci Rep 16, 12549 (2026). https://doi.org/10.1038/s41598-026-41810-x
Trefwoorden: tumorgroeimodellering, fractionele calculus, chemo-immunotherapie, spatiotemporele kankerdynamica, optimaal behandelbeleid