Clear Sky Science · pl
Ułamkowy przestrzenno‑czasowy model nowotworu typu Hahnfeldt z analizą zbieżności i sterowaniem optymalnym
Dlaczego „pamięć” nowotworu ma znaczenie
Nowotwór nie rośnie po prostu jak roślina w doniczce. Guzy zmieniają kształt, rozprzestrzeniają się przez tkanki i „pamiętają” przebyte leki oraz ataki układu odpornościowego. Wiele standardowych modeli matematycznych traktuje wzrost jako prosty proces bez pamięci, co może przeoczyć powolne nawroty, okresy uśpienia i nierównomierne rozprzestrzenianie się u prawdziwych pacjentów. W artykule wprowadzono nowe podejście do opisu guzów, które wprost wbudowuje pamięć i przestrzeń w równania, z zamiarem lepszego przewidywania wzrostu nowotworów oraz skuteczności terapii skojarzonych w dłuższej perspektywie.
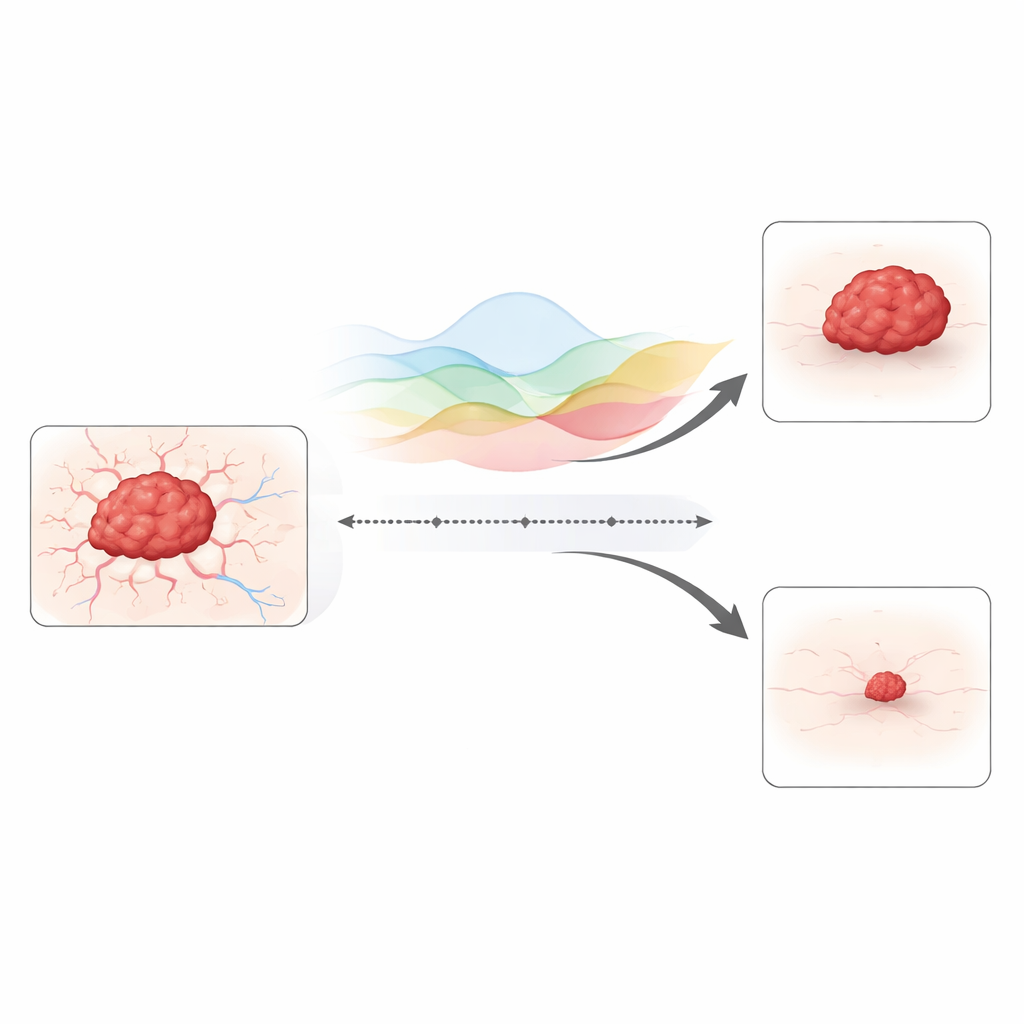
Dodanie pamięci do modelu wzrostu guza
Badanie opiera się na dobrze znanym modelu łączącym rozmiar guza z naczyniami krwionośnymi, które go odżywiają. W klasycznej wersji zmiany zachodzą krok po kroku w czasie, bez zależności od odległej przeszłości. Autor zastępuje te proste kroki czasowe operatorem „ułamkowym”, narzędziem matematycznym pozwalającym, by dzisiejsze zachowanie zależało od wszystkiego, co wydarzyło się wcześniej. W ujęciu biologicznym uwzględnia to pozostałości leków zalegające w tkance, długotrwałe uszkodzenia naczyń oraz komórki odpornościowe pozostające aktywne po terapii. Model śledzi też, jak komórki nowotworowe i naczynia krwionośne poruszają się i rozprzestrzeniają w przestrzeni, dzięki czemu może odzwierciedlać nierównomierną, palczastą inwazję zamiast gładkiej, jednolitej masy komórek.
Utrzymanie realizmu biologicznego w matematyce
Każdy użyteczny model nowotworu musi unikać niemożliwych rezultatów, takich jak ujemna liczba komórek czy nieograniczony wzrost. Artykuł dowodzi, że przy rozsądnych warunkach początkowych zarówno komórki nowotworowe, jak i naczynia w tym ramieniu pozostają nieujemne i mieszczą się w biologicznie wiarygodnym zakresie. Następnie autor analizuje konkretny schemat numeryczny — metodę predyktor‑korektor — do rozwiązywania równań na komputerze. Ustalając granice błędu i warunki stabilności, praca pokazuje, że symulacje oparte na tej metodzie są nie tylko przekonujące wizualnie, lecz także matematycznie wiarygodne, nawet gdy model zawiera długozasięgową pamięć i rozprzestrzenianie przestrzenne.
Co ujawniają symulacje
Korzystając z tego ramienia, artykuł porównuje tradycyjną, pozbawioną pamięci dynamikę z jej ułamkowymi, bogatymi w pamięć odpowiednikami. Gdy „siła pamięci” jest niewielka (bliska przypadkowi klasycznemu), guzy rosną szybko, a potem osiągają plateau i mają tendencję do szybkiego odbicia po zaprzestaniu leczenia. W miarę wzrostu efektu pamięci (odpowiadającego niższemu rzędowi ułamkowemu) wzrost zwalnia, reakcje na terapię się opóźniają, a guz może wejść w długie okresy niemal uśpienia. Model daje też nieregularne fronty inwazji, gdy komórki nowotworowe i naczynia dyfundują przez tkankę — wzór bliższy temu, co pokazują badania obrazowe i patologiczne w rzeczywistych guzach.
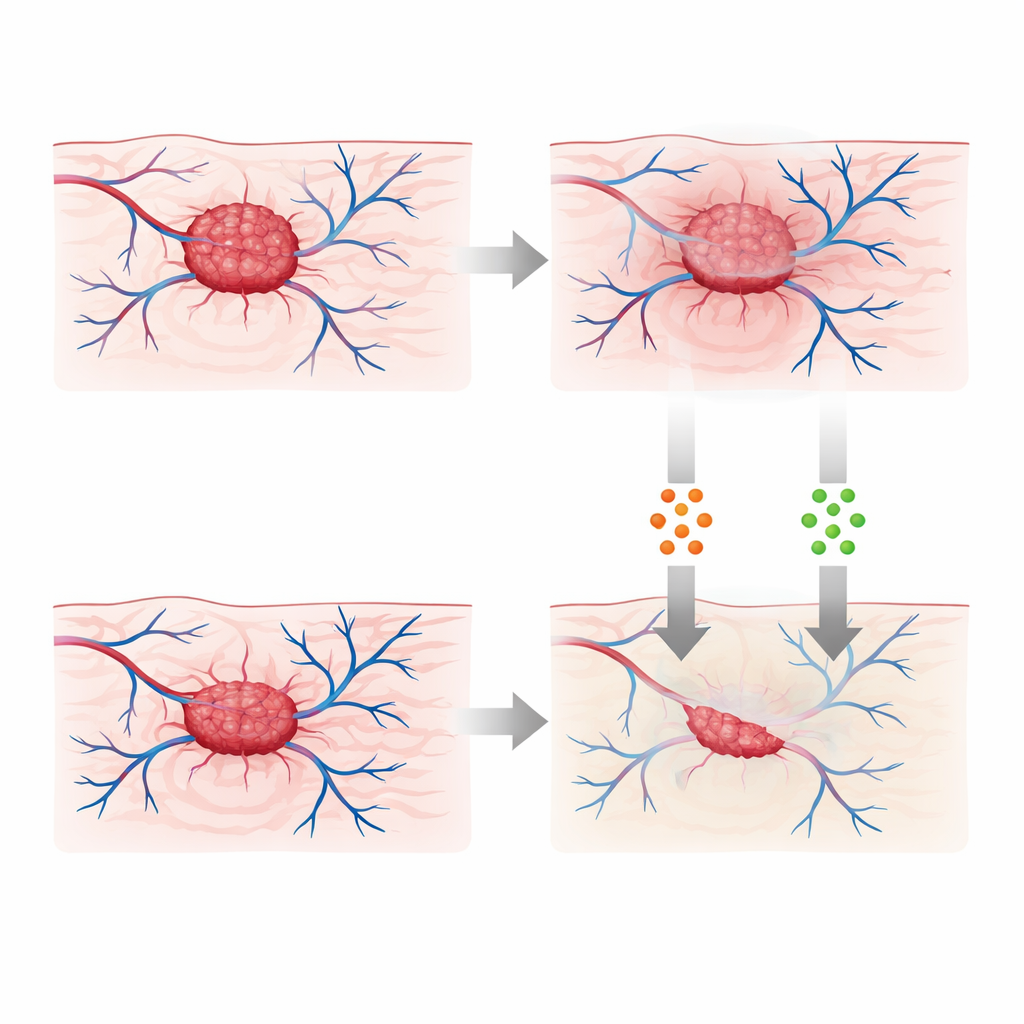
Projektowanie bardziej przemyślanych terapii skojarzonych
Badanie wykracza poza bierne przewidywanie i pyta, jak wykorzystać tę pamięć do planowania leczenia. Wprowadza dwa pokrętła sterujące reprezentujące chemioterapię i immunoterapię oraz formułuje problem optymalizacyjny: ograniczyć guz przy jednoczesnym zminimalizowaniu obciążenia lekowego. Korzystając z ułamkowej wersji standardowej teorii sterowania, autor wyprowadza reguły, jak powinny się zmieniać te terapie w czasie, gdy system ma pamięć. Symulacje trzech scenariuszy — sama chemioterapia, sama immunoterapia oraz schemat skojarzony — wskazują, że połączenie prowadzi do najgłębszego i najbardziej trwałego stłumienia guza. W ustawieniu ułamkowym korzyści z leczenia utrzymują się nawet po zaprzestaniu podawania leków, co odzwierciedla biologiczną pamięć tkanki i odpowiedzi immunologicznej.
Co to oznacza dla przyszłej opieki onkologicznej
Mówiąc wprost, artykuł pokazuje, że poważne potraktowanie pamięci guza i jego niejednorodnego rozprzestrzeniania zmienia sposób myślenia o jego przyszłości. Modele uwzględniające pamięć naturalnie odtwarzają powolne nawroty, długie ciche fazy i nierównomierną inwazję — cechy często obserwowane w praktyce klinicznej, a pomijane przez prostsze równania. Sugerują też, że starannie zaplanowane kombinacje chemioterapii i immunoterapii mogą wykorzystać te efekty pamięci, by dłużej utrzymywać supresję guza bez stałego stosowania wysokich dawek. Choć praca pozostaje teoretyczna, oferuje wierniejsze matematyczne „piaskowniczę” do testowania pomysłów terapeutycznych i może pomóc w tworzeniu naprawdę spersonalizowanych harmonogramów, które uwzględniają, jak guz konkretnego pacjenta rośnie, rozprzestrzenia się i pamięta.
Cytowanie: Can, E. Fractional spatiotemporal Hahnfeldt tumor model with convergence analysis and optimal control. Sci Rep 16, 12549 (2026). https://doi.org/10.1038/s41598-026-41810-x
Słowa kluczowe: modelowanie wzrostu guza, rachunek ułamkowy, chemo‑immunoterapia, przestrzenno‑czasowa dynamika raka, optymalne sterowanie leczeniem