Clear Sky Science · fr
Modèle fractionnaire spatiotemporel de Hahnfeldt pour la tumeur avec analyse de convergence et contrôle optimal
Pourquoi la « mémoire » du cancer compte
Le cancer ne croît pas simplement comme une plante en pot. Les tumeurs changent de forme, se propagent dans les tissus et conservent la trace des médicaments et des attaques immunitaires passés. Beaucoup de modèles mathématiques standards du cancer traitent la croissance comme un processus simple et sans mémoire, ce qui peut faire manquer des rechutes lentes, des périodes de dormance et une propagation inégale chez les patients réels. Cet article introduit une nouvelle façon de décrire les tumeurs qui intègre explicitement la mémoire et l’espace dans les équations, visant à mieux prédire la croissance des cancers et la façon dont des traitements combinés peuvent les contrôler à long terme.
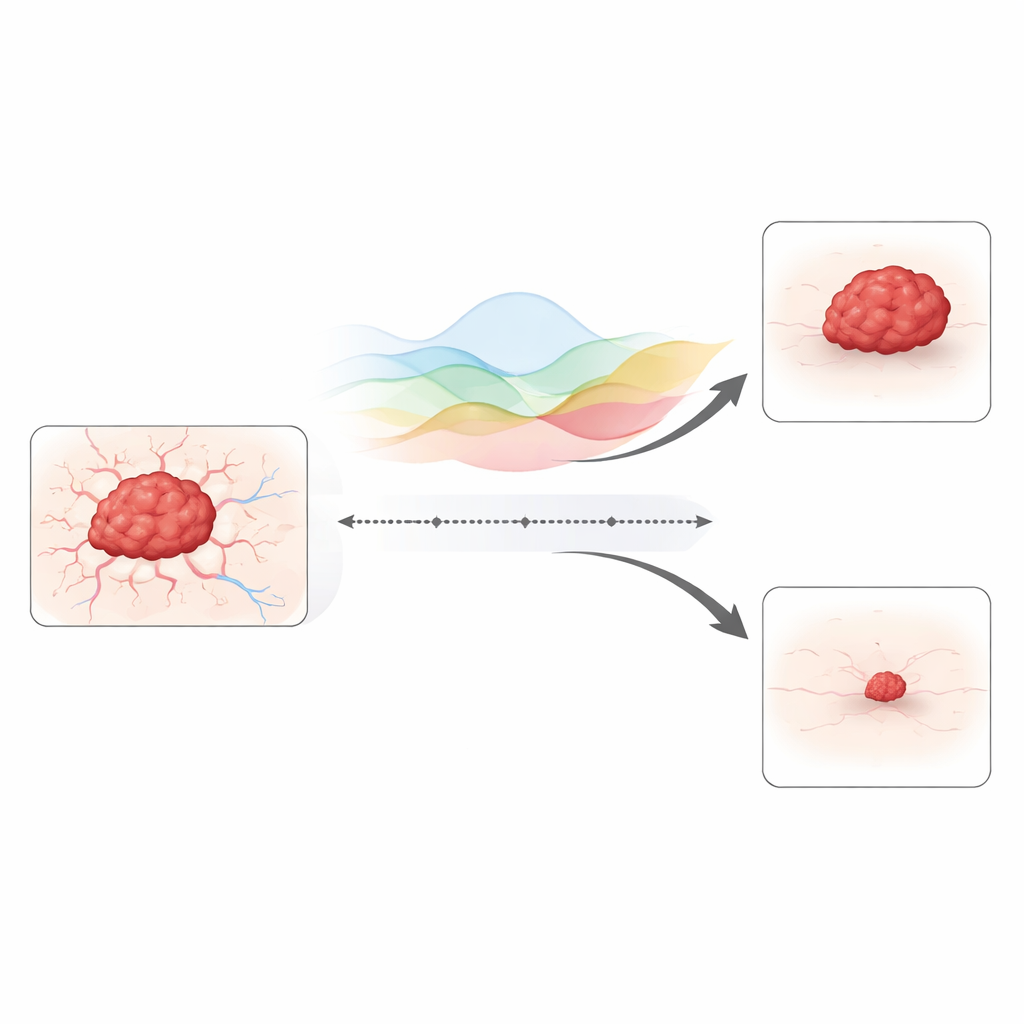
Ajouter la mémoire à la croissance tumorale
L’étude s’appuie sur un modèle bien connu qui relie la taille d’une tumeur aux vaisseaux sanguins qui l’alimentent. Dans la version classique, les variations se produisent pas à pas dans le temps, sans dépendance au passé lointain. Ici, l’auteur remplace ces pas temporels simples par un opérateur temporel « fractionnaire », un outil mathématique qui permet au comportement d’aujourd’hui de dépendre de tout ce qui s’est passé auparavant. En termes biologiques, cela capture les résidus de médicament qui persistent dans les tissus, les dommages durables aux vaisseaux sanguins et les cellules immunitaires qui restent actives après un traitement. Le modèle suit aussi comment les cellules tumorales et les vaisseaux sanguins se déplacent et se diffusent dans l’espace, de sorte qu’il peut représenter une invasion inégale en doigts plutôt qu’une masse uniforme et lisse de cellules.
Conserver un réalisme biologique dans les mathématiques
Tout modèle utile du cancer doit éviter des résultats impossibles comme des nombres négatifs de cellules ou une croissance illimitée. L’article démontre que, avec des conditions initiales raisonnables, à la fois les cellules tumorales et les vaisseaux sanguins dans ce cadre restent non négatifs et demeurent dans une plage biologiquement plausible. L’auteur analyse ensuite un schéma numérique spécifique — une méthode prédicteur‑correcteur — pour résoudre les équations sous‑jacentes sur ordinateur. En établissant des bornes sur l’erreur et des conditions de stabilité, le travail montre que les simulations basées sur cette méthode ne sont pas seulement convaincantes visuellement, mais aussi fiables mathématiquement, même lorsque le modèle inclut une mémoire à longue portée et une diffusion spatiale.
Ce que révèlent les simulations
À l’aide de ce cadre, l’article compare les dynamiques traditionnelles sans mémoire avec leurs homologues fractionnaires riches en mémoire. Lorsque la « force de la mémoire » est élevée (proche du cas classique), les tumeurs croissent rapidement puis se stabilisent, et elles ont tendance à rebondir rapidement après l’arrêt du traitement. À mesure que l’effet de mémoire augmente (correspondant à un ordre fractionnaire plus faible), la croissance ralentit, les réponses aux thérapies se font attendre, et la tumeur peut entrer dans de longues périodes de quasi‑dormance. Le modèle produit aussi des fronts d’invasion irréguliers lorsque les cellules cancéreuses et les vaisseaux de soutien diffusent dans les tissus, un motif plus proche de ce que montrent les images et les études de pathologie sur les tumeurs réelles.
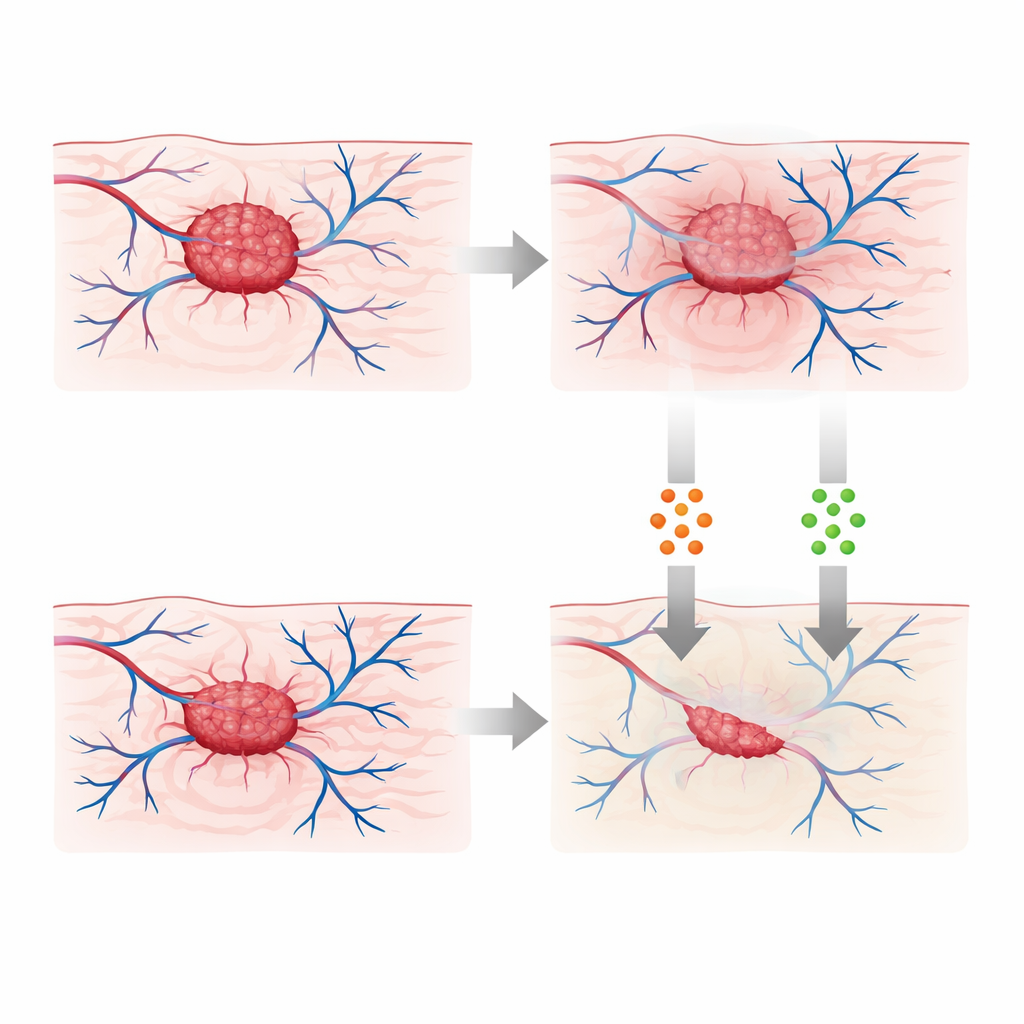
Concevoir des thérapies combinées plus intelligentes
L’étude va au‑delà de la simple prédiction et s’interroge sur la façon d’exploiter cette mémoire pour planifier les traitements. Elle introduit deux leviers de contrôle représentant la chimiothérapie et l’immunothérapie et formule un problème d’optimisation : réduire la tumeur tout en limitant la charge médicamenteuse. En utilisant une version fractionnaire de la théorie du contrôle standard, l’auteur dérive des règles pour la variation de ces traitements dans le temps lorsque le système possède une mémoire. Des simulations de trois scénarios — chimiothérapie seule, immunothérapie seule et un schéma combiné — indiquent que la combinaison conduit à la suppression tumorale la plus profonde et la plus persistante. Dans le cadre fractionnaire, les bénéfices du traitement se prolongent même après l’arrêt des médicaments, reflétant la mémoire biologique du tissu et de la réponse immunitaire.
Ce que cela implique pour les soins contre le cancer
En termes simples, l’article montre que prendre au sérieux la mémoire et la propagation inégale d’une tumeur change notre façon de penser son avenir. Les modèles sensibles à la mémoire reproduisent naturellement les rechutes lentes, les longues phases silencieuses et l’invasion inégale — caractéristiques souvent observées en clinique mais manquées par des équations plus simples. Ils suggèrent aussi que des combinaisons bien synchronisées de chimiothérapie et d’immunothérapie peuvent exploiter ces effets de mémoire pour maintenir les tumeurs sous contrôle plus longtemps, sans traitement continu à haute dose. Bien que ce travail reste théorique, il offre un « bac à sable » mathématique plus fidèle pour tester des idées de traitement et pourrait aider à orienter des calendriers véritablement personnalisés qui respectent la façon dont la tumeur de chaque patient croît, se propage et se souvient.
Citation: Can, E. Fractional spatiotemporal Hahnfeldt tumor model with convergence analysis and optimal control. Sci Rep 16, 12549 (2026). https://doi.org/10.1038/s41598-026-41810-x
Mots-clés: modélisation de la croissance tumorale, calcul fractionnaire, chimiothérapie-immunothérapie, dynamique spatiotemporelle du cancer, contrôle optimal du traitement