Clear Sky Science · ru
Дробная пространственно-временная модель опухоли Ханфельдта с анализом сходимости и оптимальным управлением
Почему «память» рака имеет значение
Рак растёт не просто как растение в горшке. Опухоли меняют форму, проникают в ткани и «помнят» прошлые лекарственные воздействия и атаки иммунной системы. Многие стандартные математические модели рассматривают рост как простой процесс без памяти, что может не фиксировать медленные рецидивы, периоды покоя и неравномерное распространение в реальных пациентах. В этой работе предложен новый подход к описанию опухолей, который прямо встраивает в математику память и пространство, с целью лучше предсказывать, как растут опухоли и как комбинированные терапии могут удерживать их под контролем в долгосрочной перспективе.
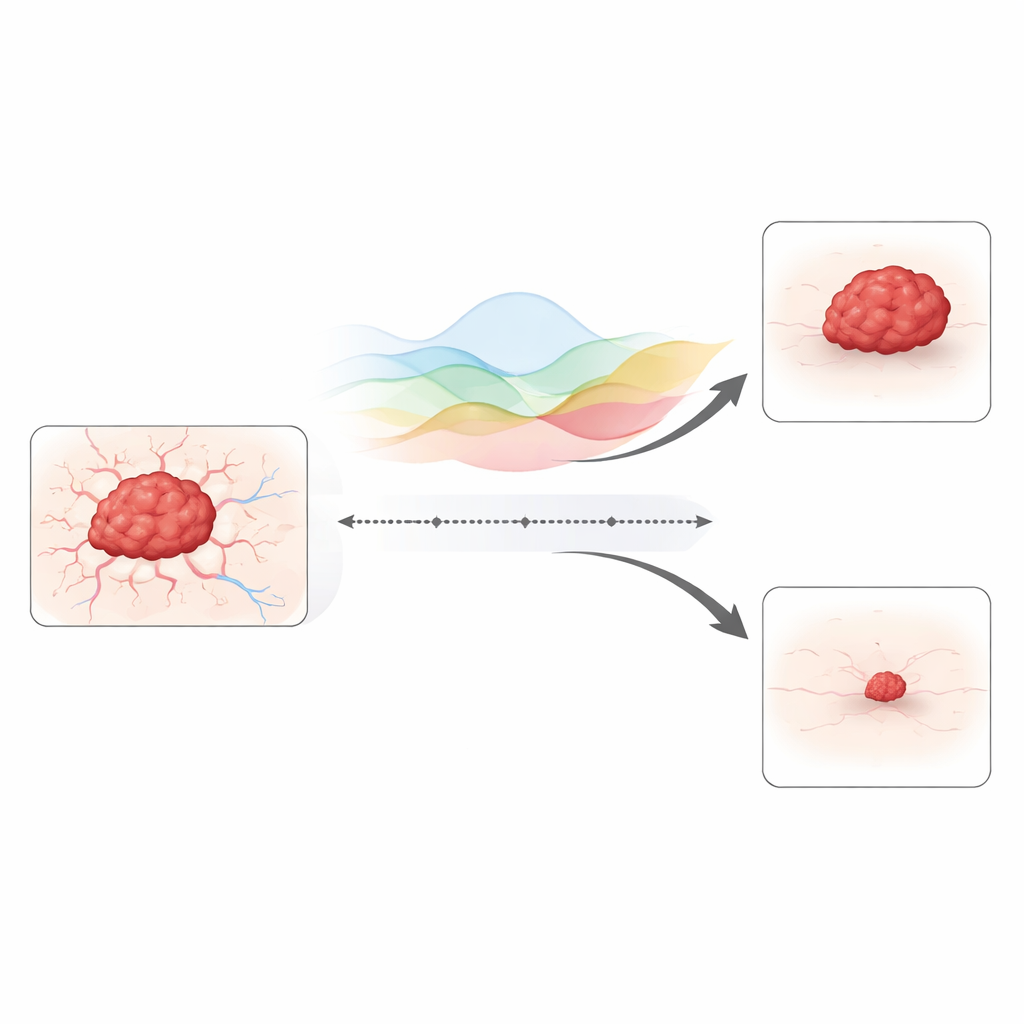
Добавление памяти в модель роста опухоли
Исследование опирается на хорошо известную модель, связывающую размер опухоли с сосудами, её питающими. В классической версии изменения происходят пошагово во времени, без учёта далёкого прошлого. Здесь автор заменяет эти простые временные шаги «дробным» оператором по времени — математическим инструментом, который позволяет поведению сегодняшнего дня зависеть от всего, что было раньше. В биологических терминах это учитывает остатки препаратов, задерживающиеся в ткани, долговременные повреждения сосудов и иммунные клетки, остающиеся активными после лечения. Модель также отслеживает перемещение и распространение клеток опухоли и сосудов в пространстве, что позволяет отображать неравномерное, пальцеобразное вторжение вместо ровного однородного шара клеток.
Сохранение биологической правдоподобности в математике
Любая полезная модель рака должна исключать невозможные результаты, такие как отрицательное число клеток или неограниченный рост. В статье доказывается, что при разумных начальных условиях и опухолевые клетки, и сосуды в этой схеме остаются неотрицательными и находятся в биологически правдоподобных пределах. Затем автор анализирует конкретную численную схему — метод предсказатель‑корректор — для решения исходных уравнений на компьютере. Установив оценки погрешности и условия устойчивости, работа показывает, что моделирование на основе этого метода не только визуально убедительно, но и математически надёжно даже при учёте долговременной памяти и пространственного распространения.
Что показывают симуляции
Воспользовавшись этой формализацией, статья сравнивает традиционную динамику без памяти с её дробными, насыщенными памятью аналогами. Когда «сила памяти» велика (близка к классическому случаю), опухоли быстро растут и затем достигают плато, а после прекращения лечения они, как правило, быстро восстанавливаются. При усилении эффекта памяти (соответствующем меньшему дробному порядку) рост замедляется, реакции на терапию задерживаются, и опухоль может войти в длительные периоды почти полного покоя. Модель также даёт нерегулярные фронты инвазии по мере диффузии раковых клеток и поддерживающих сосудов в ткани — картину, более близкую к тому, что показывают визуализация и патология реальных опухолей.
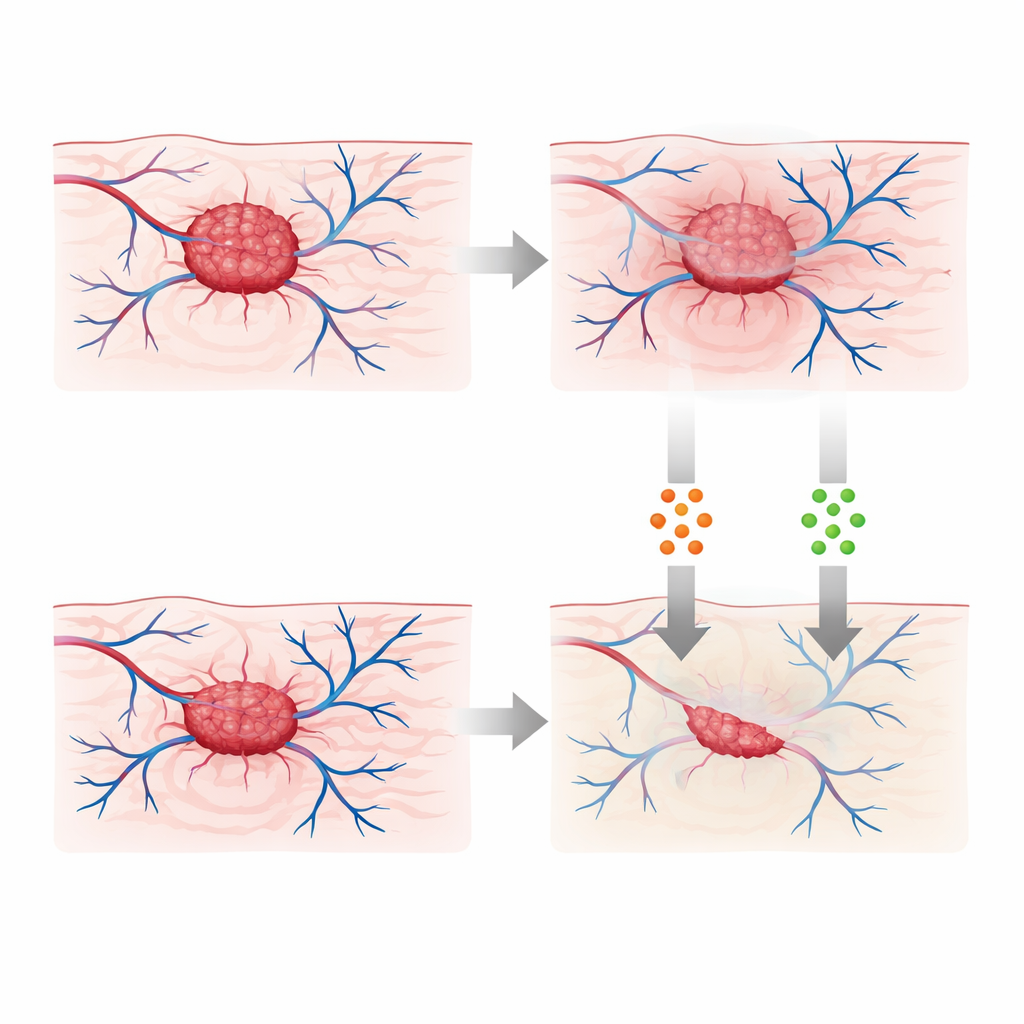
Проектирование более разумных комбинированных терапий
Исследование идёт дальше пассивного предсказания и рассматривает, как можно использовать эту память при планировании лечения. Вводятся два элемента управления, представляющие химиотерапию и иммунотерапию, и формулируется задача оптимизации: минимизировать опухоль при ограничении лекарственной нагрузки. Используя дробную версию стандартной теории управления, автор выводит правила того, как должны меняться эти терапии во времени при наличии у системы памяти. Симуляции трёх сценариев — только химиотерапия, только иммунотерапия и комбинированный режим — показывают, что комбинация обеспечивает наиболее глубокое и стойкое подавление опухоли. В дробной постановке преимущества лечения сохраняются даже после остановки приёма препаратов, что отражает биологическую память в ткани и иммунном ответе.
Что это означает для будущей онкологической помощи
Проще говоря, работа демонстрирует, что серьёзный учёт памяти опухоли и её неравномерного распространения меняет наше представление о её будущем. Модели, учитывающие память, естественно воспроизводят медленные рецидивы, длительные тихие фазы и неравномерную инвазию — особенности, часто наблюдаемые в клинике, но ускользающие от более простых уравнений. Они также предлагают, что тщательно синхронизированные комбинации химио‑ и иммунотерапии могут использовать эти эффекты памяти для более продолжительного подавления опухоли без постоянного применения высоких доз. Хотя эта работа остаётся теоретической, она предлагает более правдоподобную математическую «площадку» для проверки идей лечения и может помочь в разработке по‑настоящему персонализированных схем, учитывающих, как именно у каждого пациента опухоль растёт, распространяется и «помнит».
Цитирование: Can, E. Fractional spatiotemporal Hahnfeldt tumor model with convergence analysis and optimal control. Sci Rep 16, 12549 (2026). https://doi.org/10.1038/s41598-026-41810-x
Ключевые слова: моделирование роста опухоли, дробное исчисление, хемо‑иммунотерапия, пространственно‑временная динамика рака, оптимальное управление лечением