Clear Sky Science · tr
Entegre transkriptomik ve metabolomik analizler, iki kültür koşulu altında RPE hücrelerinin farklı enerji metabolik imzalarını ve işlevsel özelliklerini ortaya koyuyor
Göz destek hücreleri ve laboratuvar tarifleri neden önemli
Gözümüzün ışığı algılayan hücrelerinin arkasında, retinal pigment epitheliumu (RPE) adı verilen ince ama hayati bir tabaka bulunur. Bu destek hücreleri işlevini yitirdiğinde, yaşa bağlı makula dejenerasyonu gibi hastalıklarda görme azalabilir. Bilim insanları artık RPE hücrelerini araştırma ve potansiyel transplantasyon için kök hücrelerden laboratuvarda yetiştirebiliyor, ancak bu hücreleri canlı tutmak için farklı besin “tarifleri” kullanıyorlar. Bu çalışma, önemli sonuçları olan görünüşte basit bir soruyu soruyor: bu tarifler hücrelerin gerçekte ne olduğu ve nasıl davrandığını ne ölçüde değiştiriyor?
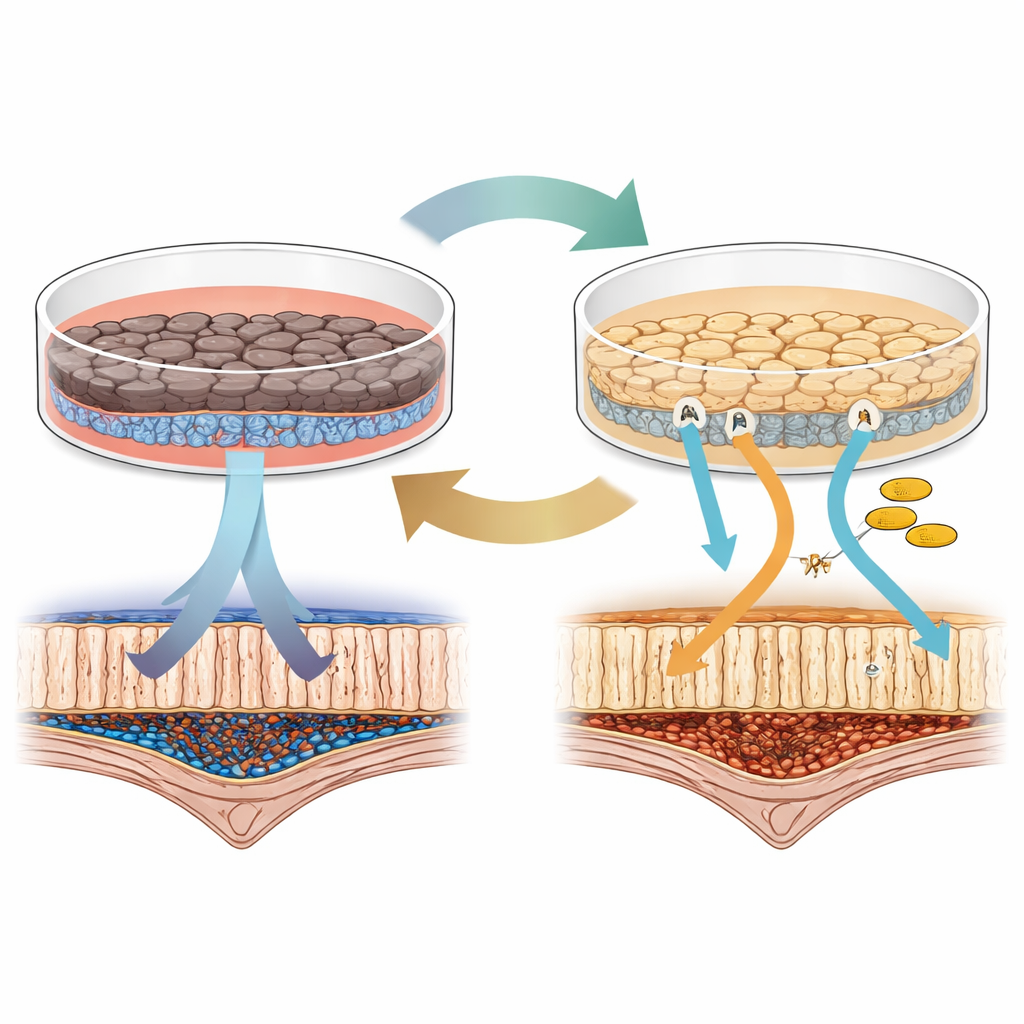
Aynı göz hücrelerini yetiştirmenin iki yolu
Araştırmacılar insan indüklenmiş pluripotent kök hücreleriyle başladılar; bu hücreler neredeyse her hücre tipine yönlendirilebilir ve RPE‑benzeri hücrelere dönüştürüldüler. Ardından bu RPE hücrelerini en yaygın kullanılan iki laboratuvar ortamından birinde tuttular: biri B27 adlı bir katkı maddesine dayalı, diğeri ise KSR adlı bir bileşen kullanan ortam. İlk bakışta her iki hücre grubu da RPE gibi göründü ve davrandı: tek katman oluşturdular, pigment ürettiler ve RPE’nin gözdeki ana görevlerinden biri olan yıpranmış fotoreseptör parçalarını fagosite edebildiler. Ancak daha yakından bakıldığında belirgin farklar ortaya çıktı. B27 ortamındaki hücreler daha koyu pigmentlendi ve daha sıkı bir bariyer oluşturdular; oysa KSR’deki hücreler görsel döngüde rol alan proteinler için daha güçlü sinyaller gösterdi — ışığı görmeye dönüştürmemizi sağlayan kimyasal adımlar.
Benzer hücrelerde farklı yakıt tercihleri
Görüntünün ötesine geçmek için ekip iki güçlü yaklaşımı birleştirdi. Tüm genom genelinde hangi genlerin aktif olduğunu ölçtüler (transkriptomik) ve hücre metabolizmasıyla ilişkili hangi küçük moleküllerin bulunduğunu incelediler (metabolomik). Bu “çok‑omik” katmanlar birlikte hücrelerin enerjiyi nasıl ürettiği ve kullandığına dair bir tablo çizdi. B27 ortamındaki RPE hücreleri, hücre sıvısında glukozun hızlıca parçalanmasına, yani glikolize ve depolama amaçlı yağ sentezine eğilim gösterdi. Buna karşılık KSR ortamındaki RPE hücreleri yağ asitlerini mitokondrilerde daha eksiksiz yakmayı tercih etti ve bunu oksidatif enerji üretimine yönlendirdi. Başka bir deyişle, aynı başlangıç hücreleri iki farklı kültür koşulunda farklı enerji kullanma eğilimlerine doğru itildi.
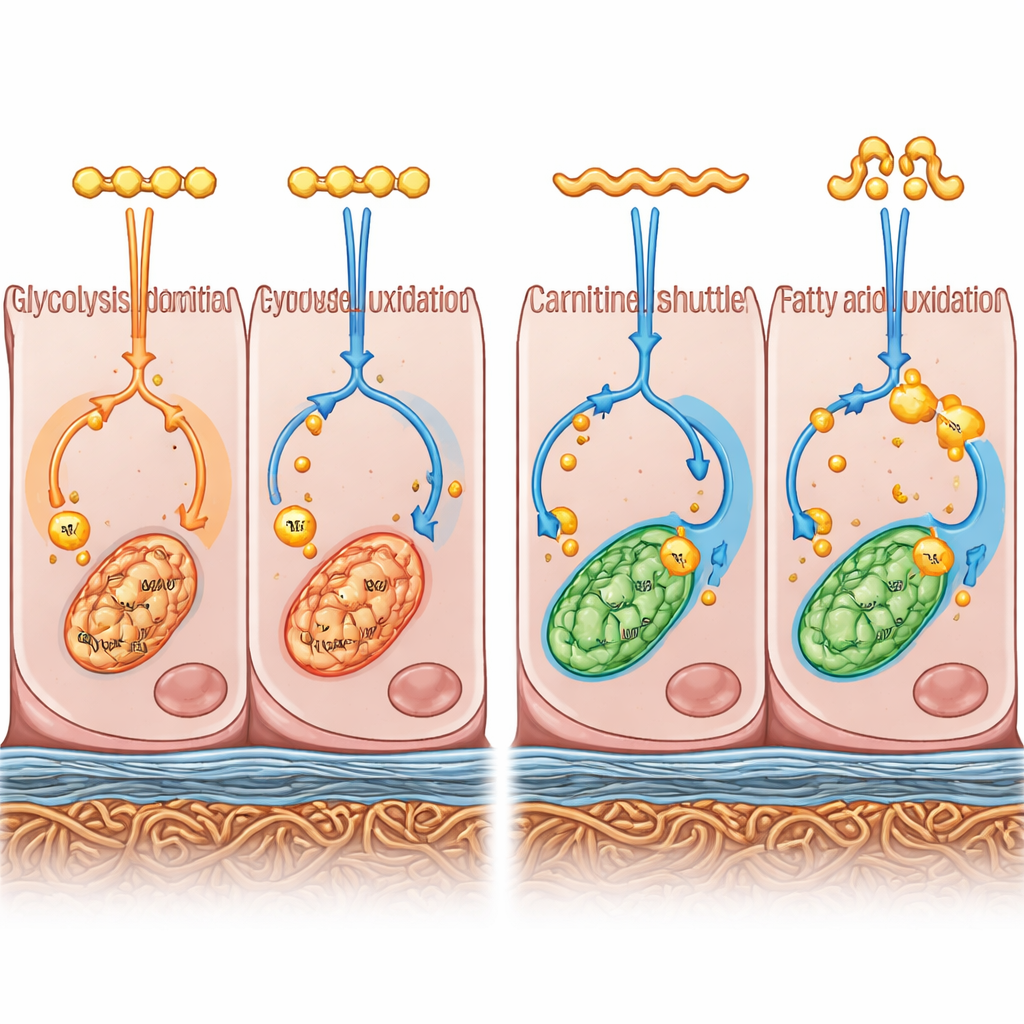
Enerji kullanımı yapıyı ve bariyerleri nasıl şekillendiriyor
Hücrelerin yakıt seçimi, dokusal olarak nasıl organize olduklarıyla sıkı bir şekilde bağlantılıydı. Glikoliz ağırlıklı metabolizmaya sahip B27’de yetişen hücreler, hücreleri destekleyen ve birbirine yapıştıran protein ve lif ağını oluşturan ekstraselüler matriksi kontrol eden daha fazla gen açtılar. Bu hücreler ayrıca katman boyunca daha yüksek elektriksel direnç gösterdiler; bu da gözdekiyle benzer bir bariyer oluşturma yeterliliklerinin bir göstergesi. Bilim insanları B27 hücrelerinde kimyasal olarak glikolizi yavaşlattıklarında, bu matriks genlerinin ifadesi düştü ve bariyer zayıfladı; bu da daha hızlı glukoz‑yönelimli durumun hücreler arasındaki sağlam sızdırmazlığı inşa etmeye ve sürdürmeye yardımcı olduğunu düşündürüyor.
Diğer ortamda daha fazla oksijene bağımlı bir mod
KSR’de yetişen hücrelerde hikâye farklıydı. İç kimyaları serbest yağ asitleri ve bu yağları mitokondriye taşıyacak bileşenlerin daha yüksek düzeylerini gösterdi. Yağın yakılması aksadığında birikebilen yağ asidi bağlantılı ara ürünleri daha az biriktirdiler; bu, daha verimli yağ yakımına işaret ediyor. Hücrelerde ayrıca son enerji üretim makinesine girdi sağlayan moleküller daha yüksek seviyelerdeydi ve oksijen kullanarak hücrenin ana enerji para birimi ATP’yi üreten oksidatif fosforilasyonla ilgili daha fazla gen aktive oldu. İlginç bir şekilde, her iki hücre grubunda da metabolizmanın merkezi düğümü olan TCA döngüsünde genel olarak benzer bir etkinlik vardı; bu da en çok farklı olanın girişteki yakıt dengesi ile aşağı yönlü enerji dönüşümü olduğunu öne sürüyor.
Bu bulguların hastalık modelleri ve gelecekteki tedaviler için anlamı
Uzman olmayanlar için ana mesaj şudur: Laboratuvar koşulları sadece RPE hücrelerini hayatta tutmakla kalmaz — hangi tür RPE hücrelerine dönüştüklerini de belirlemeye yardımcı olur. Bir ortam hücreleri glukoz‑odaklı, bariyer‑odaklı bir duruma ve daha güçlü yapısal özelliklere itiyor; diğer ortam ise yağ yakımını ve mitokondri odaklı bir durumu teşvik ediyor; bu durum fotoreseptörlerle enerji ortaklığı rolünü daha iyi yansıtabilir. Hiçbir kültür, insan gözünün içindeki ortamı tamamen yeniden oluşturmaz, ancak her biri normal RPE davranışının farklı bir dilimini yakalıyor. Yazarlar, kök hücre kaynaklı RPE’yi kör edici hastalıkları incelemek veya transplantasyon için hazırlamak amacıyla kullanırken bu metabolik “kişiliklerin” tanınmasının ve kasıtlı olarak seçilmesinin hayati olacağını; doğru bariyer gücü ve enerji desteği dengesinin görmeyi korumaya yardımcı olabileceğini savunuyorlar.
Atıf: Zhang, F., Wang, C., Tang, Q. et al. Integrated transcriptomic and metabolomic analyses reveal distinct energy metabolic signatures and functional properties of RPE cells under two culture conditions. Sci Rep 16, 11992 (2026). https://doi.org/10.1038/s41598-026-39689-9
Anahtar kelimeler: retinal pigment epitelyumu, kök hücre kaynaklı RPE, hücre metabolizması, yaşa bağlı makula dejenerasyonu, hücre kültürü koşulları