Clear Sky Science · de
Integrierte transkriptomische und metabolomische Analysen zeigen unterschiedliche energetische Stoffwechselprofile und funktionelle Eigenschaften von RPE-Zellen unter zwei Kulturbedingungen
Warum Unterstützerzellen des Auges und Laborrezepte wichtig sind
Hinter den lichtempfindlichen Zellen unseres Auges liegt eine dünne, aber entscheidende Schicht, das retinale Pigmentepithel (RPE). Wenn diese Stützzellen versagen, kann das Sehvermögen bei Erkrankungen wie der altersbedingten Makuladegeneration nachlassen. Forschende können RPE-Zellen inzwischen aus Stammzellen im Labor heranzüchten – für Forschung und mögliche Transplantationen – verwenden dafür aber verschiedene „Rezepte“ an Nährstoffen. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenschwere Frage: Wie stark verändern diese Rezepte tatsächlich, was die Zellen sind und wie sie sich verhalten?
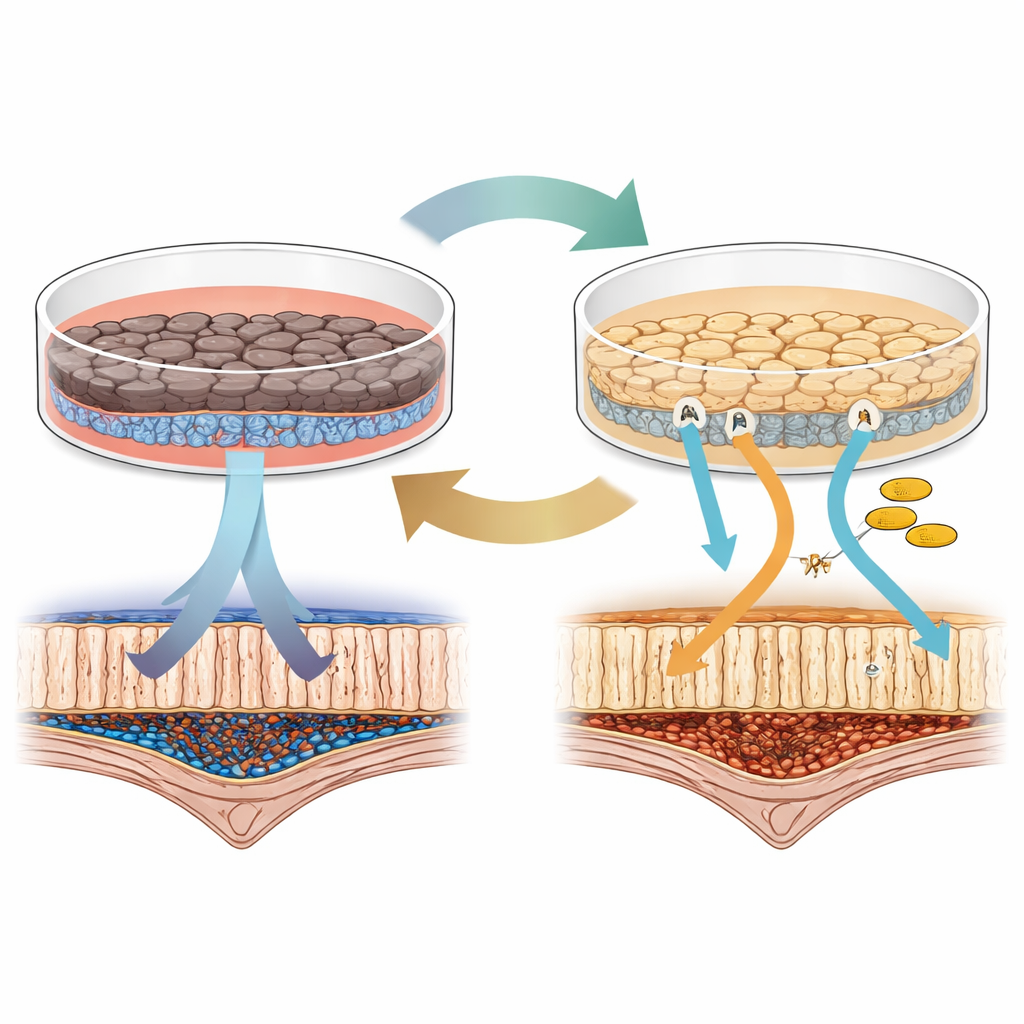
Zwei Wege, dieselben Augen-Zellen zu züchten
Die Forschenden begannen mit humanen induzierten pluripotenten Stammzellen, die sich in fast jeden Zelltyp leiten lassen, und führten sie zu RPE-ähnlichen Zellen. Diese RPE-Zellen wurden anschließend in zwei der am häufigsten verwendeten Kulturmedien gehalten: eines auf Basis eines Zusatzes namens B27 und ein anderes mit einem Bestandteil namens KSR. Auf den ersten Blick sahen und verhielten sich beide Zellgruppen wie RPE: Sie bildeten eine einschichtige Schicht, entwickelten Pigment und konnten abgenutzte Teile von Photorezeptorzellen aufnehmen – eine zentrale Aufgabe des RPE im Auge. Bei genauerer Betrachtung zeigten sich jedoch deutliche Unterschiede. Zellen in B27 wurden stärker pigmentiert und bildeten eine dichtere Barriere, während Zellen in KSR stärkere Signale für Proteine des visuellen Kreislaufs zeigten, der die chemischen Schritte ermöglicht, mit denen Licht in Sehimpulse umgewandelt wird.
Unterschiedliche Brennstoffwahl in ähnlichen Zellen
Um über das Erscheinungsbild hinauszugehen, kombinierten die Forschenden zwei leistungsfähige Methoden. Sie maßen, welche Gene im gesamten Genom aktiv waren (Transkriptomik) und welche kleinen Moleküle des Zellstoffwechsels vorhanden waren (Metabolomik). Zusammen malten diese „Multi-Omics“-Ebenen ein Bild davon, wie die Zellen Energie erzeugten und nutzten. RPE-Zellen im B27-Medium tendierten dazu, Glukose rasch im Zellplasma abzubauen – ein Weg, der als Glykolyse bekannt ist – und vermehrt Fette zum Speichern zu synthetisieren. Im Gegensatz dazu bevorzugten RPE-Zellen im KSR-Medium eine vollständigere Verbrennung von Fettsäuren in ihren Mitochondrien, den Energiemanufakturen der Zelle, und leiteten dies in oxidative Energiegewinnung. Anders gesagt: Die beiden Kulturbedingungen schubsten dieselben Ausgangszellen in unterschiedliche Präferenzen der Energieverwendung.
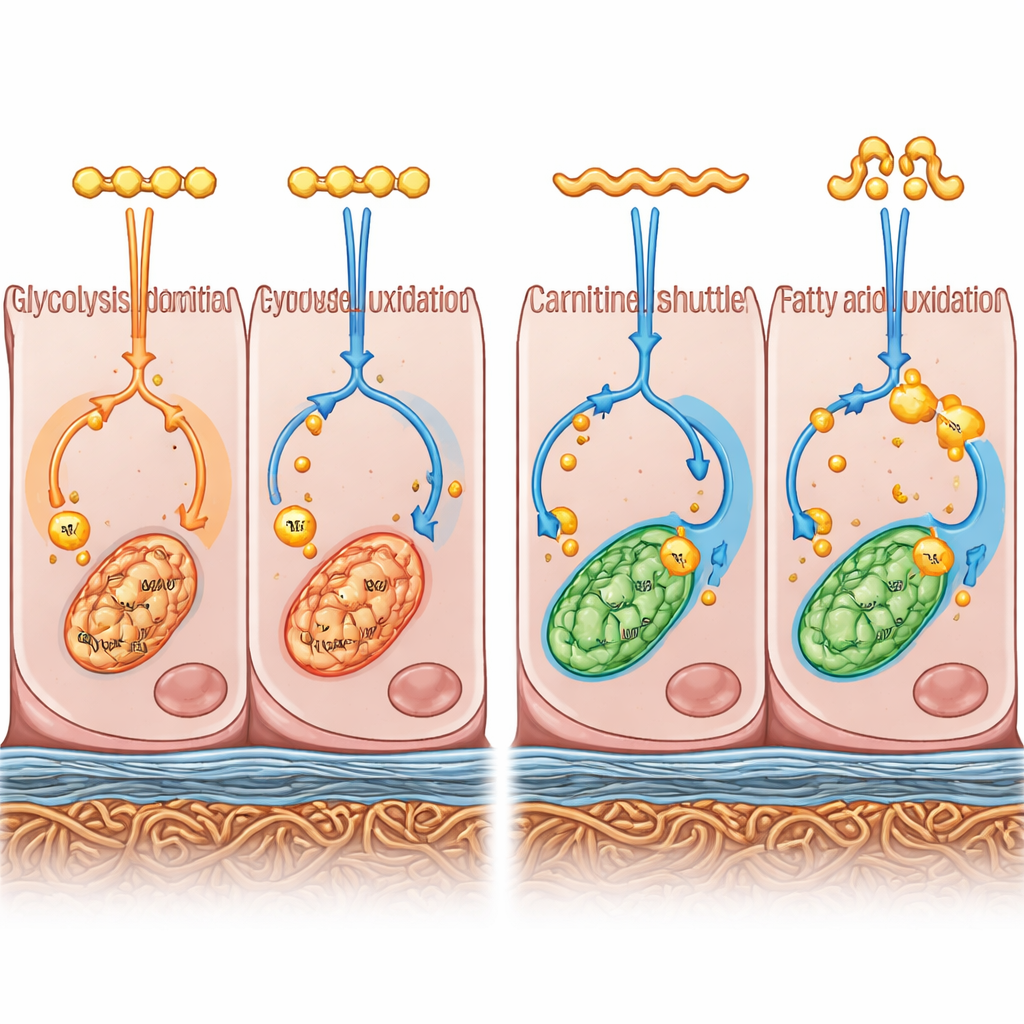
Wie Energieverwendung Struktur und Barrieren formt
Die Wahl des Brennstoffs war eng mit der Art verknüpft, wie sich die Zellen als Gewebe organisierten. B27-gezüchtete Zellen mit ihrem glykolyselastigen Stoffwechsel schalteten mehr Gene an, die die extrazelluläre Matrix steuern – das Netzwerk aus Proteinen und Fasern, das Zellen stützt und zusammenhält. Diese Zellen zeigten außerdem einen höheren elektrischen Widerstand über die Zellschicht, ein Maß dafür, wie gut sie eine Barriere bilden, die der im Auge ähnelt. Wenn die Wissenschaftler die Glykolyse in B27-Zellen chemisch verlangsamten, sank die Expression dieser Matrixgene und die Barriere wurde schwächer; dies deutet darauf hin, dass der schnellere, glukosegetriebene Zustand hilft, eine robuste Abdichtung zwischen den Zellen aufzubauen und zu erhalten.
Ein stärker sauerstoffabhängiger Modus im anderen Medium
Bei KSR-gezüchteten Zellen sah die Lage anders aus. Ihre interne Chemie wies höhere Konzentrationen freier Fettsäuren und wichtiger Komponenten auf, die nötig sind, um diese Fette in die Mitochondrien zu schleusen. Es häuften sich weniger Fettsäure-gebundene Zwischenprodukte an, die sich bilden können, wenn dieser Prozess ins Stocken gerät, was auf eine effizientere Fettverbrennung hindeutet. Die Zellen enthielten außerdem größere Mengen von Molekülen, die in die finale energieerzeugende Maschinerie einspeisen, und schalteten mehr Gene für die oxidative Phosphorylierung ein, den sauerstoffverwendenden Prozess, der den größten Teil des zellulären ATPs produziert, der universellen Energiewährung der Zelle. Interessanterweise zeigten beide Zellgruppen eine insgesamt ähnliche Aktivität im zentralen Stoffwechselknotenpunkt, dem Zitronensäurezyklus (TCA), was darauf hindeutet, dass vor allem das Verhältnis der eingespeisten Brennstoffe und die nachgeschaltete Energieumwandlung am stärksten differiert.
Was das für Krankheitsmodelle und künftige Therapien bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Laborbedingungen halten RPE-Zellen nicht nur am Leben – sie beeinflussen, welche Art von RPE-Zellen daraus wird. Ein Medium drängt die Zellen in einen glukosegetriebenen, barrierefokussierten Zustand mit stärkeren strukturellen Merkmalen, während das andere einen fettverbrennenden, mitochondriengetriebenen Modus fördert, der die Rolle des RPE als Energiepartner für Photorezeptoren besser abbilden könnte. Keine der beiden Kulturen reproduziert vollständig die Umgebung im menschlichen Auge, aber jede fängt einen anderen Ausschnitt normalen RPE-Verhaltens ein. Die Autoren argumentieren, dass das Erkennen und die gezielte Wahl zwischen diesen metabolischen „Persönlichkeiten“ entscheidend sein wird, wenn aus Stammzellen abgeleitetes RPE zur Untersuchung erblindender Erkrankungen oder zur Vorbereitung von Zellen für die Transplantation verwendet wird, wo das richtige Gleichgewicht aus Barrierestärke und Energieunterstützung dazu beitragen könnte, das Sehvermögen zu schützen.
Zitation: Zhang, F., Wang, C., Tang, Q. et al. Integrated transcriptomic and metabolomic analyses reveal distinct energy metabolic signatures and functional properties of RPE cells under two culture conditions. Sci Rep 16, 11992 (2026). https://doi.org/10.1038/s41598-026-39689-9
Schlüsselwörter: retinale Pigmentepithel, aus Stammzellen abgeleitetes RPE, Zellstoffwechsel, altersbedingte Makuladegeneration, Zellkulturbedingungen