Clear Sky Science · fr
Analyses intégrées transcriptomiques et métabolomiques révèlent des signatures métaboliques énergétiques distinctes et des propriétés fonctionnelles des cellules de l’EPR selon deux conditions de culture
Pourquoi les cellules de soutien de l’œil et les recettes de laboratoire comptent
Derrière les cellules photoréceptrices de nos yeux se trouve une couche mince et cruciale appelée épithélium pigmentaire rétinien (EPR). Lorsque ces cellules de soutien défaillent, la vision peut décliner dans des maladies comme la dégénérescence maculaire liée à l’âge. Les scientifiques savent maintenant faire croître des cellules de l’EPR à partir de cellules souches au laboratoire pour la recherche et d’éventuelles greffes, mais ils utilisent différentes « recettes » de nutriments pour les maintenir en vie. Cette étude pose une question apparemment simple mais aux grandes conséquences : dans quelle mesure ces recettes modifient-elles ce que les cellules sont réellement et comment elles se comportent ?
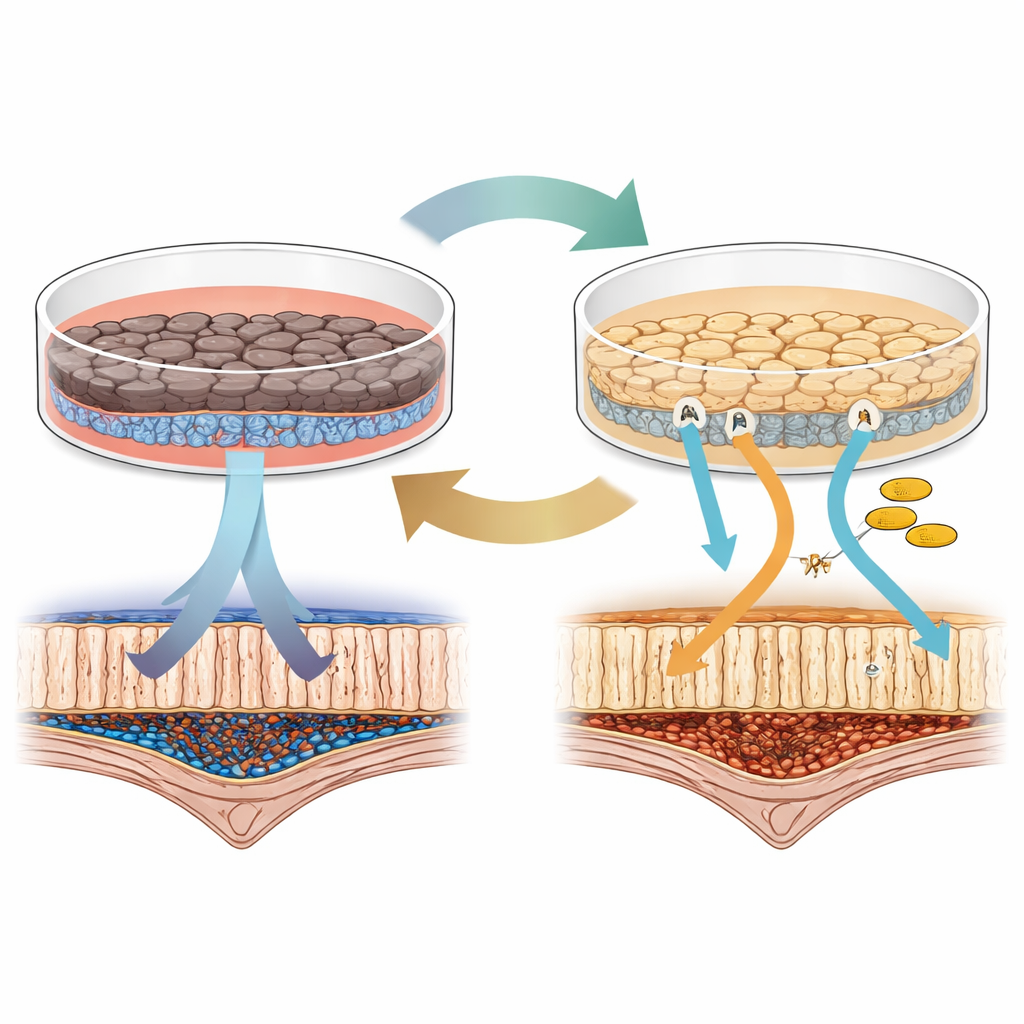
Deux façons de cultiver les mêmes cellules oculaires
Les chercheurs ont commencé avec des cellules souches pluripotentes induites humaines, capables d’être dirigées vers presque n’importe quel type cellulaire, et les ont guidées pour donner des cellules de type EPR. Ils ont ensuite maintenu ces cellules EPR dans deux milieux de culture parmi les plus utilisés en laboratoire : l’un basé sur un additif appelé B27, et l’autre utilisant un composant appelé KSR. À première vue, les deux populations de cellules ressemblaient et se comportaient comme des EPR : elles formaient une couche monostratifiée, produisaient du pigment et pouvaient phagocyter des fragments âgés de photorécepteurs, l’une des fonctions clés de l’EPR dans l’œil. Mais une inspection plus fine a révélé des différences nettes. Les cellules en B27 devenaient plus pigmentées et formaient une barrière plus étanche, tandis que les cellules en KSR présentaient des signaux plus forts pour des protéines impliquées dans le cycle visuel, les étapes chimiques qui nous permettent de convertir la lumière en vision.
Différents choix de carburant au sein de cellules similaires
Pour aller au‑delà de l’apparence, l’équipe a combiné deux approches puissantes. Ils ont mesuré les gènes actifs à l’échelle du génome (transcriptomique) et les petites molécules liées au métabolisme présentes (métabolomique). Ensemble, ces couches « multi‑omiques » ont dessiné un portrait de la manière dont les cellules fabriquaient et utilisaient l’énergie. Les cellules EPR en milieu B27 penchaient vers une dégradation rapide du glucose dans le cytosol, une voie connue sous le nom de glycolyse, et vers la synthèse de lipides pour stockage. En revanche, les cellules en KSR favorisaient l’oxydation plus complète des acides gras dans leurs mitochondries, les centrales énergétiques de la cellule, et canalisaient cela vers une production d’énergie oxydative. Autrement dit, les deux conditions de culture ont poussé des cellules de même origine vers des préférences distinctes d’utilisation de l’énergie.
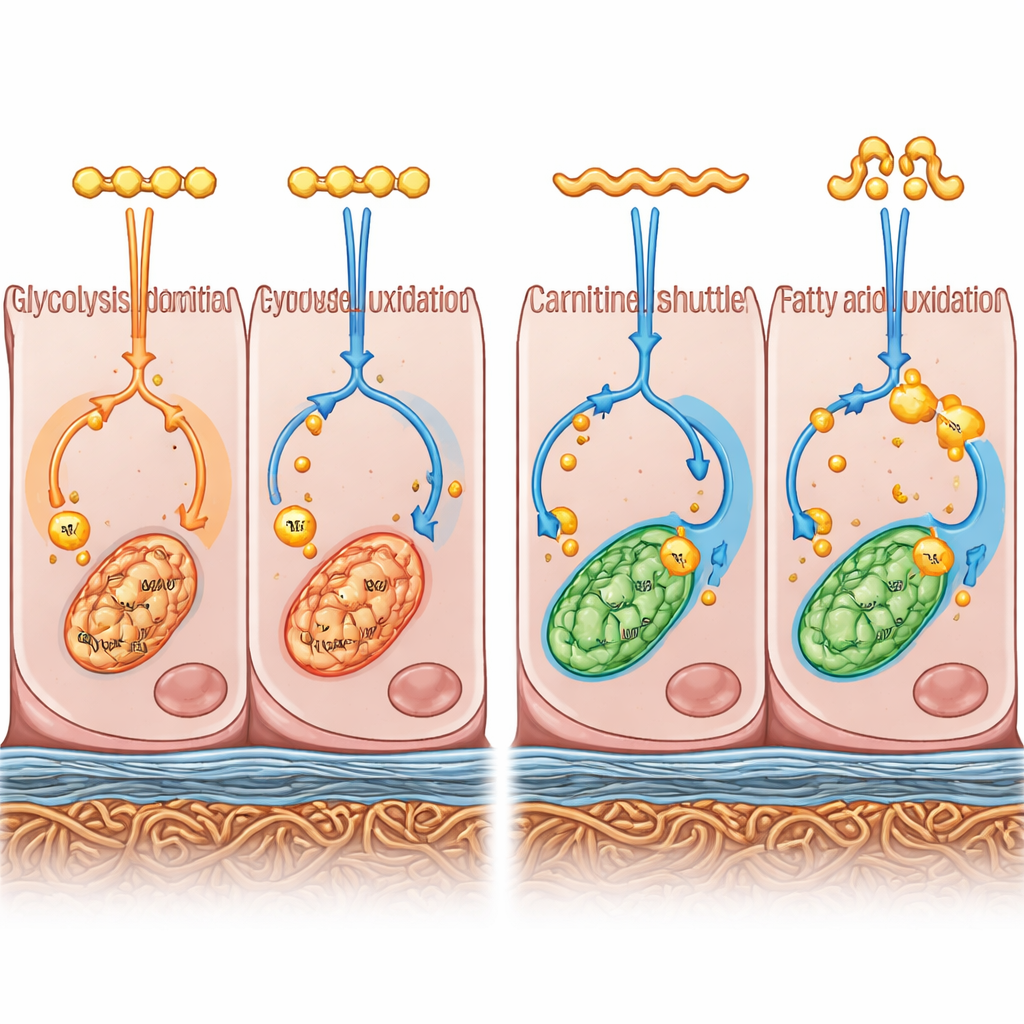
Comment l’usage de l’énergie façonne la structure et les barrières
Le choix de carburant des cellules était étroitement lié à leur organisation tissulaire. Les cellules cultivées en B27, avec leur métabolisme axé sur la glycolyse, activaient davantage de gènes contrôlant la matrice extracellulaire — le réseau de protéines et de fibres qui soutient et colle les cellules entre elles. Ces cellules présentaient également une résistance électrique plus élevée à travers la couche, un indicateur de la qualité de la barrière similaire à celle de l’œil. Lorsque les chercheurs ont ralenti chimiquement la glycolyse dans les cellules B27, l’expression de ces gènes de la matrice a diminué et la barrière est devenue plus faible, ce qui suggère que l’état favorisé par un métabolisme rapide du glucose aide à construire et maintenir un joint robuste entre les cellules.
Un mode plus demandeur en oxygène dans l’autre milieu
Dans les cellules cultivées en KSR, le tableau était différent. Leur chimie interne montrait des niveaux plus élevés d’acides gras libres et des composants clés nécessaires pour acheminer ces lipides vers les mitochondries. Elles accumulaient moins d’intermédiaires liés aux acides gras qui peuvent s’accumuler lorsque ce processus est bloqué, ce qui suggère une oxydation des lipides plus efficace. Les cellules présentaient aussi des quantités plus élevées des molécules alimentant la machinerie finale de production d’énergie et activaient davantage de gènes de la phosphorylation oxydative, le processus utilisant l’oxygène qui produit la majorité de l’ATP cellulaire, la monnaie énergétique universelle. Fait intéressant, les deux groupes de cellules avaient une activité globalement similaire dans le carrefour central du métabolisme, le cycle TCA, ce qui indique que ce sont surtout l’équilibre des carburants entrants et la conversion énergétique en aval qui diffèrent.
Ce que cela signifie pour les modèles de maladie et les thérapies futures
Pour les non‑spécialistes, le message clé est que les conditions de laboratoire ne se contentent pas de maintenir les cellules EPR en vie — elles contribuent à déterminer quel type de cellules EPR elles deviennent. Un milieu oriente les cellules vers un état axé sur le glucose et les fonctions de barrière avec des caractéristiques structurelles renforcées, tandis que l’autre favorise un état axé sur la combustion des graisses et la fonction mitochondriale qui peut mieux refléter le rôle de l’EPR en tant que partenaire énergétique des photorécepteurs. Aucun des milieux ne reproduit complètement l’environnement à l’intérieur de l’œil humain, mais chacun capture une facette différente du comportement normal de l’EPR. Les auteurs soutiennent que reconnaître et choisir délibérément entre ces « personnalités » métaboliques sera essentiel lors de l’utilisation d’EPRE dérivés de cellules souches pour étudier les maladies responsables de cécité ou pour préparer des cellules en vue de transplantations, où le bon équilibre entre solidité de la barrière et soutien énergétique pourrait aider à protéger la vision.
Citation: Zhang, F., Wang, C., Tang, Q. et al. Integrated transcriptomic and metabolomic analyses reveal distinct energy metabolic signatures and functional properties of RPE cells under two culture conditions. Sci Rep 16, 11992 (2026). https://doi.org/10.1038/s41598-026-39689-9
Mots-clés: épithélium pigmentaire rétinien, EPRE dérivé de cellules souches, métabolisme cellulaire, dégénérescence maculaire liée à l’âge, conditions de culture cellulaire