Clear Sky Science · sv
Integrerade transkriptomiska och metabolomiska analyser avslöjar distinkta energimetaboliska signaturer och funktionella egenskaper hos RPE‑celler under två odlingsförhållanden
Varför stödjeceller i ögat och laboratorierecept spelar roll
Bakom ögats ljuskänsliga celler ligger ett tunt, avgörande skikt som kallas retinalt pigmentepitel (RPE). När dessa stödjeceller sviktar kan synen försämras i sjukdomar som åldersrelaterad makuladegeneration. Forskare kan nu odla RPE‑celler från stamceller i laboratoriet för forskning och potentiella transplantationer, men de använder olika ”recept” av näringslösningar för att hålla cellerna vid liv. Denna studie ställer en förenklat formulerad men viktig fråga: hur mycket ändrar dessa recept vad cellerna faktiskt är och hur de beter sig?
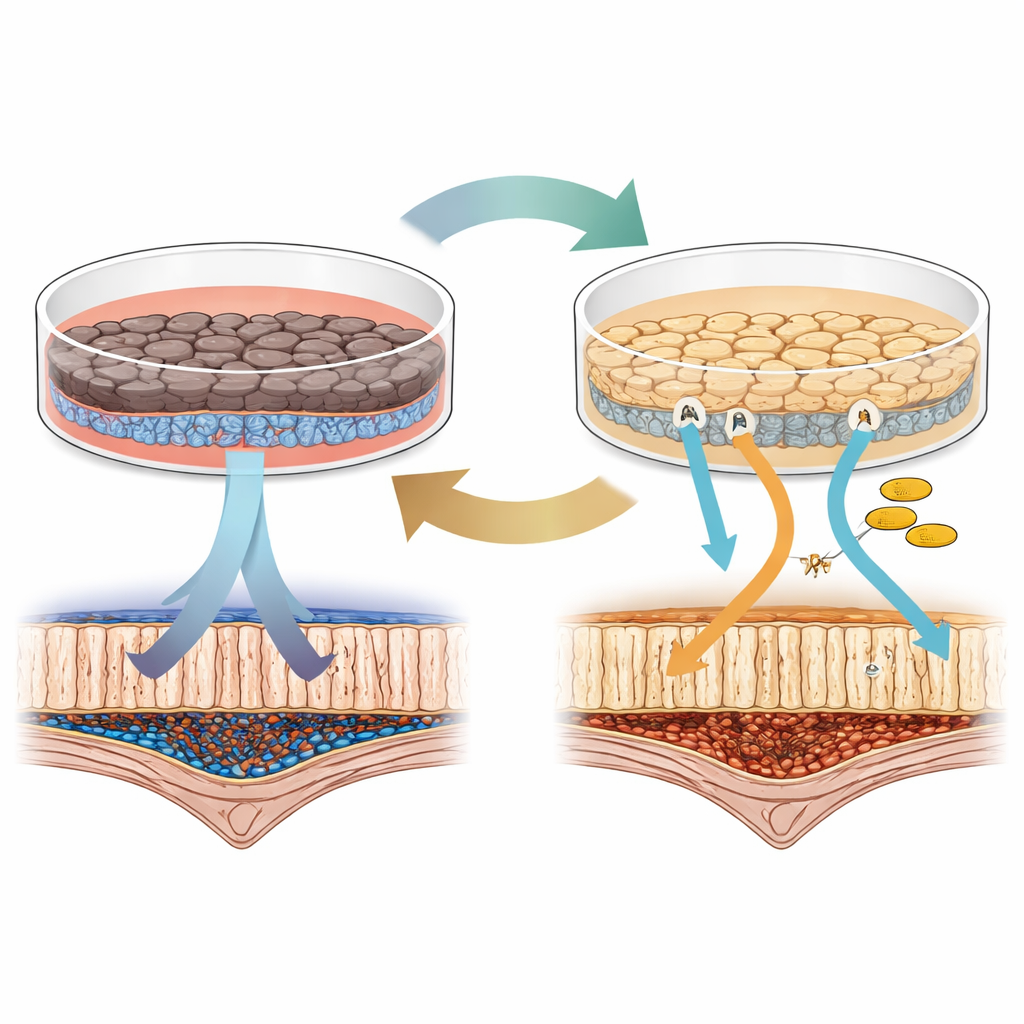
Två sätt att odla samma ögonceller
Forskarna började med mänskliga inducerade pluripotenta stamceller, som kan styras att bli nästan vilken celltyp som helst, och vägledde dem till RPE‑lika celler. De höll sedan dessa RPE‑celler i två av de mest använda odlingsmedierna: ett baserat på ett tillskott kallat B27 och ett annat som använde en komponent kallad KSR. Vid första anblick såg båda cellgrupperna ut och uppträdde som RPE: de bildade ett enda skikt, producerade pigment och kunde fagocytera utslitna delar av fotoreceptorceller, en av RPE:s nyckeluppgifter i ögat. Men vid närmare undersökning framträdde tydliga skillnader. Celler i B27 blev mer djupt pigmenterade och bildade en tätare barriär, medan celler i KSR visade starkare signaler för proteiner som är involverade i det visuella kretsloppet, de kemiska stegen som gör att vi kan omvandla ljus till syn.
Olika bränsleval i liknande celler
För att gå bortom utseendet kombinerade teamet två kraftfulla metoder. De mätte vilka gener som var aktiva över hela genomet (transkriptomik) och vilka små molekyler relaterade till cellmetabolism som fanns närvarande (metabolomik). Tillsammans målade dessa ”multi‑omics” upp en bild av hur cellerna tillverkade och använde energi. RPE‑celler i B27‑medium lutade mot att bryta ner glukos snabbt i cellvätskan, en väg känd som glykolys, och mot att bygga upp fetter för lagring. Däremot föredrog RPE‑celler i KSR‑medium att förbränna fettsyror mer fullständigt i sina mitokondrier, cellens energifabriker, och kanaliserade detta till oxidativ energiproduktion. Med andra ord puttade de två odlingsförhållandena samma ursprungsceller mot distinkta preferenser för energianvändning.
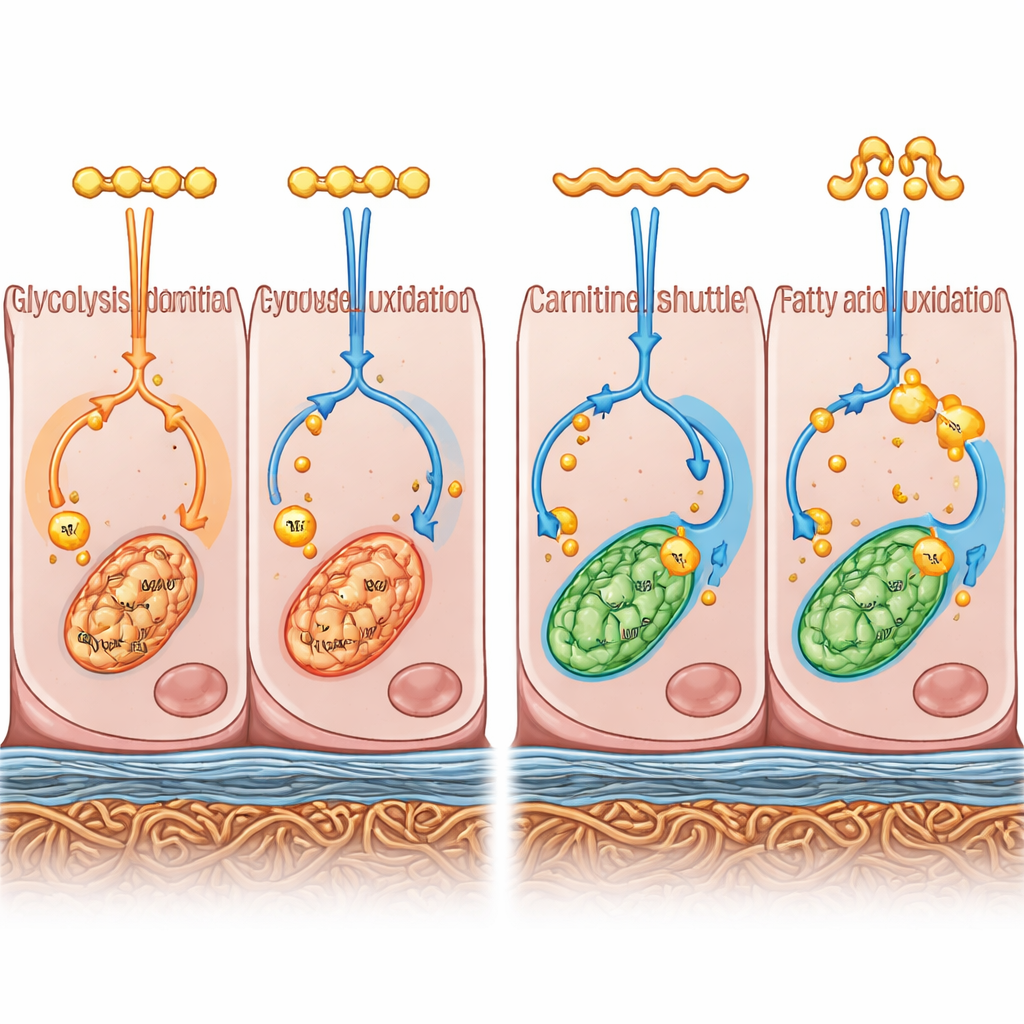
Hur energianvändning formar struktur och barriärer
Hur cellerna valde sitt bränsle var starkt kopplat till hur de organiserade sig som en vävnad. B27‑odlade celler, med sin glykolysdominerade metabolism, slog på fler gener som styr den extracellulära matrisen — nätverket av proteiner och fibrer som stödjer och binder samman celler. Dessa celler visade också högre elektriskt motstånd över skiktet, ett mått på hur väl de bildar en barriär liknande den i ögat. När forskarna kemiskt bromsade glykolysen i B27‑celler sjönk uttrycket av dessa matrixgener och barriären försvagades, vilket tyder på att det snabbare glukosdrivna tillståndet hjälper till att bygga och upprätthålla en robust tätning mellan cellerna.
Ett mer syrekrävande läge i det andra mediet
I KSR‑odlade celler såg bilden annorlunda ut. Deras interna kemi visade högre nivåer av fria fettsyror och nyckelkomponenter som behövs för att föra in dessa fetter i mitokondrierna. De ackumulerade färre fettsyra‑kopplade intermediärer som kan byggas upp när denna process stannar av, vilket antyder effektivare fettförbränning. Cellerna hade också högre mängder av molekyler som matar in i den slutliga energi‑genererande maskineriet och slog på fler gener för oxidativ fosforylering, den syrekrävande process som producerar det mesta av cellens ATP, dess universella energivaluta. Intressant nog hade båda cellgrupperna i stort sett liknande aktivitet i metabolismens centrala nav, TCA‑cykeln, vilket tyder på att det är balansen mellan ingående bränslen och den efterföljande energiomvandlingen som skiljer sig mest.
Vad detta betyder för sjukdomsmodeller och framtida terapier
För icke‑specialister är huvudbudskapet att laboratorieomständigheter inte bara håller RPE‑celler vid liv — de hjälper avgöra vilken typ av RPE‑celler de blir. Ett medium driver cellerna mot ett glukosdrivet, barriärfokuserat tillstånd med starkare strukturella egenskaper, medan det andra uppmuntrar ett fettförbrännande, mitokondrie‑drivet läge som kan bättre spegla RPE:s roll som energipartner åt fotoreceptorer. Inget odlingsmedium reproducerar fullständigt miljön inne i det mänskliga ögat, men vardera fångar en annan aspekt av normal RPE‑funktion. Författarna argumenterar för att igenkänna och medvetet välja mellan dessa metaboliska ”personligheter” blir avgörande när man använder stamcells‑härlett RPE för att studera blindinge sjukdomar eller förbereda celler för transplantation, där rätt balans mellan barriärstyrka och energistöd kan hjälpa till att skydda synen.
Citering: Zhang, F., Wang, C., Tang, Q. et al. Integrated transcriptomic and metabolomic analyses reveal distinct energy metabolic signatures and functional properties of RPE cells under two culture conditions. Sci Rep 16, 11992 (2026). https://doi.org/10.1038/s41598-026-39689-9
Nyckelord: retinal pigmentepitel, stamcells‑härlett RPE, cellmetabolism, åldersrelaterad makuladegeneration, cellodlingsförhållanden