Clear Sky Science · ru
Интегрированные транскриптомные и метаболомные анализы выявляют различные энергетические метаболические подписи и функциональные свойства клеток RPE при двух условиях культивирования
Почему поддерживающие клетки глаза и лабораторные «рецепты» важны
За светочувствительными клетками нашего глаза располагается тонкий, но жизненно важный слой — пигментный эпителий сетчатки (RPE). Когда эти поддерживающие клетки дают сбой, зрение может ухудшаться при таких заболеваниях, как возрастная макулярная дегенерация. Ученые теперь могут выращивать клетки RPE из стволовых клеток в лаборатории для исследований и потенциальных трансплантаций, но для их поддержания используют разные «рецепты» питательных сред. В этом исследовании поставлен на первый взгляд простой, но важный вопрос: насколько сильно эти рецепты меняют то, какими фактически становятся клетки и как они функционируют?
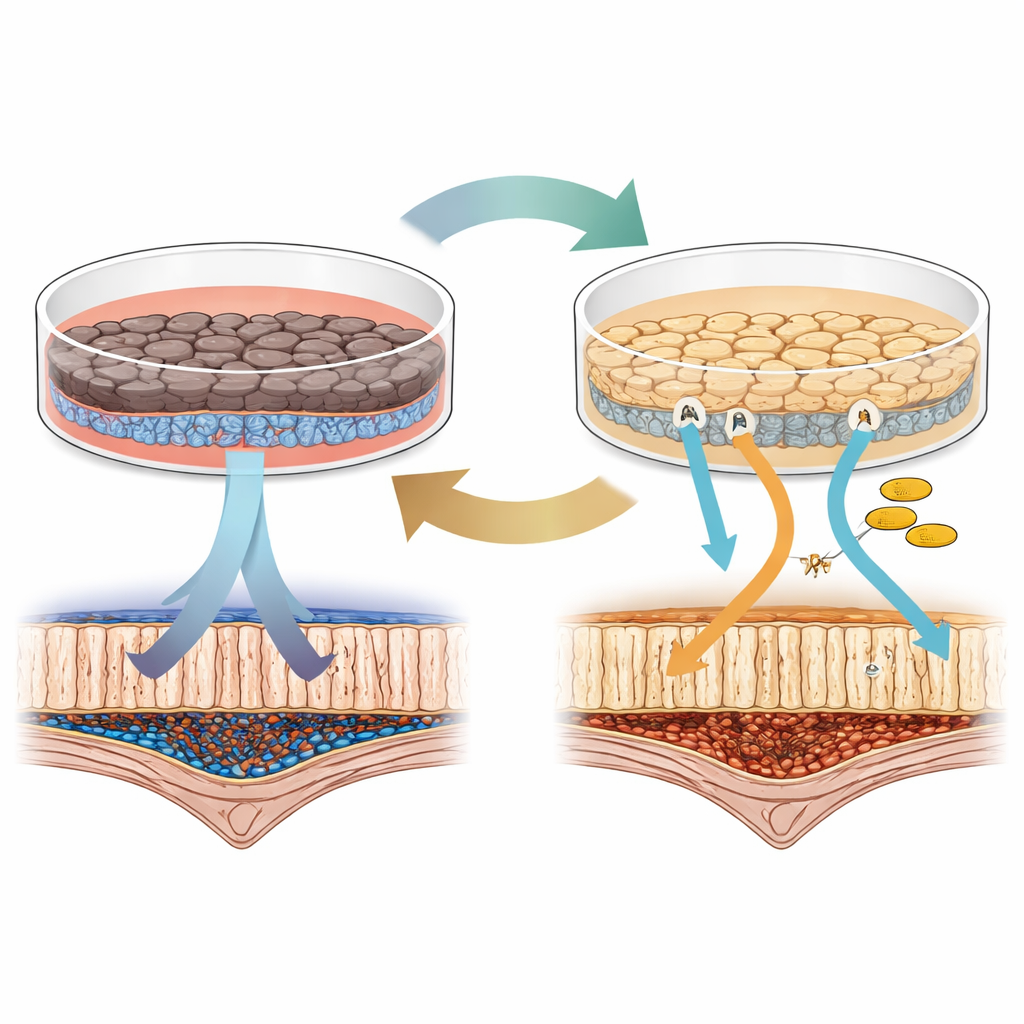
Два способа вырастить одни и те же клетки глаза
Исследователи начали с индуцированных плюрипотентных стволовых клеток человека, которые можно направить в почти любой тип клеток, и получили из них клетки, похожие на RPE. Затем эти RPE содержали в двух широко используемых лабораторных средах: одна основана на добавке под названием B27, другая — с компонентом KSR. На первый взгляд обе группы клеток выглядели и вели себя как RPE: они образовывали однослойный эпителий, продуцировали пигмент и могли фагоцитировать омертвевшие фрагменты фоторецепторов — одну из ключевых функций RPE в глазу. Однако при более тщательном рассмотрении обнаружились явные различия. Клетки в среде B27 стали глубже пигментированными и сформировали более плотный барьер, тогда как клетки в KSR проявляли более сильные сигналы белков, вовлеченных в визуальный цикл — химические реакции, превращающие свет в зрительное восприятие.
Разные выборы топлива внутри похожих клеток
Чтобы выйти за рамки внешнего вида, команда объединила два мощных подхода. Они измеряли активность генов по всему геному (транскриптомика) и определяли, какие малые молекулы, связанные с клеточным метаболизмом, присутствуют (метаболомика). Вместе эти «мульти‑омные» слои нарисовали картину того, как клетки производят и используют энергию. Клетки RPE в среде B27 смещались в сторону быстрого расщепления глюкозы в цитоплазме — пути, известного как гликолиз — и в сторону синтеза жиров для хранения. Напротив, клетки RPE в среде KSR предпочитали более полное окисление жирных кислот в митохондриях — энергетических «фабриках» клетки — и направляли это на окислительное производство энергии. Иными словами, два режима культивирования подтолкнули одни и те же исходные клетки к различным приоритетам использования энергии.
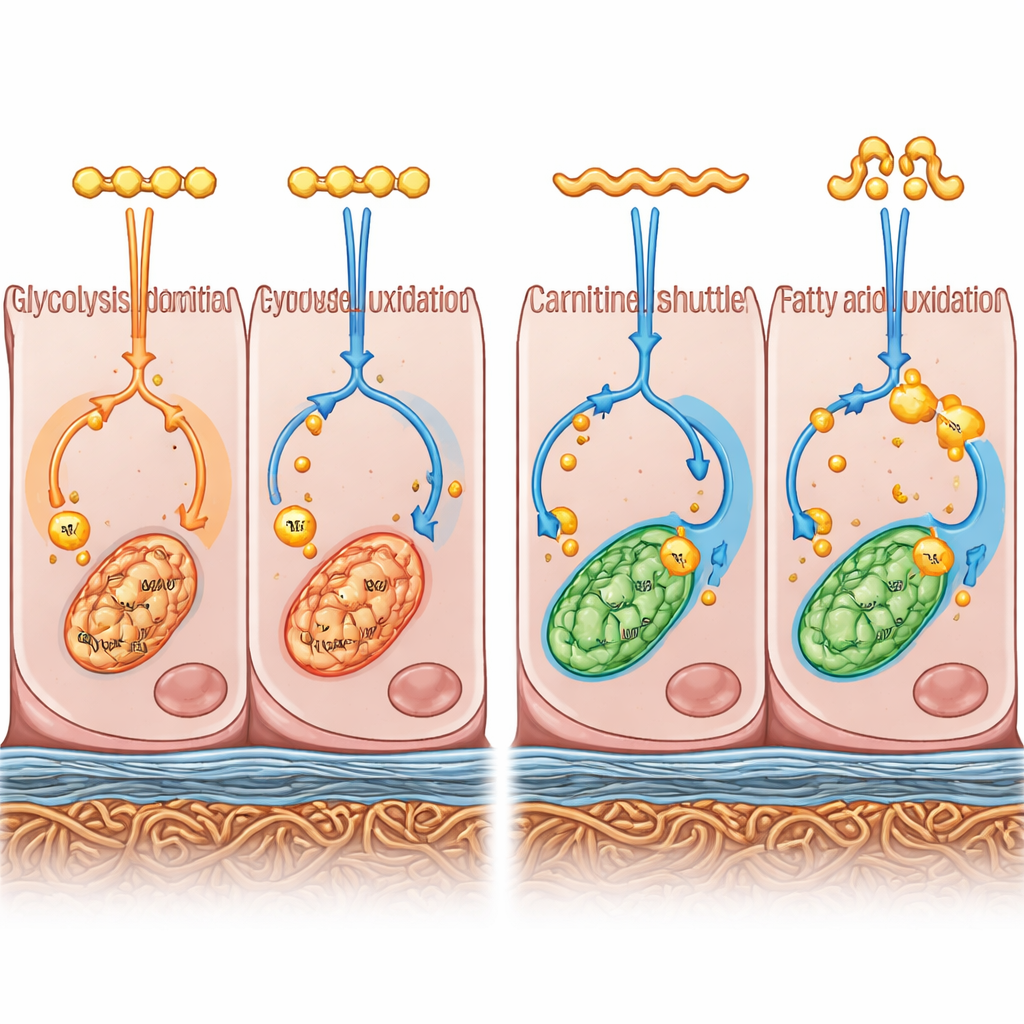
Как использование энергии формирует структуру и барьеры
Выбор топлива клетками был тесно связан с тем, как они организовывались как ткань. Клетки, выращенные в B27 с доминированием гликолиза, активировали больше генов, контролирующих внеклеточный матрикс — сеть белков и волокон, поддерживающая и склеивающая клетки. Эти клетки также демонстрировали более высокое электрическое сопротивление через слой, показатель того, насколько хорошо они формируют барьер, аналогичный глазному. Когда ученые химически замедляли гликолиз в клетках B27, экспрессия генов матрикса снижалась, а барьер ослабевал, что указывает на то, что более быстрый глюкозозависимый режим помогает строить и поддерживать прочное межклеточное уплотнение.
Более «кислородный» режим в другой среде
В клетках, выращенных в KSR, картинка была иной. Их внутренний метаболизм показывал повышенные уровни свободных жирных кислот и ключевых компонентов, необходимых для транспортировки этих жиров в митохондрии. Они аккумулировали меньше промежуточных соединений, связанных с жирными кислотами, которые могут накапливаться, когда процесс замедляется, что указывает на более эффективное сжигание жиров. Также в этих клетках было больше молекул, подающих сырье для окончательного энергетического аппарата, и активировалось больше генов окислительного фосфорилирования — кисородозависимого процесса, производящего большую часть АТФ, универсальной «валюты» энергии клетки. Интересно, что в обеих группах клеток центральный цикл метаболизма, цикл трикарбоновых кислот (ТКЦ), имел в целом схожую активность, что позволяет предположить: различия в основном заключаются в балансе подаваемых топлив и последующей конверсии энергии.
Что это означает для моделей болезней и будущих терапий
Для неспециалистов ключевая мысль такова: условия культивирования в лаборатории не просто сохраняют клетки RPE живыми — они помогают определить, какими именно RPE эти клетки станут. Одна среда смещает клетки в сторону глюкозо‑зависимого, ориентированного на барьер состояния с более выраженными структурными чертами, тогда как другая стимулирует режим сжигания жиров, зависящий от митохондрий, который может лучше отражать роль RPE как энергетического партнёра фоторецепторов. Ни одна из сред полностью не воспроизводит среду внутри человеческого глаза, но каждая захватывает разный фрагмент нормального поведения RPE. Авторы утверждают, что осознанное признание и целенаправленный выбор между этими метаболическими «персонами» будет жизненно важным при использовании RPE, полученных из стволовых клеток, для изучения слепящих болезней или приготовления клеток для трансплантации, где правильный баланс прочности барьера и энергетической поддержки может помочь сохранить зрение.
Цитирование: Zhang, F., Wang, C., Tang, Q. et al. Integrated transcriptomic and metabolomic analyses reveal distinct energy metabolic signatures and functional properties of RPE cells under two culture conditions. Sci Rep 16, 11992 (2026). https://doi.org/10.1038/s41598-026-39689-9
Ключевые слова: пигментный эпителий сетчатки, RPE, полученные из стволовых клеток, клеточный метаболизм, возрастная макулярная дегенерация, условия культивирования клеток