Clear Sky Science · tr
Karşıt öğrenme ile DEL ceplerinin desenlerini çözümlemek
Protein “ceplerine” bakmanın yeni ilaçları hızlandırmasının nedeni
Modern ilaç avcıları artık DNA-kodlu kütüphaneler (DEL’ler) kullanarak aynı anda trilyonlarca küçük molekülü tarayabiliyor. Yine de bu DEL kaynaklı moleküllerden yalnızca birkaçı gerçek ilaç haline geldi. Eksik olan büyük parçalardan biri, vücutta hangi proteinlerin DEL moleküllerinin tutunabileceği doğru türde girinti ve oyuklara—yani “ceplere”—sahip olduğunu bilmektir. Bu çalışma, başarılı DEL ceplerinin nasıl göründüğünü haritalayarak bu boşluğu dolduruyor ve benzer cepleri insan vücudu boyunca bulmak için ErePOC adında bir yapay zekâ modeli geliştiriyor.
DEL teknolojisi yeni ilaç moleküllerini nasıl arar
DEL’ler, bir çeşit barkodlu yem gibi çalışır. Kimyagerler küçük aday molekülleri kimlik etiketi görevi gören kısa DNA parçalarına bağlar ve bu etiketli moleküllerin geniş karışımlarını hedef proteinle temas ettirir. Yapışan moleküller DNA’nın dizilenmesiyle tespit edilir. Bu yöntem hızlı ve ucuzdur, ancak DEL tespitlerini gerçek ilaçlara dönüştürmek hâlâ zordur. Bunun nedenlerinden biri, DEL moleküllerinin su içinde üretilme biçimi ve DNA etiketinin bağlanma şekli gibi belli kimyasal kısıtlamalara sahip olmalarıdır. Bu kısıtlamalar, DEL’lerin belirli türde protein ceplerini tercih etmesine yol açar; ancak şimdiye dek bu tercihlerin sistematik bir haritası çıkarılmamıştı.
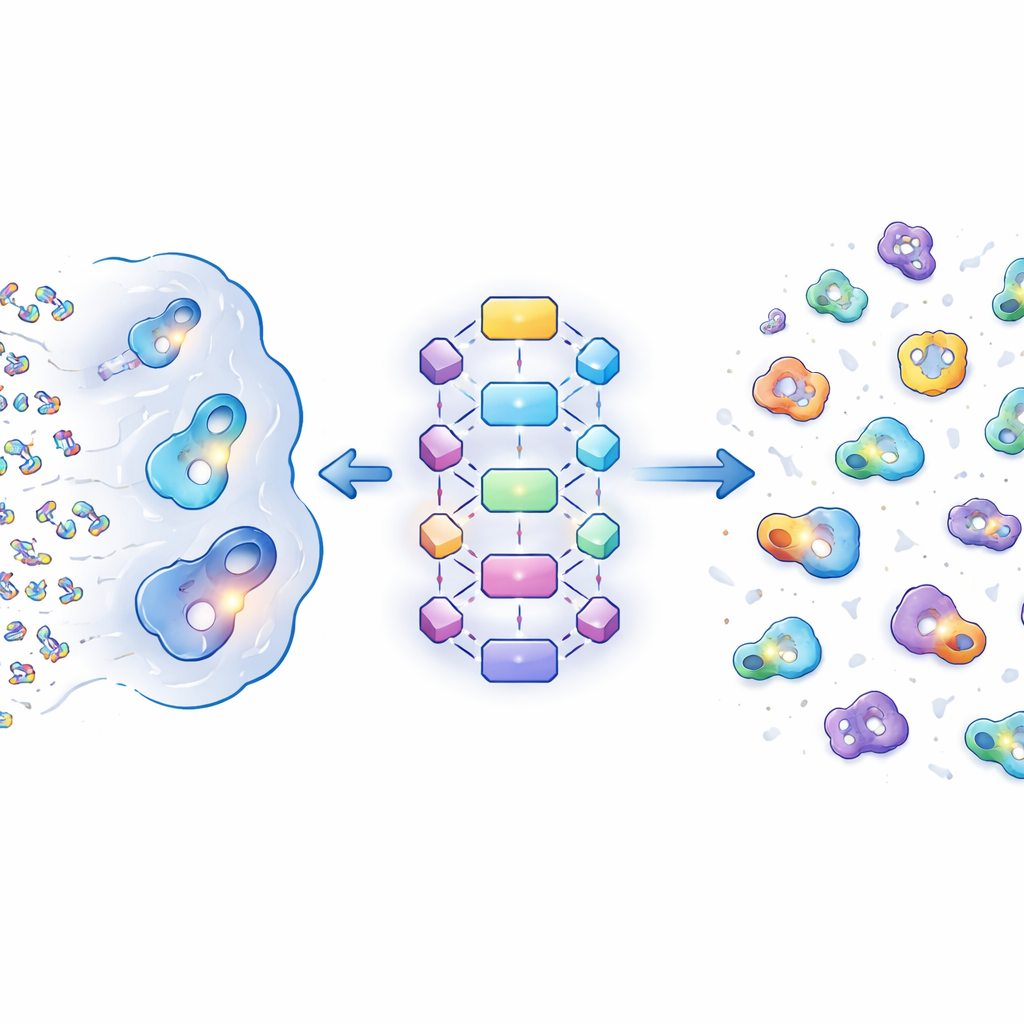
DEL molekülleri için bir cebi çekici kılan nedir
Yazarlar öncelikle farklı ligand türlerine bağlanan binlerce protein cebini karşılaştırdı: sıradan biyolojik küçük moleküller, FDA onaylı ilaçlar ve DEL tespitleri. DEL ve ilaç ceplerinin doğal ligand ceplerine göre daha büyük ve kimyasal olarak daha karmaşık olma eğiliminde olduğunu buldular. Özellikle, DEL cepleri daha açık ve hidrofobik—yani yağlı, suyu iten etkileşimleri destekleyen—olma eğilimindeydi, ancak bağlanmayı incelikle ayarlayan küçük ama önemli bir polar temas noktaları setini koruyorlardı. Tirozin ve fenilalanin gibi aromatik ve hidrofobik yüzeyler sağlayan bazı hacimli amino asitler, DEL ve ilaç bağlayan ceplerde tipik protein yüzeylerine göre daha sık görülüyordu. Genel olarak, DEL cepleri klasik ilaç-hedef ceplerine daha çok benziyor, ancak büyük, hidrofobik oyuklara ek bir eğilim gösteriyordu.
Ceplerin “kişiliklerini” tanımayı öğreten bir yapay zekâ
Basit boyut ve kimya sayımlarının ötesine geçmek için ekip, her bağlanma cebini bir çeşit parmak izi olarak ele alan ErePOC adlı bir temsil modeli geliştirdi. Model, milyonlarca diziden öğrenilen desenleri yakalayan protein dil modeli yerleştirmelerini temel alıyor ve bir cebi oluşturan kalıntılar hakkındaki bilgiyi sıkıştırarak kompakt bir sayısal vektöre dönüştürüyor. Karşıt öğrenme kullanılarak eğitilen ErePOC, kimyasal olarak benzer ligandlara bağlanan ceplerin bu soyut uzayda birbirine yakın, çok farklı moleküllere bağlananların ise uzak olacak şekilde düzenlenmesini sağlıyor. Yazarlar bu uzayı görselleştirdiklerinde, ATP veya hem gibi aynı kofaktöre bağlandığı bilinen ceplerin iyi ayrılmış kümeler oluşturduğunu gördüler; bu da modelin cepleri sadece genel protein şekline göre değil, işlevsel davranışlarına göre gruplayacak şekilde öğrendiğini gösteriyordu.
İnsan proteomunda DEL-dostu hedefleri bulmak
ErePOC eğitildikten sonra, araştırmacılar bilinen DEL ceplerini, ilaç ceplerini ve deneysel ile tahmini protein yapılardan elde edilmiş yüz binlerce cebi aynı manzaraya projeksiyonladılar. DEL cepleri genişçe dağıldı; bu da DEL taramasının prensipte geleneksel “ilaçlanabilir” alanın büyük bir kısmına ulaşabileceğini gösteriyor, ancak yine de büyük, hidrofobik ceplerle ilişkili belirli bölgelere açık tercihlerini korudular. Ekip daha sonra 23.000’den fazla AlphaFold ile tahmin edilmiş insan proteinini taradı, iyi tanımlanmış cepleri filtreledi ve ErePOC uzayında bilinen DEL ceplerine en çok benzeyenleri sordu. Başarılı DEL bölgelerine yüksek benzerlik gösteren yaklaşık 2.800 insan proteini belirlediler; transferazlar, hidrolazlar, oksidoredüktazlar, kromatin düzenleyicileri ve bazı RNA-bağlayıcı proteinler gibi ailelerde güçlü bir zenginleşme görüldü. Büyük bir sanal DEL ile yapılan takip bilgisayar bazlı eşleştirme (docking) çalışmaları, ErePOC tarafından işaretlenen bu ceplerin gerçekten DEL-benzeri molekülleri daha ziyade bağlama eğiliminde olduğunu öne sürdü.
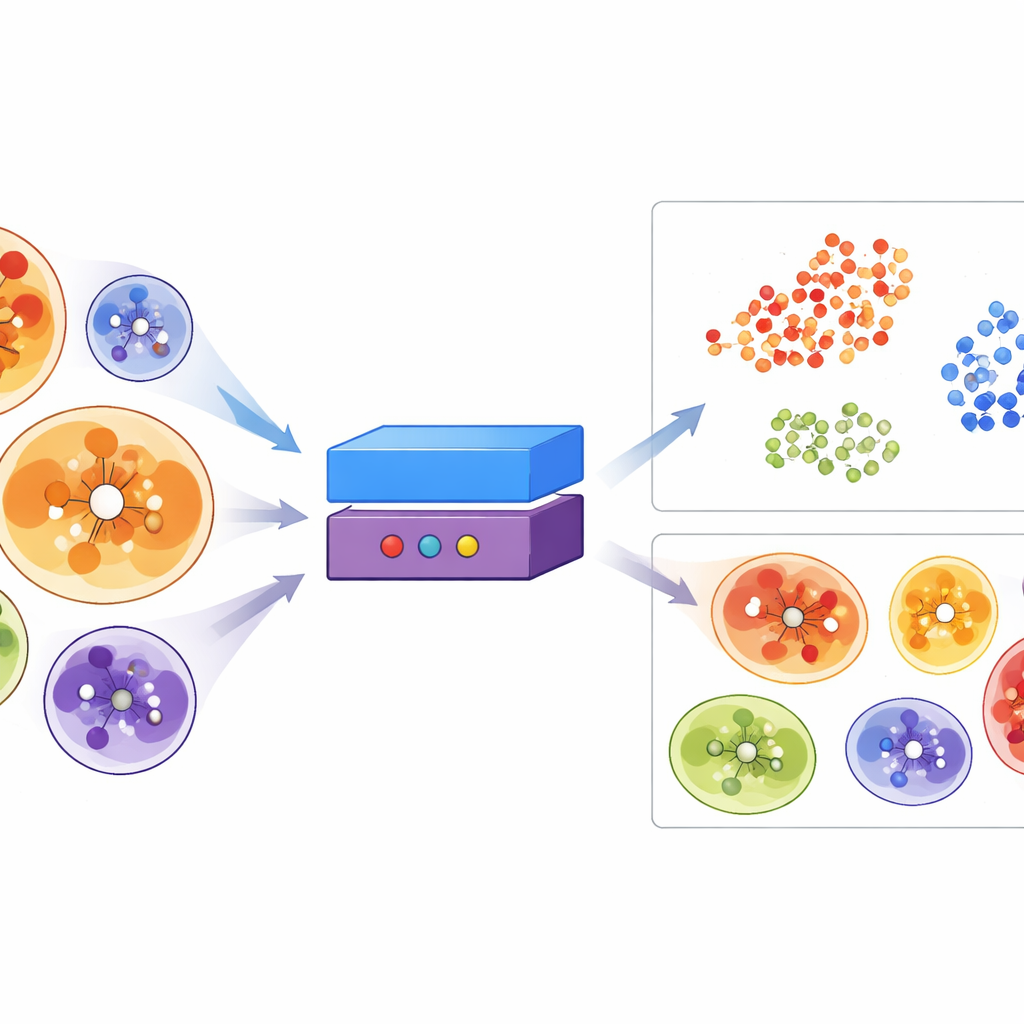
Gelecekteki ilaç keşfi için bunun önemi
Uzman olmayanlar için ana çıkarım, ultra-büyük kimyasal kütüphanelerin başarısının moleküller kadar doğru protein ceplerini seçmeye de dayandığıdır. Bu çalışma, DEL tespitlerinin genellikle büyük, esnek ve hidrofobik ceplerden geldiğini gösteriyor ve yalnızca dizi veya yapıdan bu tür cepleri tanımak için güçlü bir yapay zekâ aracı sunuyor. ErePOC’u kullanarak DEL taramalarını zaten DEL-uyumlu görünen ceplere sahip proteinlere odaklayarak, ilaç araştırmacıları daha umut verici hedefleri önceliklendirebilir, gereksiz tarama çabasını azaltabilir ve kromatin ile RNA-bağlayıcı proteinler gibi daha az keşfedilmiş sınıflara potansiyel olarak açılabilir. Kısacası, çalışma hem “DEL-ready” bir cebin nasıl göründüğüne dair daha net bir resim sunuyor hem de insan proteomu boyunca çok daha fazlasını bulmak için pratik bir harita ve pusula sağlıyor.
Atıf: Zhang, W., Wang, Y., Zhan, R. et al. Deciphering DEL pocket patterns through contrastive learning. Nat Commun 17, 2810 (2026). https://doi.org/10.1038/s41467-026-69663-y
Anahtar kelimeler: DNA-kodlu kütüphaneler, protein bağlanma cepleri, karşıt öğrenme, ilaç keşfi yapay zekası, ErePOC