Clear Sky Science · pl
Odkodowywanie wzorców kieszonek DEL za pomocą uczenia kontrastowego
Dlaczego analiza „kieszonek” białek może przyspieszyć rozwój nowych leków
Współczesni poszukiwacze leków mogą teraz testować biliony drobnych cząsteczek jednocześnie, korzystając z bibliotek kodowanych DNA, zwanych DEL. Mimo to tylko niewielka liczba związków pochodzących z DEL stała się faktycznymi lekami. Jednym z brakujących elementów jest wiedza, które białka w organizmie mają odpowiednie wnęki — „kieszonki” — do których cząsteczki z DEL mogą się przyczepić. Badanie to wypełnia tę lukę, mapując, jak wyglądają skuteczne kieszonki DEL, oraz budując model sztucznej inteligencji o nazwie ErePOC, służący do odnajdywania podobnych kieszonek w całym ludzkim proteomie.
Jak technologia DEL poszukuje nowych molekuł leczniczych
DEL działają trochę jak zapachowa przynęta z kodem kreskowym. Chemicy przyłączają małe kandydujące cząsteczki do krótkich fragmentów DNA pełniących rolę etykiet identyfikacyjnych, a następnie eksponują ogromne mieszaniny tych oznakowanych związków na białko będące celem. Molekuły, które przylegają, są identyfikowane poprzez sekwencjonowanie DNA. Ta metoda jest szybka i relatywnie tania, ale przekształcenie trafień z DEL w prawdziwe leki pozostaje trudne. Jedną z przyczyn są specyficzne ograniczenia chemiczne charakterystyczne dla związków DEL, wynikające m.in. z ich wytwarzania w wodnym środowisku i sposobu przyłączania tagu DNA. Ograniczenia te sprawiają, że preferują one określone typy kieszonek białkowych, które do tej pory nie były systematycznie zmapowane.
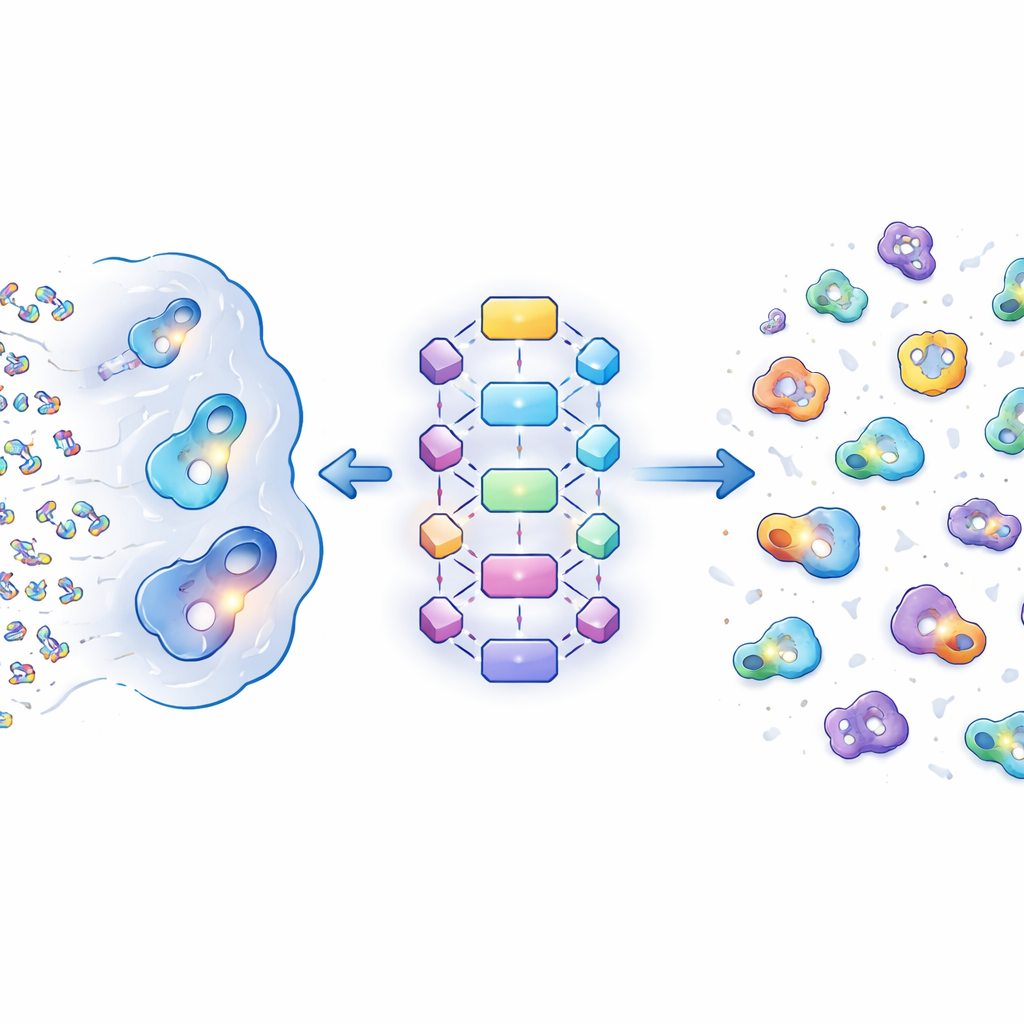
Co sprawia, że kieszonka jest atrakcyjna dla cząsteczek DEL
Autorzy najpierw porównali tysiące kieszonek białkowych wiążących różne typy ligandów: zwykłe biologiczne małe cząsteczki, leki zatwierdzone przez FDA oraz trafienia z DEL. Odkryli, że kieszonki związane z DEL i lekami mają tendencję do bycia większymi i bardziej złożonymi chemicznie niż kieszonki dla naturalnych ligandów. W szczególności kieszonki DEL są bardziej otwarte i hydrofobowe — co oznacza, że sprzyjają „oleistym”, odpychającym wodę interakcjom — jednocześnie zachowując niewielki, ale istotny zestaw spolaryzowanych punktów kontaktu, które doprecyzowują wiązanie. Pewne steryczne aminokwasy tworzące aromatyczne i hydrofobowe powierzchnie, takie jak tyrozyna i fenyloalanina, pojawiają się częściej w kieszonkach wiążących DEL i leki niż na typowych powierzchniach białek. Ogólnie rzecz biorąc, kieszonki DEL bardziej przypominają klasyczne kieszonki celów lekowych niż zwykłe miejsca metaboliczne, ale z dodatkowym przesunięciem w stronę dużych, hydrofobowych wnęk.
Nauczanie modelu AI, by rozpoznawał „osobowości” kieszonek
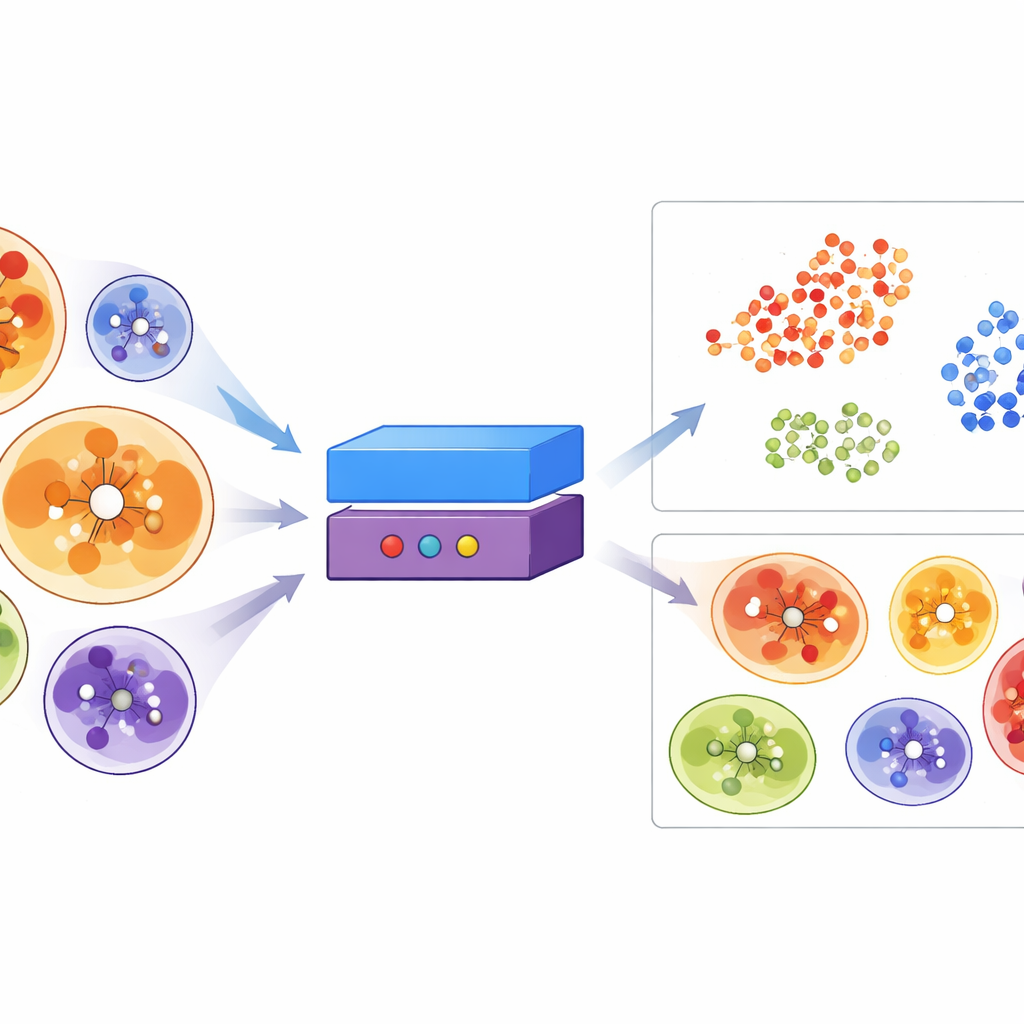
Aby wyjść poza proste miary rozmiaru i składu chemicznego, zespół stworzył ErePOC — model reprezentacji traktujący każdą kieszonkę jako rodzaj odcisku palca. Bazuje on na osadzeniach z modeli języka białkowego, które uchwyciły wzorce z milionów sekwencji, i kompresuje informacje o resztach tworzących kieszonkę do zwartego wektora numerycznego. Dzięki uczeniu kontrastowemu ErePOC jest trenowany tak, aby kieszonki wiążące chemicznie podobne ligandy znajdowały się blisko siebie w tej abstrakcyjnej przestrzeni, a te wiążące bardzo różne cząsteczki oddzielały się od siebie. Po wizualizacji tej przestrzeni kieszonki znane z wiązania tych samych kofaktorów, takich jak ATP czy hem, tworzyły wyraźnie oddzielone klastry, co świadczy o tym, że model nauczył się grupować kieszonki według funkcjonalnego zachowania, a nie tylko po kształcie całego białka.
Wyszukiwanie przyjaznych DEL celów w ludzkim proteomie
Po wytrenowaniu ErePOC, badacze umieścili znane kieszonki DEL, kieszonki leków oraz setki tysięcy kieszonek pochodzących ze struktur doświadczalnych i przewidywanych w tej samej przestrzeni. Kieszonki DEL rozproszyły się szeroko, co wskazuje, że skrining DEL w zasadzie może objąć dużą część tradycyjnej przestrzeni «drugowalnej», ale nadal wykazywały wyraźne preferencje dla regionów powiązanych z większymi, hydrofobowymi kieszonkami. Zespół przeskanował następnie ponad 23 000 białek ludzkich przewidzianych przez AlphaFold, filtrując pod kątem dobrze zdefiniowanych kieszonek i pytając, które z nich najbardziej przypominają znane kieszonki DEL w przestrzeni ErePOC. Zidentyfikowali niemal 2 800 ludzkich białek z kieszonkami wysoce podobnymi do udanych miejsc DEL, ze znaczną wzbogaconą reprezentacją rodzin takich jak transferazy, hydrolazy, oksydoreduktazy, regulatory chromatyny oraz niektóre białka wiążące RNA. Dalsze dokowanie komputerowe z dużą wirtualną biblioteką DEL zasugerowało, że kieszonki oznaczone przez ErePOC rzeczywiście mają tendencję do korzystniejszego wiązania cząsteczek podobnych do DEL.
Dlaczego to ma znaczenie dla przyszłego odkrywania leków
Dla osób niebędących specjalistami kluczowe wnioski są takie, że sukces ultra‑wielkich bibliotek chemicznych zależy równie mocno od wyboru odpowiednich kieszonek białkowych, co od samych molekuł. Praca ta pokazuje, że trafienia z DEL zwykle pochodzą z kieszonek dużych, elastycznych i hydrofobowych, oraz wprowadza potężne narzędzie AI umożliwiające rozpoznawanie takich kieszonek wyłącznie na podstawie sekwencji lub struktury. Korzystając z ErePOC, grupy prowadzące skrining DEL mogą skoncentrować wysiłki na białkach, których kieszonki już wyglądają na kompatybilne z DEL, dzięki czemu można priorytetyzować bardziej obiecujące cele, zmniejszyć straty związane z nieefektywnym skrinigiem i potencjalnie wejść w mniej eksplorowane klasy, takie jak regulatory chromatyny i białka wiążące RNA. Krótko mówiąc, badanie dostarcza zarówno jaśniejszego obrazu tego, jak wygląda «kieszonka gotowa na DEL», jak i praktycznej mapy i kompasu do odnalezienia wielu takich miejsc w całym ludzkim proteomie.
Cytowanie: Zhang, W., Wang, Y., Zhan, R. et al. Deciphering DEL pocket patterns through contrastive learning. Nat Commun 17, 2810 (2026). https://doi.org/10.1038/s41467-026-69663-y
Słowa kluczowe: Biblioteki kodowane DNA, kieszonki wiążące białka, uczenie kontrastowe, Sztuczna inteligencja w odkrywaniu leków, ErePOC