Clear Sky Science · sv
Avkoda DEL-ficka mönster genom kontrastiv inlärning
Varför studier av protein"fickor" kan påskynda nya läkemedel
Moderna läkemedelsjägare kan nu testa biljoner små molekyler samtidigt med hjälp av DNA-kodade bibliotek, eller DEL:er. Ändå har bara ett fåtal av de molekyler som identifierats via DEL blivit riktiga läkemedel. En viktig sak som saknats är kunskap om vilka proteiner i kroppen som faktiskt har rätt slags nischer—"fickor"—för DEL-molekyler att fästa i. Denna studie tar itu med den luckan genom att kartlägga hur framgångsrika DEL-fickor ser ut och bygga en artificiell intelligensmodell, kallad ErePOC, för att hitta liknande fickor i hela människokroppen.
Hur DEL-tekniken söker efter nya läkemedelsmolekyler
DEL fungerar lite som märkta fiskedrag. Kemister fäster små kandidat-molekyler vid korta DNA-bitar som fungerar som ID-taggar, och utsätter sedan stora blandningar av dessa märkta molekyler för ett målprotein. Molekyler som fastnar läses av genom DNA-sekvensering. Detta tillvägagångssätt är snabbt och billigt, men att förvandla DEL-hits till verkliga läkemedel är fortfarande svårt. En anledning är att DEL-molekyler delar vissa kemiska begränsningar, till exempel hur de syntetiseras i vatten och hur DNA-taggen är fäst. Dessa begränsningar gör att de tenderar att föredra särskilda typer av proteinfickor, men hittills har dessa preferenser inte kartlagts systematiskt.
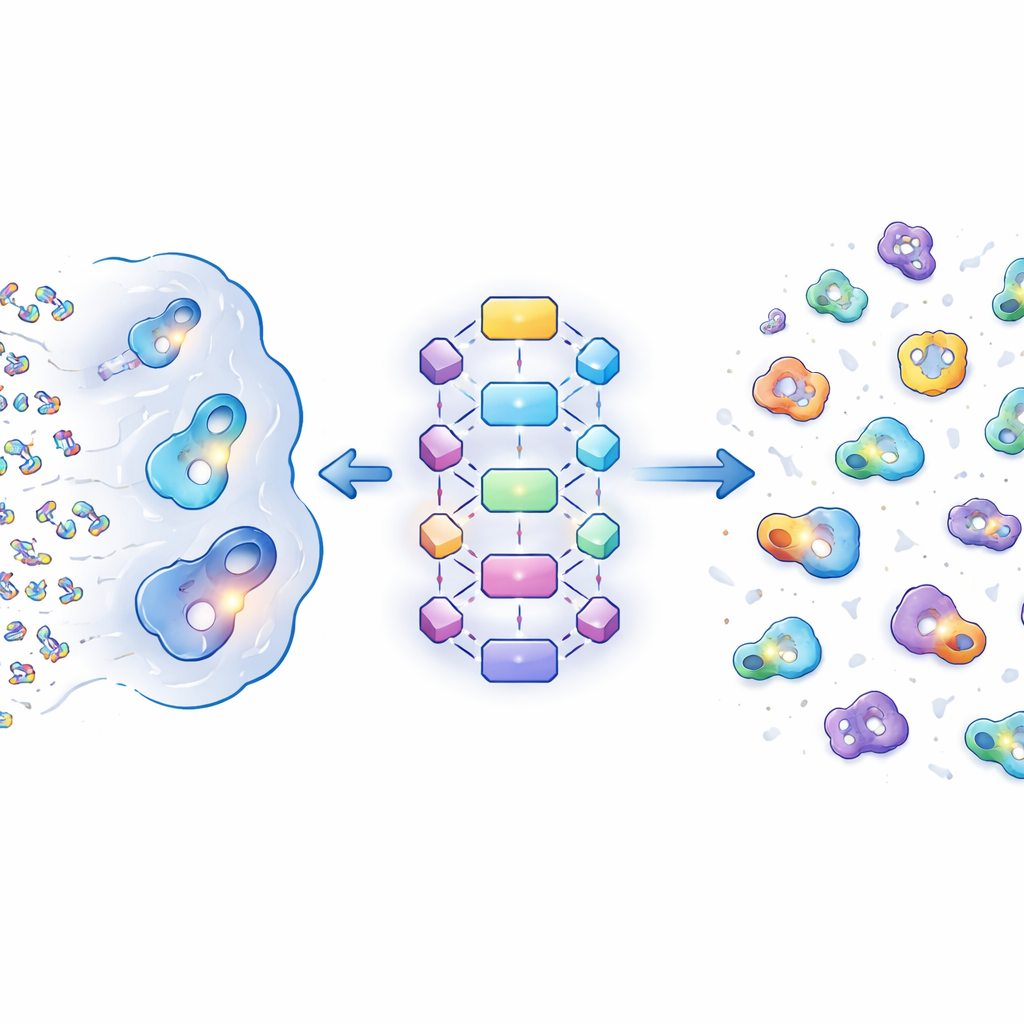
Vad som gör en ficka attraktiv för DEL-molekyler
Författarna jämförde först tusentals proteinfickor som binder olika typer av ligander: vanliga biologiska småmolekyler, FDA-godkända läkemedel och DEL-hits. De fann att DEL- och läkemedelsfickor tenderar att vara större och kemiskt mer komplexa än fickor för naturliga ligander. Specifikt är DEL-fickor mer öppna och hydrofoba—det vill säga de gynnar oljiga, vattenavstötande interaktioner—samtidigt som de behåller en liten men viktig uppsättning polära kontaktpunkter som finjusterar bindningen. Vissa skrymmande aminosyror som ger aromatiska och hydrofoba ytor, såsom tyrosin och fenylalanin, förekommer oftare i DEL- och läkemedelsbindande fickor än på typiska proteinytor. Sammantaget liknar DEL-fickor mer klassiska läkemedelsmålfickor än vanliga metabola platser, men med en extra förskjutning mot stora, hydrofoba håligheter.
Att lära en AI-modell att känna igen fickors "personligheter"
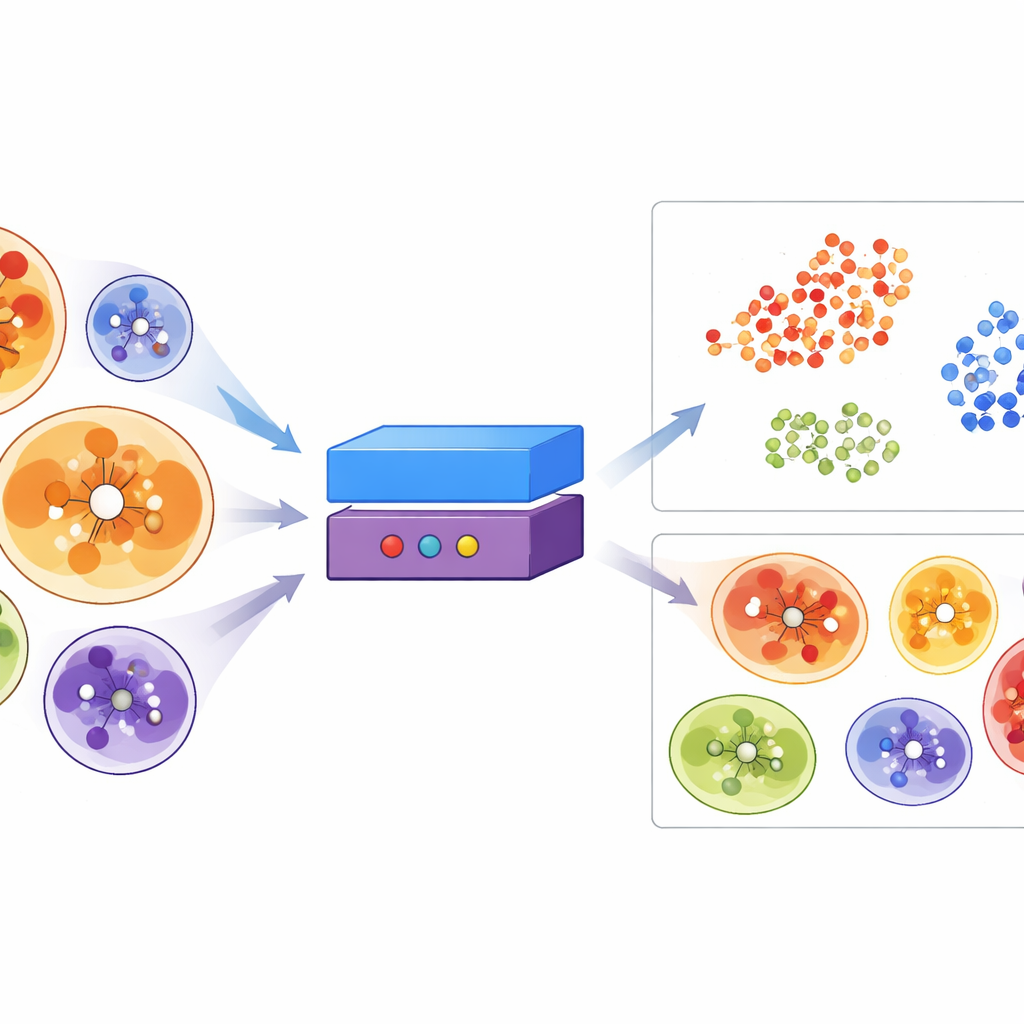
För att gå bortom enkla mått på storlek och kemi byggde teamet ErePOC, en representationsmodell som behandlar varje bindningsficka som ett slags fingeravtryck. Den utgår från inbäddningar från protein-språkmodeller, som fångar mönster lärda från miljontals sekvenser, och komprimerar informationen om de rester som bildar en ficka till en kompakt numerisk vektor. Med kontrastiv inlärning tränas ErePOC så att fickor som binder kemiskt liknande ligander hamnar nära varandra i detta abstrakta rum, medan de som binder mycket olika molekyler glider isär. När författarna visualiserade detta rum bildade fickor som är kända för att binda samma kofaktorer, som ATP eller hem, tydligt separerade kluster—vilket visar att modellen lärt sig gruppera fickor efter funktionellt beteende snarare än enbart efter proteinernas övergripande form.
Hitta DEL-vänliga mål i hela det mänskliga proteomet
Med ErePOC tränad projicerade forskarna kända DEL-fickor, läkemedelsfickor och hundratusentals fickor från experimentella och förutsagda proteinstrukturer in i samma landskap. DEL-fickor spreds brett, vilket indikerar att DEL-screening i princip kan nå stora delar av det traditionella "druggable" utrymmet, men de visade fortfarande tydliga preferenser för vissa regioner kopplade till större, hydrofoba fickor. Teamet skannade därefter mer än 23 000 AlphaFold-förutsagda humana proteiner, filtrerade för väl definierade fickor och frågade vilka som mest liknade kända DEL-fickor i ErePOC-rummet. De identifierade nästan 2 800 humana proteiner med fickor som var mycket lika framgångsrika DEL-ställen, med stark överrepresentation i familjer som transferaser, hydrolaser, oxideroreduktaser, kromatinregulatorer och vissa RNA-bindande proteiner. Uppföljande datorbaserad dokning med ett stort virtuellt DEL föreslog att dessa av ErePOC flaggade fickor faktiskt tenderar att binda DEL-liknande molekyler mer gynnsamt.
Varför detta betyder något för framtida läkemedelsupptäckt
För icke-specialister är huvudpoängen att framgången för ultrastora kemiska bibliotek beror lika mycket på att välja rätt proteinfickor som på själva molekylerna. Detta arbete visar att DEL-hits tenderar att komma från fickor som är stora, flexibla och hydrofoba, och introducerar ett kraftfullt AI-verktyg för att känna igen sådana fickor enbart utifrån sekvens eller struktur. Genom att använda ErePOC för att rikta DEL-screening mot proteiner vars fickor redan ser DEL-kompatibla ut kan forskare prioritera mer lovande mål, minska bortkastad screeninginsats och potentiellt utvidga till mindre utforskade klasser som kromatin- och RNA-bindande proteiner. Sammanfattningsvis erbjuder studien både en klarare bild av hur en "DEL-redo" ficka ser ut och en praktisk karta och kompass för att hitta många fler av dem i det mänskliga proteomet.
Citering: Zhang, W., Wang, Y., Zhan, R. et al. Deciphering DEL pocket patterns through contrastive learning. Nat Commun 17, 2810 (2026). https://doi.org/10.1038/s41467-026-69663-y
Nyckelord: DNA-kodade bibliotek, proteins bindningsfickor, kontrastiv inlärning, AI för läkemedelsupptäckt, ErePOC