Clear Sky Science · he
פענוח דפוסי כיסי DEL באמצעות למידה קונטרסטיבית
מדוע הסתכלות על "כיסים" בחלבון יכולה להאיץ פיתוח תרופות חדשות
ציידי תרופות מודרניים יכולים כעת לבדוק טריליוני מולקולות זעירות בו‑זמנית באמצעות ספריות מקודדות ב‑DNA, או DEL. ועדיין, רק מספר מועט מהמולקולות שזוהו מ‑DEL הפכו לתרופות בפועל. חסרון מרכזי הוא חוסר הוודאות אילו חלבונים בגוף אכן מכילים את החריצים והנישות—"כיסים"—המתאימים לקשירת מולקולות DEL. המחקר הזה מתמודד עם הפער על‑ידי מיפוי המאפיינים של כיסי DEL מוצלחים ובניית מודל בינה מלאכותית, שנקרא ErePOC, כדי לזהות כיסים דומים בכל רחבי הפרוטאום האנושי.
כיצד טכנולוגיית DEL מחפשת מולקולות תרופתיות חדשות
DEL פועלת קצת כמו פיתיונות דיג עם ברקודים. כימאים מצמידים מועמדי מולקולות קטנים לחתיכות קצרות של DNA המשמשות כתגי זיהוי, ואז חושפים תערובות עצומות של מולקולות מתוייגות אלה לחלבון מטרה. מולקולות שנשארות קשורות מזוהות על‑ידי ריצוף ה‑DNA. שיטה זו מהירה וזולה יחסית, אך הפיכה של "היטים" מ‑DEL לתרופות ממשיות נשארת מאתגרת. סיבה אחת היא שמולקולות DEL מושפעות מגבולות כימיים מסוימים, כמו האופן שבו מיוצרות במים ואיך תווית ה‑DNA מחוברת. מגבלות אלה גורמות להן להעדיף סוגים מסוימים של כיסי חלבון, אך עד כה העדפות אלה לא ממופו באופן שיטתי.
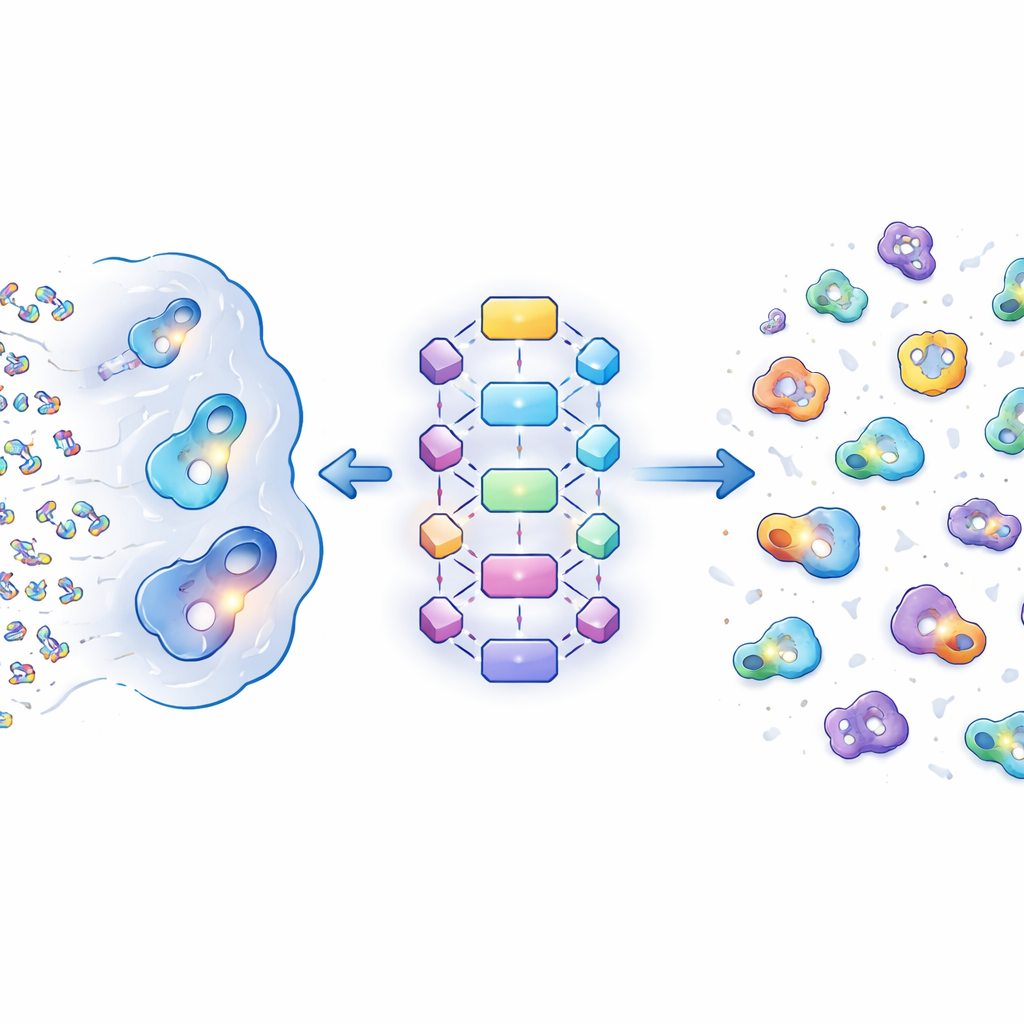
מה מושך כיסים למולקולות DEL
המחברים השוו תחילה אלפי כיסים של חלבונים שקושרים סוגים שונים של ליגנדים: מולקולות ביולוגיות קטנות טיפוסיות, תרופות שאושרו על‑ידי ה‑FDA ו"היטים" מ‑DEL. הם מצאו שכיסי DEL וכיסי תרופות נוטים להיות גדולים ומורכבים כימית יותר מאשר כיסים הקושרים ליגנדים טבעיים. בפרט, כיסי DEL פתוחים יותר והידרופוביים יותר—כלומר מעדיפים אינטראקציות שמעדיפות שטחים שדוחים מים—ועדיין שומרים על קבוצה קטנה אך משמעותית של נקודות מגע פולריות שמדייקות את הקשירה. חומצות אמינו מסוימות ובולטות שמספקות משטחים ארומטיים והידרופוביים, כגון טירוזין ופנילאלנין, מופיעות בתדירות גבוהה יותר בכיסים שקושרים DEL ותרופות מאשר על פני השטח החלבוני הטיפוסי. בסך הכל, כיסי DEL דומים יותר לכיסי מטרה טיפוסיים של תרופות מאשר לאתרים מטבוליים רגילים, אך עם הטיה נוספת לעבר חללים גדולים והידרופוביים.
לימוד מודל בינה מלאכותית לזהות "אישיות" של כיסים
כדי להתקדם מעבר לספירות של גודל וכימיה, הקבוצה בנתה את ErePOC, מודל ייצוג שטוען כל כיס כטביעת אצבע. המודל מתחיל מתוך מוטמעות של מודלי שפה לחלבון, שתופסות דפוסים שנלמדו ממיליוני רצפים, ודוחס את המידע על שיירי החומצות שמרכיבים כיס לתוך וקטור מספרי קומפקטי. באמצעות למידה קונטרסטיבית, ErePOC מאומן כך שכיסים שקושרים ליגנדים כימית דומים יקרבו זה לזה במרחב המופשט, וכיסים שקושרים מולקולות שונות מאוד יסתדרו רחוקים. כאשר המחברים ויזואליזו את המרחב הזה, כיסים הידועים כקשורים לאותם קופקטורים, כמו ATP או המה, יצרו אשכולות נפרדות היטב, מה שמראה שהמודל למד לקבץ כיסים לפי התנהגות פונקציונלית ולא רק לפי צורת החלבון הכללית.
מציאת מטרות ידידותיות ל‑DEL בפרוטאום האנושי
בשימוש ב‑ErePOC המאומן, החוקרים הקרינו כיסי DEL ידועים, כיסי תרופות, ומאות אלפי כיסים ממבנים חלבוניים ניסיוניים ומחושבים אל אותו נוף. כיסי DEL התפזרו במרחב, מה שמרמז שסינון DEL יכול בתיאוריה להגיע לחלק גדול מהמרחב ה"ניתן לטיפול" המסורתי, אך הם עדיין הראו העדפות ברורות לאזורים הקשורים לכיסים גדולים והידרופוביים. הצוות סרק אז יותר מ‑23,000 חלבונים אנושיים שחזו מתקבצי AlphaFold, סינן כיסים מוגדרים היטב ושאל אילו מהם דומים ביותר לכיסי DEL ידועים במרחב ErePOC. הם זיהו כמעט 2,800 חלבונים אנושיים עם כיסים הדומים מאוד לאתרים מוצלחים של DEL, עם העשרה חזקה במשפחות כגון טרנספראזות, הידרולאזות, אוקסידורדוקטאזות, רגולטורים של כרומטין וחלק מחלבוני קשירת RNA. עיגון ממוחשב נוסף עם DEL וירטואלי גדול הציע כי הכיסים שסומנו על‑ידי ErePOC אכן נוטים לקשור מולקולות דמויות DEL ביתר עדיפות.
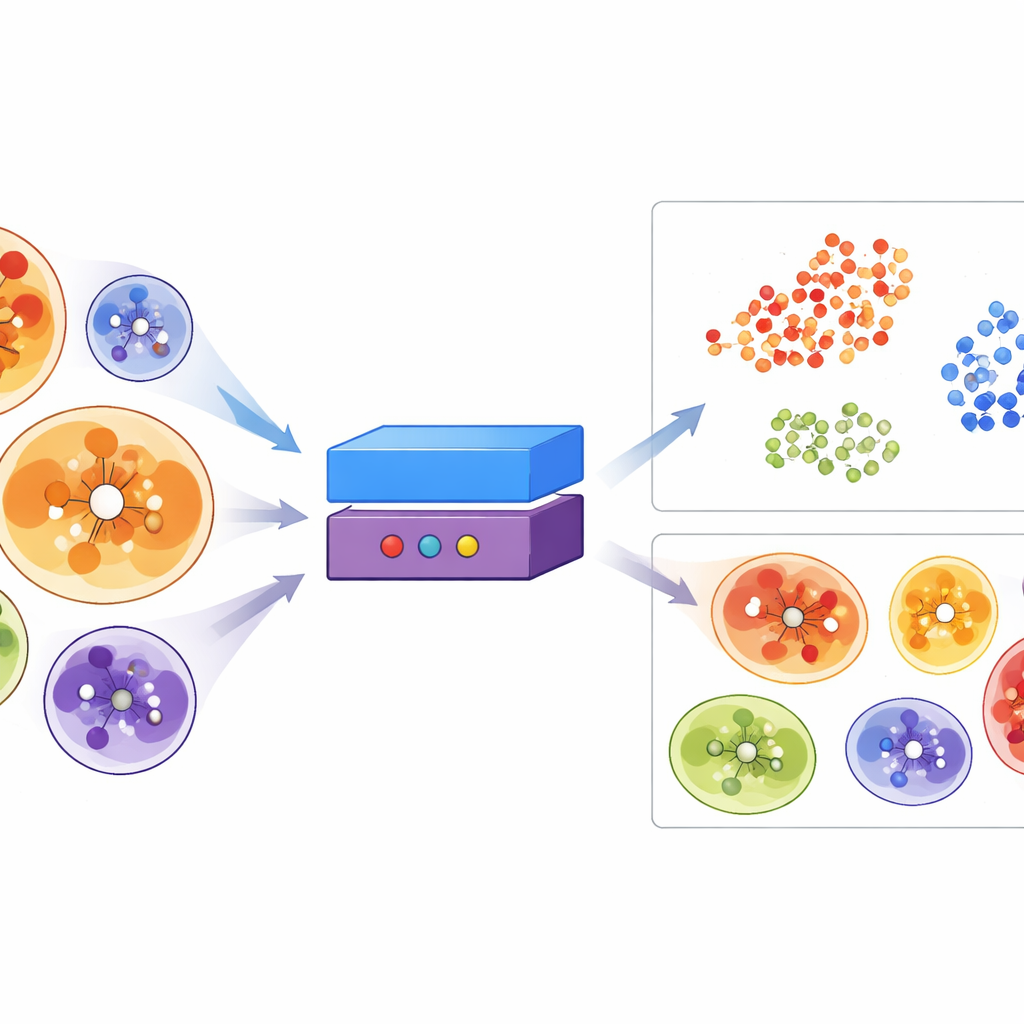
מדוע זה חשוב לגילוי תרופות בעתיד
ללא מומחיות מיוחדת, המסקנה המרכזית היא שהצלחת ספריות כימיות ענקיות תלויה לא פחות בבחירת כיסי החלבון הנכונים מאשר במולקולות עצמן. עבודה זו מראה שהיטים מ‑DEL נוטים להופיע בכיסים שהם גדולים, גמישים והידרופוביים, ומציגה כלי בינה מלאכותית רב‑עוצמה לזיהוי כיסים כאלה מתוך רצף או מבנה בלבד. באמצעות שימוש ב‑ErePOC למקד את סקרי DEL על חלבונים שכיסיהם כבר נראים תואמי‑DEL, ציידי תרופות יכולים לתת עדיפות למטרות מבטיחות יותר, להפחית בזבוז מאמצי סינון, ואולי להתרחב לכיתות פחות ממודעות כגון חלבוני כרומטין וחלבוני קשירת RNA. בקיצור, המחקר מציע הן תמונה ברורה יותר של איך נראה "כיס מוכן ל‑DEL" והן מפת דרכים פרקטית למציאת רבים נוספים מהם בפרוטאום האנושי.
ציטוט: Zhang, W., Wang, Y., Zhan, R. et al. Deciphering DEL pocket patterns through contrastive learning. Nat Commun 17, 2810 (2026). https://doi.org/10.1038/s41467-026-69663-y
מילות מפתח: ספריות מקודדות ב‑DNA, כיסי קשירה של חלבונים, למידה קונטרסטיבית, בינה מלאכותית לגילוי תרופות, ErePOC