Clear Sky Science · tr
Redoks döngüsel nitroksit, hücresel demir bulunabilirliğini sınırlar ve demir-kükürt kümesi metabolizmini seçici olarak inhibe eder
Günlük Sağlık İçin Neden Önemli
Hücrelerimiz sadece kandaki oksijeni taşımak için değil, aynı zamanda enerji üretimini sağlamak ve DNA’yı onarmak için de demire bağımlıdır. Yine de yanlış türde çok fazla demir zararlı kimyasal reaksiyonları körükleyebilir ve hatta bir hücre ölüm biçimini tetikleyebilir. Bu çalışma, birkaç hastalık modelinde zaten test edilmiş küçük bir molekül olan Tempol’un hücrelerin demiri işlemesini nasıl ince ince değiştirdiğini araştırıyor. Demiri daha az kullanılabilir bir duruma iterek ve vitamin C’nin etkisine karşı çıkarak, Tempol demir kullanımını kontrol eden daha önce yeterince takdir edilmemiş bir katmanı ortaya koyuyor; bu katman nörodejenerasyondan kansere kadar uzanan durumlarla ilgili olabilir.
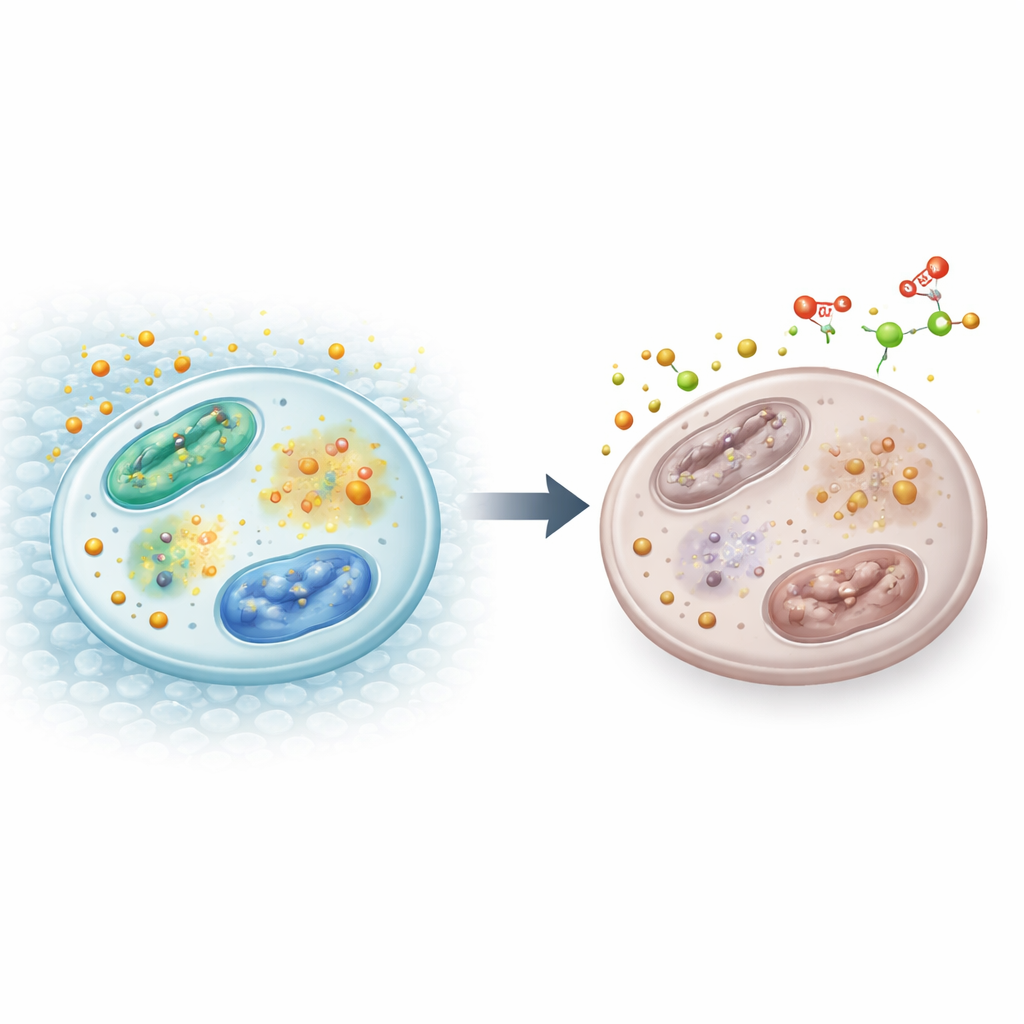
Demirin İnce Dengesi
Hücrelerin içinde demir ya serbest iyonlar olarak ya da enerji üretimi, DNA kopyalanması ve diğer hayati süreçlerde birçok enzimin işlevine yardımcı olan demir–kükürt kümeleri adı verilen özel yapılara entegre olarak kullanılır. Demir kimyasal durumlar arasında kolaylıkla geçiş yapabildiği için hem faydalı hem de potansiyel olarak zararlıdır. Bu nedenle hücreler, küçük ve dikkatle yönetilen bir kullanılabilir demir havuzunu korumak için sensörler ve düzenleyiciler ağına güvenir. IRP1 ve IRP2 adlı iki protein demir durumunu algılar ve ne kadar demirin içeri alındığını, depolandığını veya dışarı verildiğini ayarlar. Aynı zamanda vitamin C, birçok enzimin düzgün çalışması için gereken kimyasal olarak “indirgenmiş” formda demiri korumaya yardımcı olur.
Demiri Sınırlamanın Farklı Bir Yolu
Araştırmacılar, daha önce esas olarak bir antioksidan olarak hareket ettiği ve doğrudan demir–kükürt kümelerine zarar verdiği düşünülen redoks-aktif bileşik Tempol’a odaklandı. Tempol’un bunun yerine daha çok bir “anti–vitamin C” gibi davrandığını buldular. Hücre kültürlerinde Tempol, kullanılabilir demir havuzunu azalttı ve demir kıtlığının bir işareti olan IRP2’yi stabilize etti. Bununla birlikte, klasik demir bağlayıcı ilaçların aksine, Tempol’un etkileri sadece ek demir ekleyerek tam olarak geri alınamadı ve Tempol aynı şekilde mitokondrilerden güçlü biçimde demir çekmedi. Bunun yerine etkisi neredeyse tamamen vitamin C eklenmesiyle geri döndürüldü; vitamin C hücre büyümesini, demir kullanımını ve demir–kükürt kümelerine bağlı enzimleri geri getirdi. Bu, Tempol’un demiri aktif durumuna geri döndüren vitamin C destekli geri dönüşüm sürecine müdahale ederek demiri daha az reaktif bir forma kaydırdığı bir mekanizmaya işaret ediyor.
Ana Hücresel Süreçlere Seçici Etki
Tempol tüm hücre tiplerini aynı şekilde etkilemedi. Onlarca insan kanser hücre hattından oluşan bir panelde bazıları Tempol’e iyi dayanırken, diğerlerinde büyüme belirgin şekilde azaldı. Duyarlı hücreler özellikle enerji metabolizminin merkezinde yer alan mitokondriyal bir enzim olan ACO2 dahil olmak üzere birden fazla demir–kükürt kümesi enziminin aktivitesini kaybetti. Genetik veri setleri, ACO2’ye daha bağımlı olan hücre hatlarının Tempol’a karşı daha savunmasız olduğunu ortaya koydu; bu da demir–kükürt kimyasına daha fazla dayanan hücrelerin demirin redoks dengesi bozulduğunda başa çıkma kapasitesinin daha düşük olduğunu düşündürüyor. Önemli olarak, birçok dokunun vücutta deneyimlediğine daha yakın olan daha düşük oksijen seviyeleri, demir–kükürt kümelerini ve hücre büyümesini Tempol’dan korurken demir algılama yanıtını engellemedi; bu da laboratuvarın standart koşulları altında görülen zarara oksijenin kendisinin katkıda bulunduğunu gösteriyor.
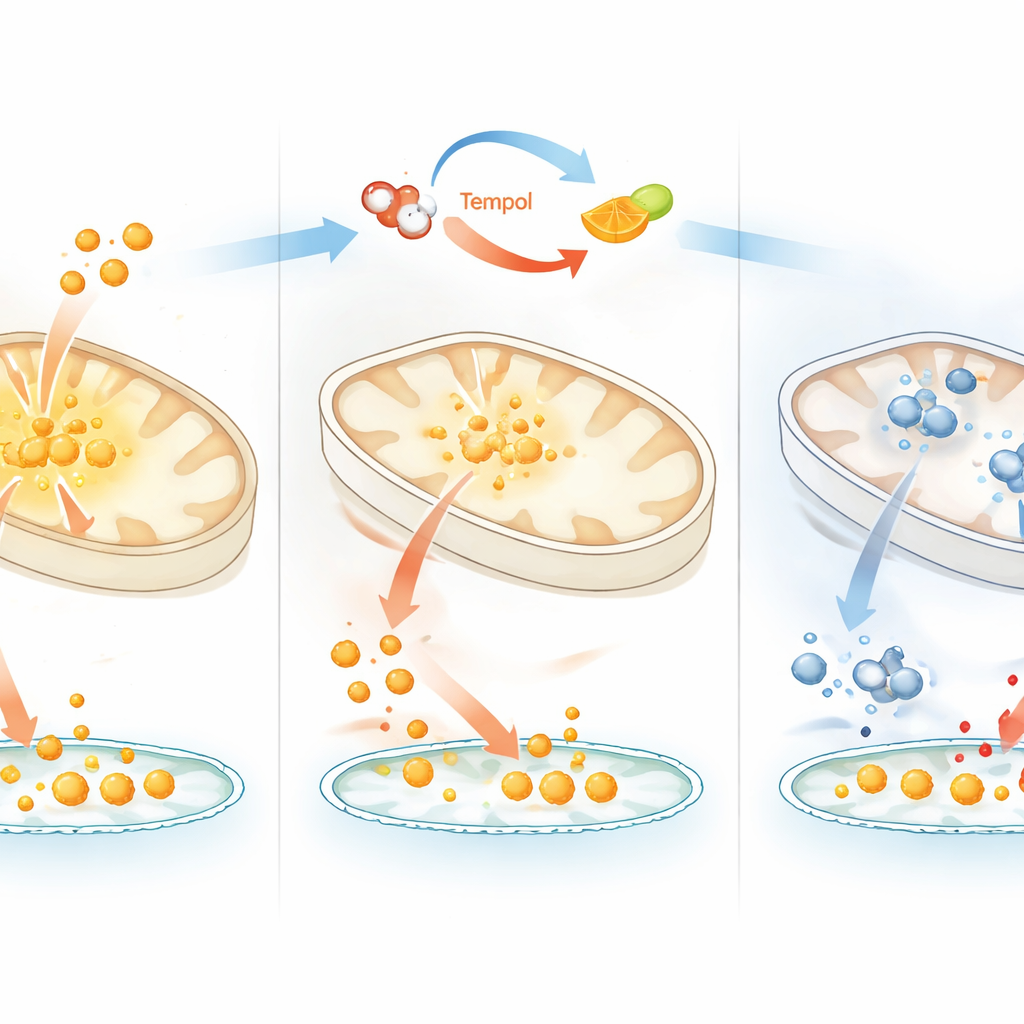
Demir, Hücre Ölümü ve Hastalık Bağlantıları
Metabolizmanın ötesinde, Tempol’un redoks-temelli demir sınırlaması iki çarpıcı sinyal etkisine sahipti. Birincisi, hem demir hem de vitamin C destekli enzimlere bağlı olarak yıkıma uğrayan düşük oksijene cevap veren bir protein olan HIF1α’yı hızla stabilize etti. İkincisi, membran yağlarına demir katalizli hasarın yol açtığı bir hücre ölümü türü olan ferroptozu tutarlı biçimde bastırdı. Her iki etki de kullanılabilir demiri azaltan ancak demir–kükürt kümelerinin belirgin kaybından önce görülen Tempol dozlarında ortaya çıktı; bu da demirin kimyasal durumundaki ılımlı değişimlerin stres yanıtlarını ve hücre hayatta kalmasını güçlü şekilde etkileyebileceğini gösteriyor. Yazarlar ayrıca benzer davranışın genel antioksidanlar veya indirgeyici ajanlarla yeniden üretilmediğini göstererek Tempol’un spesifik vitamin C ile ilişkili kimyasallığını vurguladılar.
Gelecekteki Tedaviler İçin Anlamı
Daha açık bir ifadeyle bu çalışma, Tempol’un hücrelerin demiri kimyasal olarak nasıl “ayarladığını” hedefli biçimde bozduğunu, büyük ölçüde vitamin C’ye karşı çıkarak yaptığını gösteriyor. Bu, birçok enzimin ihtiyaç duyduğu demir formunu azaltır, demir kaynaklı hücre ölümünü zayıflatır ve ACO2 gibi demir–kükürt kümesi enzimlerine güçlü şekilde bağımlı olan belirli hücrelerde büyümeyi yavaşlatır. Demir yönetimindeki bozulmanın beyin hastalıkları, enfeksiyonlar ve kanserle ilişkilendirildiği düşünüldüğünde, bu redoks-temelli demir sınırlamasını anlamak ve potansiyel olarak kullanmak, demiri basitçe uzaklaştırmak yerine hücrelerin demiri nasıl kullanabileceğini değiştiren yeni stratejilerin kapısını açıyor.
Atıf: Terzi, E.M., Fujihara, K.M., Molenaars, M. et al. Redox cycling nitroxide limits cellular iron availability and selectively inhibits iron-sulfur cluster metabolism. Cell Death Discov. 12, 165 (2026). https://doi.org/10.1038/s41420-026-03042-w
Anahtar kelimeler: demir metabolizması, Tempol, vitamin C, demir–kükürt kümeleri, ferroptoz