Clear Sky Science · de
Redoxzyklus des Nitroxids begrenzt zelluläre Eisenverfügbarkeit und hemmt selektiv den Eisen-Schwefel-Cluster-Stoffwechsel
Warum das für die alltägliche Gesundheit wichtig ist
Unsere Zellen sind auf Eisen angewiesen – nicht nur, um Sauerstoff im Blut zu transportieren, sondern auch, um Energie zu erzeugen und DNA zu reparieren. Zu viel von der falschen Form von Eisen kann jedoch schädliche chemische Reaktionen fördern und sogar eine Form des Zelltods auslösen. Diese Studie untersucht, wie ein kleines Molekül namens Tempol, das bereits in mehreren Krankheitsmodellen getestet wurde, die zelluläre Eisenhandhabung subtil verändert. Indem es Eisen in einen weniger nutzbaren Zustand verschiebt und der Wirkung von Vitamin C entgegenwirkt, legt Tempol eine bislang wenig beachtete Steuerungsebene der Eisenverwertung offen, die für Erkrankungen von Neurodegeneration bis Krebs relevant sein könnte.
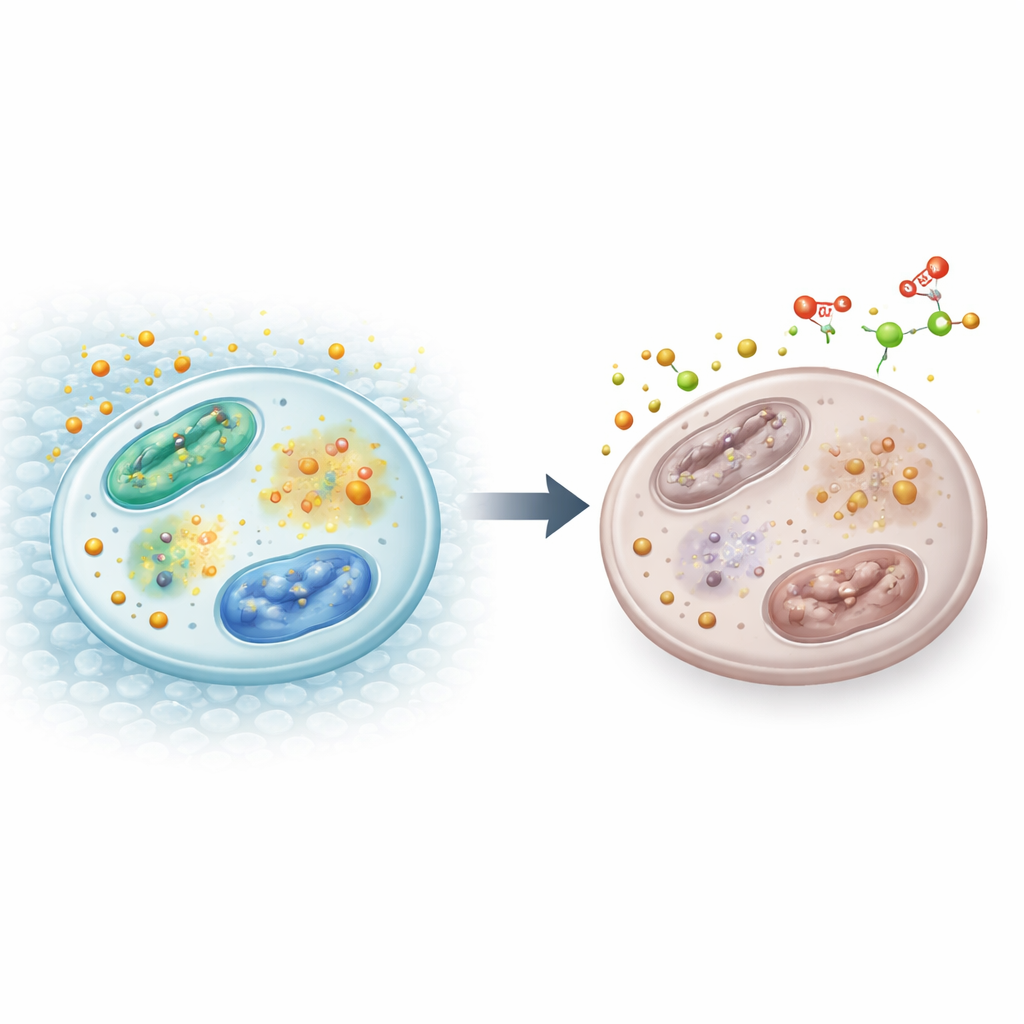
Das empfindliche Gleichgewicht des Eisens
Innerhalb der Zellen wird Eisen entweder als freie Ionen verwendet oder in speziellen Strukturen, den Eisen–Schwefel-Clustern, eingebaut, die vielen Enzymen bei Energiegewinnung, DNA-Replikation und anderen lebenswichtigen Prozessen helfen. Weil Eisen leicht zwischen chemischen Zuständen wechseln kann, ist es sowohl nützlich als auch potenziell schädlich. Zellen verlassen sich daher auf ein Netzwerk von Sensoren und Regulatoren, um einen kleinen, sorgfältig verwalteten Pool verfügbaren Eisens zu erhalten. Zwei Proteine, IRP1 und IRP2, messen den Eisenstatus und regeln, wie viel Eisen importiert, gespeichert oder exportiert wird. Gleichzeitig hilft Vitamin C, Eisen in einer chemisch „reduzierten“ Form zu halten, die viele Enzyme für ihre Funktion benötigen.
Ein anderer Weg, Eisen zu begrenzen
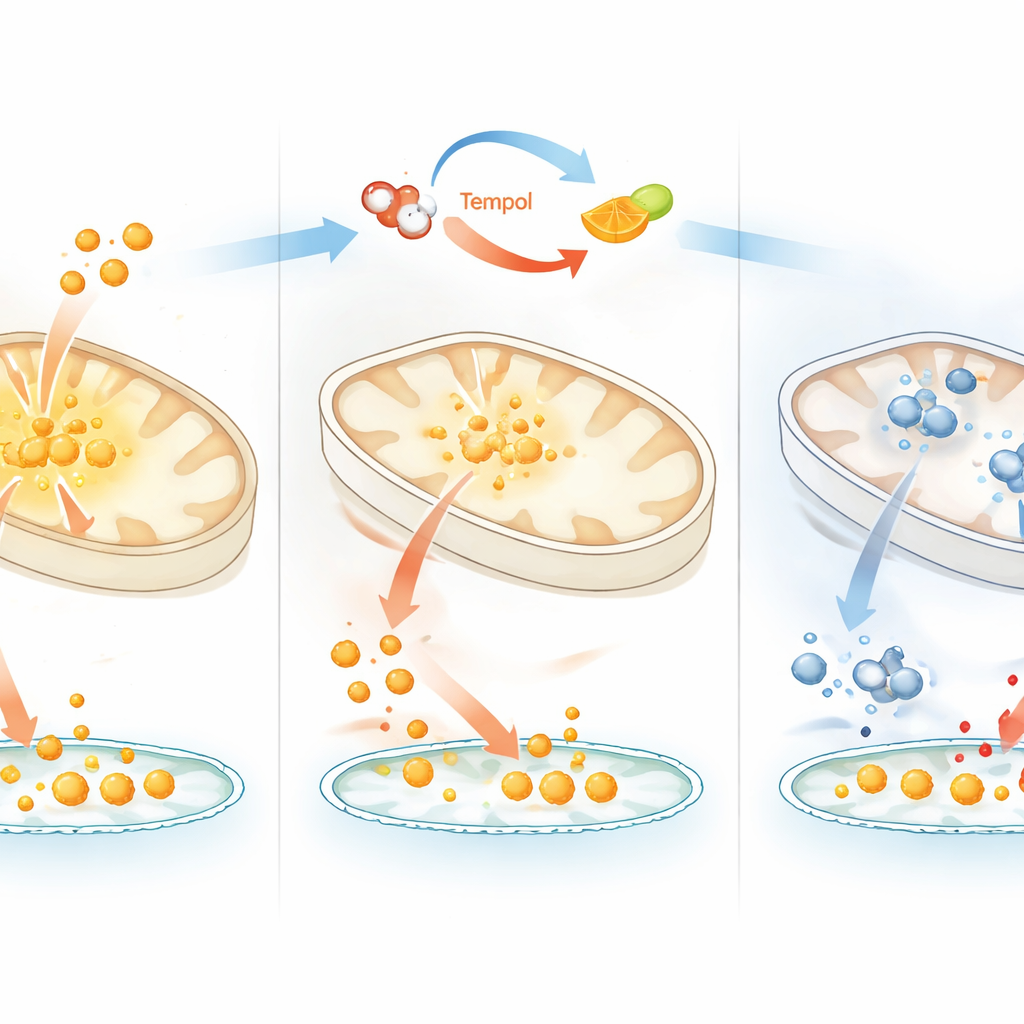
Die Forschenden konzentrierten sich auf Tempol, eine redoxaktive Verbindung, die zuvor hauptsächlich als Antioxidans und als direkter Schädiger von Eisen–Schwefel-Clustern angesehen wurde. Sie fanden heraus, dass Tempol sich eher wie ein „Anti‑Vitamin C“ verhält. In Zellkulturen verringerte Tempol den Pool nutzbaren Eisens und stabilisierte IRP2 – ein Kennzeichen von Eisenmangel. Anders als klassische eisenbindende Wirkstoffe ließen sich die Effekte von Tempol jedoch nicht vollständig allein durch Zugabe von zusätzlichem Eisen aufheben, und Tempol entzog den Mitochondrien nicht in gleicher Weise stark Eisen. Stattdessen wurde seine Wirkung nahezu vollständig durch Zugabe von Vitamin C rückgängig gemacht, was Zellwachstum, Eisenverwertung und eisen–schwefel‑cluster‑abhängige Enzyme wiederherstellte. Das deutet auf einen Mechanismus hin, bei dem Tempol die von Vitamin C getriebene Rückführung (Recycling) von Eisen in seinen aktiven Zustand stört und so Eisen in eine weniger reaktive Form verschiebt.
Selektiver Treffer für zentrale Zellprozesse
Tempol traf nicht alle Zelltypen gleichermaßen. In einer Reihe von Dutzenden menschlicher Krebszelllinien vertrugen einige Tempol gut, während bei anderen das Wachstum stark reduziert war. Empfindliche Zellen verloren die Aktivität mehrerer Eisen–Schwefel‑Cluster‑Enzyme, insbesondere eines mitochondrialen Enzyms namens ACO2, das zentral für den Energiestoffwechsel ist. Genetische Datensätze zeigten, dass Zelllinien, die stärker von ACO2 abhängig sind, auch anfälliger für Tempol waren. Das legt nahe, dass Zellen mit größerer Abhängigkeit von Eisen‑Schwefel‑Chemie weniger gut zurechtkommen, wenn das redoxchemische Gleichgewicht des Eisens gestört wird. Bemerkenswert ist, dass eine Absenkung des Sauerstoffgehalts – näher an dem, was viele Gewebe im Körper erleben – die Eisen–Schwefel‑Cluster und das Zellwachstum vor Tempol schützte, ohne die eisen‑sensible Antwort zu verhindern. Das deutet darauf hin, dass Sauerstoff selbst zu dem unter Standard‑Laborbedingungen beobachteten Schaden beiträgt.
Eisen, Zelltod und Krankheitsverknüpfungen
Über den Stoffwechsel hinaus bewirkte die redoxbasierte Eisenbegrenzung durch Tempol zwei auffällige Signalwirkungen. Erstens stabilisierte sie rasch HIF1α, ein Protein, das auf niedrigen Sauerstoff reagiert und dessen Abbau sowohl von Eisen als auch von Vitamin‑C‑abhängigen Enzymen abhängt. Zweitens unterdrückte Tempol konsistent die Ferroptose, eine Form des Zelltods, die durch eisenkatalysierte Schäden an Membranlipiden angetrieben wird. Beide Effekte traten bei Tempol‑Dosen auf, die nutzbares Eisen reduzierten, aber vor einem offensichtlichen Verlust von Eisen–Schwefel‑Clustern, was zeigt, dass schon mäßige Verschiebungen im chemischen Zustand des Eisens Stressantworten und Zellüberleben stark beeinflussen können. Die Autoren zeigten außerdem, dass ein ähnliches Verhalten nicht durch generelle Antioxidantien oder Reduktionsmittel reproduziert wurde, was die spezifische Vitamin‑C‑bezogene Chemie von Tempol unterstreicht.
Was das für zukünftige Therapien bedeutet
Kurz gesagt zeigt die Studie, dass Tempol als gezielter Störer der chemischen „Feineinstellung“ von Eisen in Zellen wirkt, hauptsächlich durch die Gegenspielung von Vitamin C. Das reduziert die Form von Eisen, die viele Enzyme benötigen, dämpft eisengetriebenen Zelltod und verlangsamt in bestimmten Zellen, die stark auf Eisen–Schwefel‑Cluster‑Enzyme wie ACO2 angewiesen sind, das Wachstum. Da Fehlsteuerungen des Eisens an Hirnerkrankungen, Infektionen und Krebs beteiligt sind, eröffnet das Verständnis und gegebenenfalls die Nutzung dieser redoxbasierten Eisenbegrenzung neue Strategien, die Eisen nicht einfach entfernen, sondern vielmehr die Art und Weise verändern, wie Zellen es nutzen können.
Zitation: Terzi, E.M., Fujihara, K.M., Molenaars, M. et al. Redox cycling nitroxide limits cellular iron availability and selectively inhibits iron-sulfur cluster metabolism. Cell Death Discov. 12, 165 (2026). https://doi.org/10.1038/s41420-026-03042-w
Schlüsselwörter: Eisenstoffwechsel, Tempol, Vitamin C, Eisen–Schwefel-Cluster, Ferroptose