Clear Sky Science · ar
التدوير التأكسدي للنيتروكسيد يحد من توافر الحديد داخل الخلايا ويثبِط انتقائياً أيض مجموعات الحديد-كبريت
لماذا يهم هذا للصحة اليومية
تعتمد خلايانا على الحديد ليس فقط لحمل الأكسجين في الدم، بل أيضاً لتشغيل إنتاج الطاقة وإصلاح الحمض النووي. ومع ذلك، فإن فائضاً من نوع خاطئ من الحديد يمكن أن يغذي تفاعلات كيميائية ضارة ويؤدي حتى إلى شكل من أشكال موت الخلايا. تستكشف هذه الدراسة كيف يغير جزيء صغير يُسمى تمبول، الذي خضع للاختبار سابقاً في نماذج مرضية متعددة، بشكل دقيق طريقة تعامل الخلايا مع الحديد. من خلال دفع الحديد إلى حالة أقل قابلية للاستخدام ومعارضة عمل فيتامين ج، يكشف تمبول عن طبقة من التحكم في استخدام الحديد كانت قليلة التقدير سابقاً وقد تكون ذات صلة بحالات تتراوح من التنكس العصبي إلى السرطان.
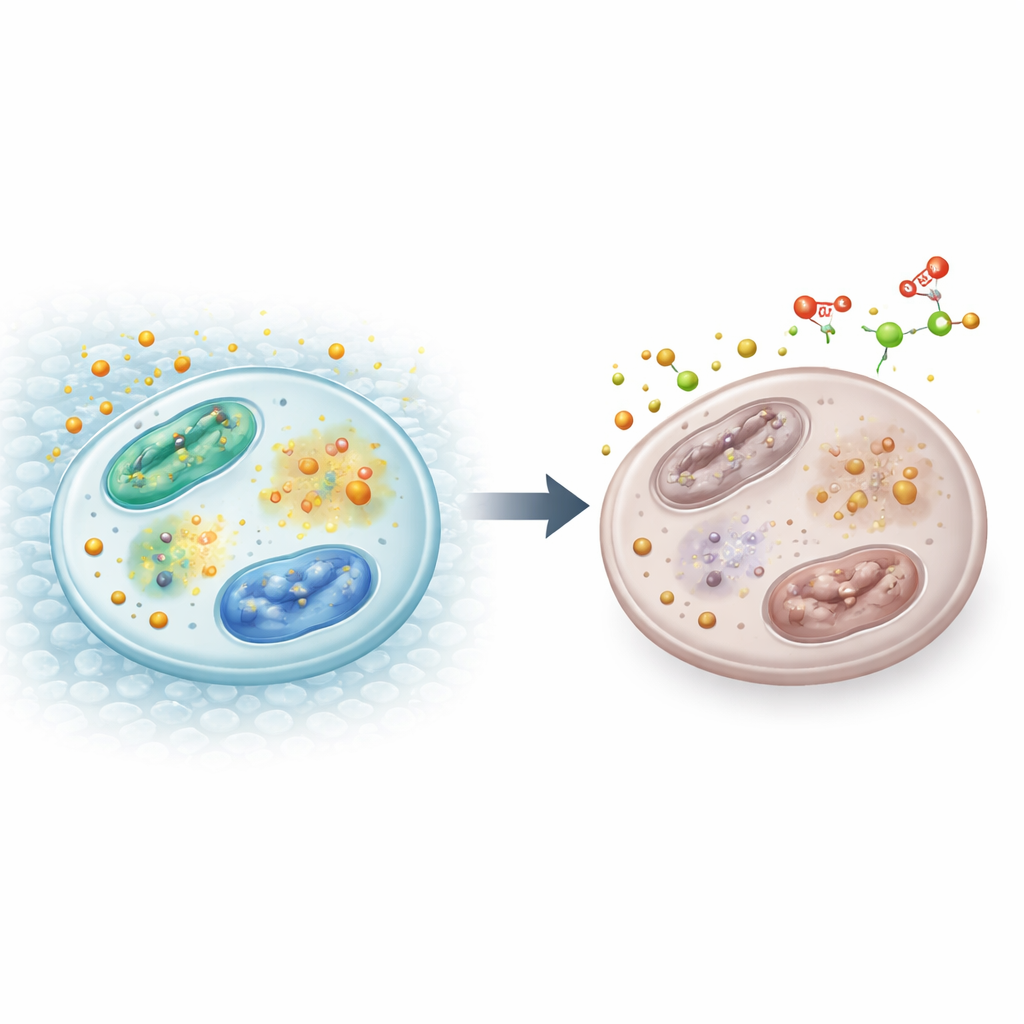
التوازن الدقيق للحديد
داخل الخلايا، يُستخدم الحديد إما كأيونات حرة أو يُبنى داخل هياكل خاصة تسمى مجموعات الحديد–كبريت التي تساعد العديد من الإنزيمات على أداء وظائفها في إنتاج الطاقة ونسخ الحمض النووي وغيرها من العمليات الحيوية. وبما أن الحديد يمكنه التبدل بسهولة بين حالات كيميائية مختلفة، فإنه مفيد لكنه قد يكون ضاراً أيضاً. لذا تعتمد الخلايا على شبكة من المستشعرات والمنظِّمات للحفاظ على مخزون صغير ومُدار بعناية من الحديد المتاح. مستقبلان بروتينيان، IRP1 وIRP2، يستشعران حالة الحديد ويعدّلان مقدار الحديد المستورد أو المخزن أو المُصدَّر. وفي الوقت نفسه، يساعد فيتامين ج على إبقاء الحديد في الحالة الكيميائية «المُختزلة» التي تحتاجها العديد من الإنزيمات للعمل بشكل صحيح.
طريقة مختلفة للحد من الحديد
ركز الباحثون على تمبول، مركب نشط في عمليات الأكسدة والاختزال كان يُعتقد سابقاً أنه يعمل أساساً كمضاد للأكسدة وأنه يتسبب مباشرة في تلف مجموعات الحديد–كبريت. وجدوا أن تمبول يتصرف بدلاً من ذلك بشكل أشبه بـ «مضاد لفيتامين ج». في مزارع الخلايا، خفّض تمبول حوض الحديد القابل للاستخدام وحفَظ IRP2، وهو علامة على نقص الحديد. ومع ذلك، وعلى عكس الأدوية التقليدية المربوطة بالحديد، لم تُعكس تأثيرات تمبول تماماً بمجرد إضافة كمية إضافية من الحديد، ولم يقم تمبول بنزع الحديد بقوة من المتقدرات بالطريقة نفسها. بدلاً من ذلك، تم إلغاء تأثيره تقريباً تماماً بإضافة فيتامين ج، الذي استعاد نمو الخلايا واستخدام الحديد وإنزيمات المعتمدة على مجموعات الحديد–كبريت. هذا يشير إلى آلية يتداخل فيها تمبول مع إعادة تدوير الحديد إلى حالته النشطة المدعومة بفيتامين ج، محوَّلاً الحديد إلى شكل أقل تفاعلية.
ضربة انتقائية لعمليات خلوية رئيسية
لم يؤثر تمبول على جميع أنواع الخلايا بالتساوي. في لوحة تضم عشرات خطوط خلايا سرطان بشرية، تحملت بعض الخلايا تمبول جيداً، في حين أظهرت خلايا أخرى انخفاضاً حاداً في النمو. فقدت الخلايا الحساسة نشاط عدة إنزيمات معتمدة على مجموعات الحديد–كبريت، خاصة إنزيم متقدري يُدعى ACO2 يلعب دوراً مركزياً في استقلاب الطاقة. كشفت مجموعات البيانات الجينية أن خطوط الخلايا الأكثر اعتماداً على ACO2 كانت أيضاً أكثر عرضة لتأثير تمبول، مما يوحي بأن الخلايا التي تعتمد بشكل أكبر على كيمياء الحديد–كبريت أقل قدرة على التكيّف عندما يتعطل توازن تأكسد الحديد. ومن اللافت أن خفض مستويات الأكسجين، بما يقترب من الظروف التي تُختبر فيها العديد من الأنسجة داخل الجسم، حمى مجموعات الحديد–كبريت ونمو الخلايا من تأثير تمبول دون أن يمنع استجابة استشعار الحديد، مشيراً إلى أن الأكسجين نفسه يساهم في الضرر الذي يُرى في ظروف المختبر القياسية.
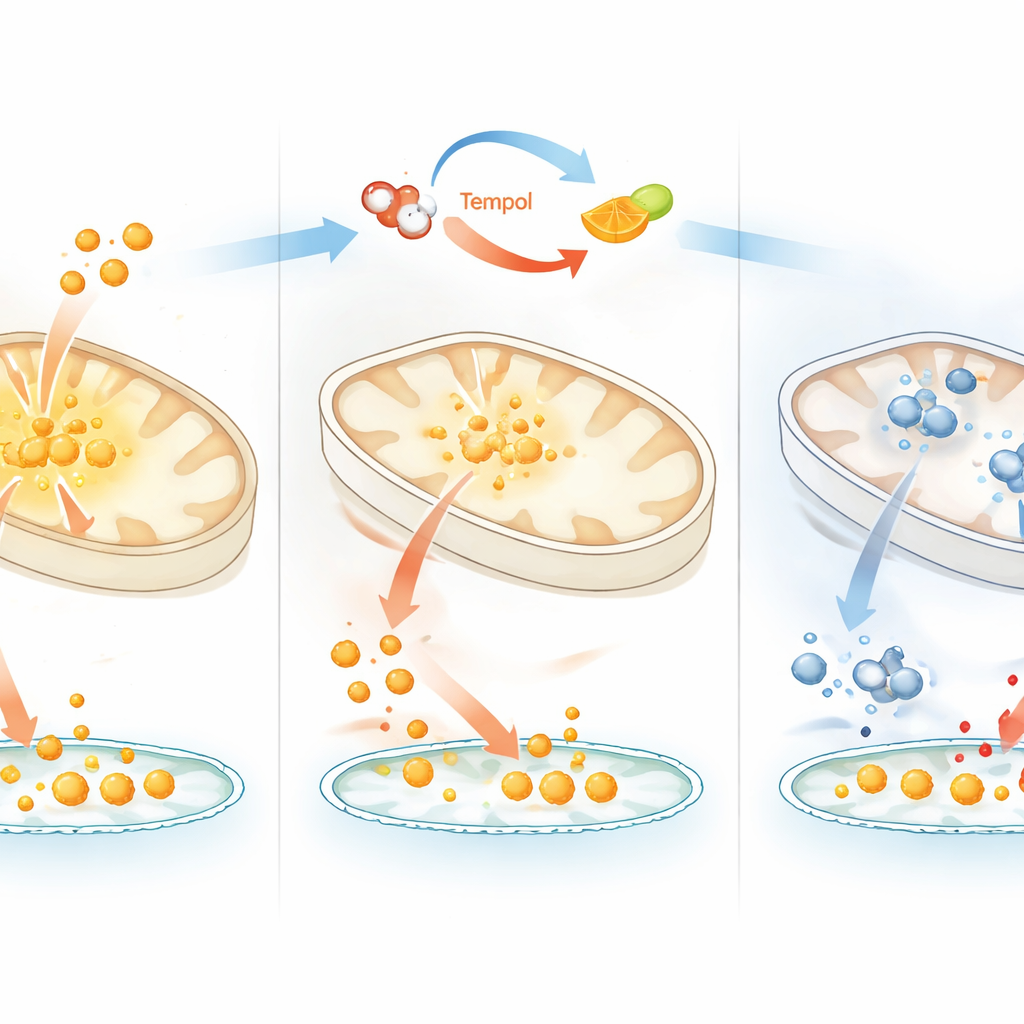
الحديد وموت الخلايا وصلات بالأمراض
بعيداً عن الأيض، كان لحد تمبول القائم على الأكسدة والاختزال للحديد تأثيران إشاريان بارزان. أولاً، عمل بسرعة على تثبيت HIF1α، وهو بروتين يستجيب لانخفاض الأكسجين ويعتمد على كل من الحديد والإنزيمات المدعومة بفيتامين ج ليتم تحلله. ثانياً، قمع باستمرار النخر الخاطف (الفروبتوسيس)، وهو نوع من موت الخلايا يقوده تلف الدهون الغشائية المحفز بواسطة الحديد. ظهرت كلتا الظاهرتين عند جرعات من تمبول خفّضت الحديد القابل للاستخدام لكنها سبقت فقدان واضح لمجموعات الحديد–كبريت، مما يدل على أن تحولات متواضعة في الحالة الكيميائية للحديد يمكن أن تؤثر بقوة على استجابات الإجهاد وبقاء الخلايا. كما أظهر المؤلفون أن سلوكاً مشابهاً لم يتكرر بواسطة مضادات الأكسدة العامة أو عوامل الاختزال، مما يؤكد الكيمياء الخاصة المرتبطة بفيتامين ج لدى تمبول.
ماذا يعني هذا للعلاجات المستقبلية
بعبارات بسيطة، تُظهر الدراسة أن تمبول يعمل كمشوِش مستهدف على الطريقة التي «يضبط» بها الخلايا الحديد كيميائياً، إلى حد كبير من خلال معارضة فيتامين ج. هذا يقلل الشكل الذي يحتاجه العديد من الإنزيمات، يخمد موت الخلايا المدفوع بالحديد، وفي خلايا معينة تعتمد بشدة على إنزيمات مجموعات الحديد–كبريت مثل ACO2، يبطئ النمو. ونظراً لأن سوء إدارة الحديد مرتبط باضطرابات الدماغ والعدوى والسرطان، فإن فهم هذا الحد القائم على التأكسد والاختزال للحديد واستغلاله قد يفتح الباب لاستراتيجيات جديدة لا تكتفي بإزالة الحديد فحسب، بل تغيّر طريقة استخدام الخلايا له.
الاستشهاد: Terzi, E.M., Fujihara, K.M., Molenaars, M. et al. Redox cycling nitroxide limits cellular iron availability and selectively inhibits iron-sulfur cluster metabolism. Cell Death Discov. 12, 165 (2026). https://doi.org/10.1038/s41420-026-03042-w
الكلمات المفتاحية: أيض الحديد, تمبول, فيتامين ج, مجموعات الحديد–كبريت, النخر الخاطف (فروبتوسيس)