Clear Sky Science · pl
Redoks cykling nitroksydu ogranicza dostępność żelaza w komórkach i selektywnie hamuje metabolizm klastrów żelazo-siarka
Dlaczego to ma znaczenie dla zdrowia codziennego
Nasze komórki potrzebują żelaza nie tylko do przenoszenia tlenu we krwi, ale także do napędzania produkcji energii i naprawy DNA. Jednak nadmiar nieodpowiedniej formy żelaza może napędzać szkodliwe reakcje chemiczne, a nawet wywołać specyficzny rodzaj śmierci komórkowej. W tym badaniu zbadano, jak mała cząsteczka o nazwie Tempol, już testowana w modelach chorobowych, subtelnie zmienia sposób, w jaki komórki gospodarują żelazem. Poprzez przesunięcie żelaza w mniej użyteczny stan i przeciwstawianie się działaniu witaminy C, Tempol ujawnia wcześniej niedoceniany poziom kontroli nad użyciem żelaza, który może być istotny w schorzeniach od neurodegeneracji po raka.
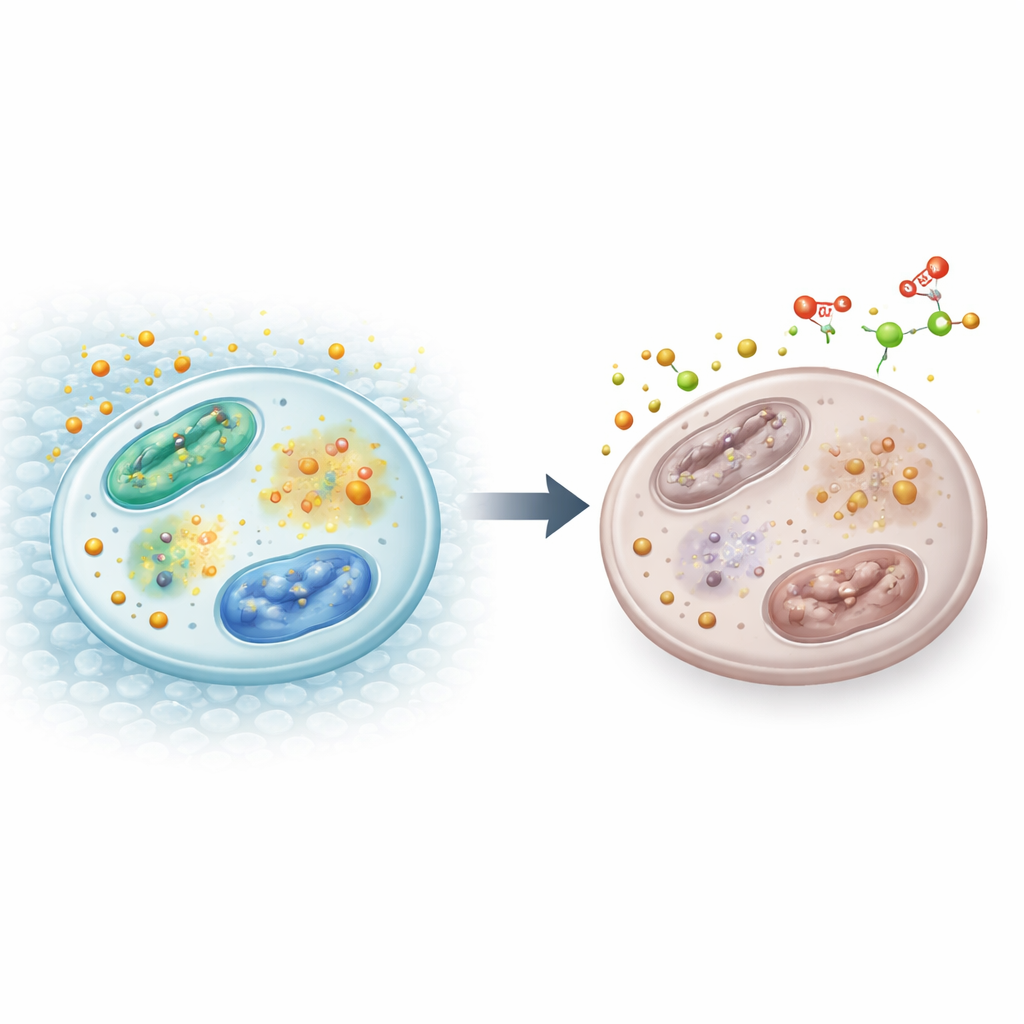
Delikatna równowaga żelaza
W komórkach żelazo występuje albo jako jony swobodne, albo wbudowane w specjalne struktury zwane klastrami żelazo–siarka, które pomagają wielu enzymom w procesach produkcji energii, kopiowania DNA i innych niezbędnych funkcjach. Ponieważ żelazo łatwo przechodzi między stanami chemicznymi, jest zarówno użyteczne, jak i potencjalnie szkodliwe. Komórki polegają więc na sieci czujników i regulatorów, aby utrzymywać małą, starannie zarządzaną pulę dostępnego żelaza. Dwa białka, IRP1 i IRP2, wykrywają stan żelaza i regulują, ile żelaza jest importowane, magazynowane lub eksportowane. Równocześnie witamina C pomaga utrzymywać żelazo w chemicznie «zredukowanej» formie, której wiele enzymów potrzebuje, by działać prawidłowo.
Inny sposób ograniczania żelaza
Naukowcy skupili się na Tempolu, związku aktywnym redoksowo, wcześniej uważanym głównie za przeciwutleniacz i za bezpośrednio uszkadzający klastry żelazo–siarka. Odkryli, że Tempol zachowuje się raczej jak «antywitamina C». W hodowlach komórkowych Tempol obniżał pulę użytecznego żelaza i stabilizował IRP2, co jest oznaką niedoboru żelaza. Jednak w przeciwieństwie do klasycznych leków wiążących żelazo, skutki Tempolu nie mogły być w pełni odwrócone przez dodanie dodatkowego żelaza, a Tempol nie odprowadzał żelaza z mitochondriów w ten sam sposób. Zamiast tego jego wpływ był niemal całkowicie znoszony przez dodanie witaminy C, która przywracała wzrost komórek, wykorzystanie żelaza i aktywność enzymów zależnych od klastrów żelazo–siarka. Wskazuje to na mechanizm, w którym Tempol zakłóca napędzaną przez witaminę C recyklingową przemianę żelaza do formy aktywnej, przesuwając jego równowagę w stronę mniej reaktywnej formy.
Selektywny cios w kluczowe procesy komórkowe
Tempol nie wpływał jednak równo na wszystkie typy komórek. W panelu kilkudziesięciu ludzkich linii komórkowych nowotworowych niektóre dobrze tolerowały Tempol, podczas gdy inne wykazywały wyraźne zahamowanie wzrostu. Komórki wrażliwe traciły aktywność wielu enzymów zależnych od klastrów żelazo–siarka, zwłaszcza mitochondrialnego enzymu ACO2, który jest kluczowy dla metabolizmu energetycznego. Zestawy danych genetycznych wykazały, że linie komórkowe bardziej zależne od ACO2 były też bardziej podatne na Tempol, sugerując, że komórki silniej polegające na chemii klastrów żelazo–siarka gorzej znoszą zaburzenie równowagi redoks żelaza. Co istotne, obniżenie poziomu tlenu, bliższe warunkom panującym w tkankach organizmu, chroniło klastry żelazo–siarka i wzrost komórek przed działaniem Tempolu, nie zapobiegając jednocześnie odpowiedzi czujników żelaza, co wskazuje, że sam tlen przyczynia się do uszkodzeń obserwowanych w standardowych warunkach laboratoryjnych.
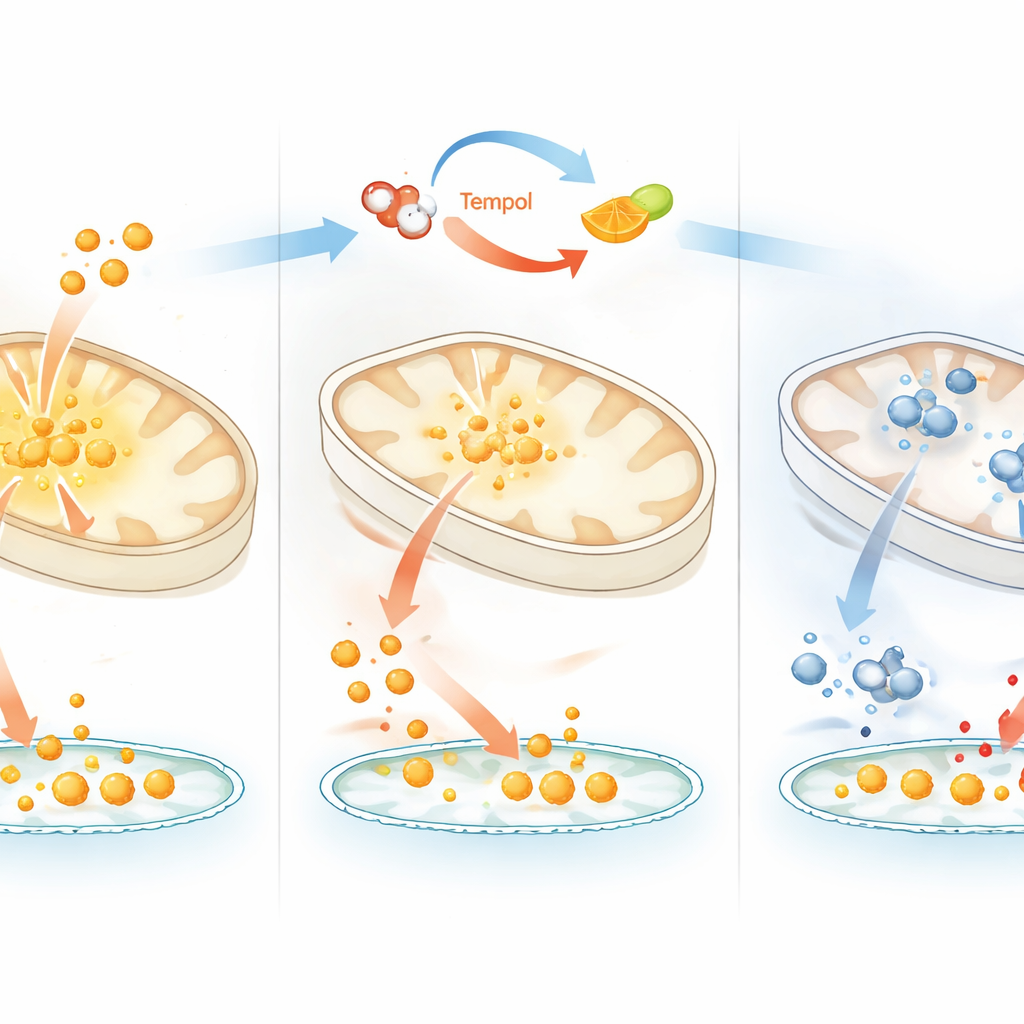
Żelazo, śmierć komórek i związki z chorobami
Ponad aspektem metabolicznym, redoksowe ograniczanie żelaza przez Tempol wywołało dwa uderzające efekty sygnalizacyjne. Po pierwsze, szybko stabilizował HIF1α, białko reagujące na niski poziom tlenu, którego degradacja zależy od enzymów wymagających zarówno żelaza, jak i wsparcia witaminy C. Po drugie, konsekwentnie tłumił ferroptozę, rodzaj śmierci komórkowej napędzanej przez żelazo-katalizowane uszkodzenie lipidów błonowych. Oba efekty pojawiały się przy dawkach Tempolu, które zmniejszały ilość użytecznego żelaza, ale przed oczywistą utratą klastrów żelazo–siarka, co wskazuje, że umiarkowane przesunięcia chemicznego stanu żelaza mogą silnie wpływać na reakcje na stres i przeżycie komórek. Autorzy wykazali również, że podobne zachowanie nie występowało przy zastosowaniu ogólnych przeciwutleniaczy czy czynników redukujących, podkreślając specyficzną chemię Tempolu związaną z witaminą C.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, badanie pokazuje, że Tempol działa jako celowy zakłócacz sposobu, w jaki komórki chemicznie «stroją» żelazo, w dużej mierze przez przeciwstawianie się witaminie C. Zmniejsza to formę żelaza potrzebną wielu enzymom, tłumi żelazo-zależne śmierci komórkowe i w pewnych komórkach silnie zależnych od enzymów klastrów żelazo–siarka, takich jak ACO2, spowalnia wzrost. Ponieważ zaburzenia gospodarki żelazem wiążą się z chorobami mózgu, zakażeniami i rakiem, zrozumienie i potencjalne wykorzystanie tego redoksowego ograniczania żelaza otwiera drogę do nowych strategii, które nie polegają jedynie na usuwaniu żelaza, lecz zmieniają sposób, w jaki komórki mogą je wykorzystywać.
Cytowanie: Terzi, E.M., Fujihara, K.M., Molenaars, M. et al. Redox cycling nitroxide limits cellular iron availability and selectively inhibits iron-sulfur cluster metabolism. Cell Death Discov. 12, 165 (2026). https://doi.org/10.1038/s41420-026-03042-w
Słowa kluczowe: metabolizm żelaza, Tempol, witamina C, klastry żelazo–siarka, ferroptoza