Clear Sky Science · ja
レドックス循環性ニトロキシドは細胞内の鉄利用性を制限し、鉄硫黄クラスター代謝を選択的に阻害する
日常の健康にとってなぜ重要か
細胞は血中で酸素を運ぶだけでなく、エネルギー産生やDNA修復を駆動するためにも鉄に依存しています。しかし、不適切な形の鉄が過剰になると有害な化学反応を引き起こし、ある種の細胞死を誘発することさえあります。本研究は、いくつかの疾病モデルで既に検証されている小分子テンポルが、細胞の鉄処理をどのように微妙に変化させるかを探ります。テンポルは鉄を利用しにくい形に傾け、ビタミンCの作用に拮抗することで、鉄の利用を制御するこれまで十分に評価されてこなかった層を明らかにし、これは神経変性からがんまでさまざまな状態に関係し得ます。
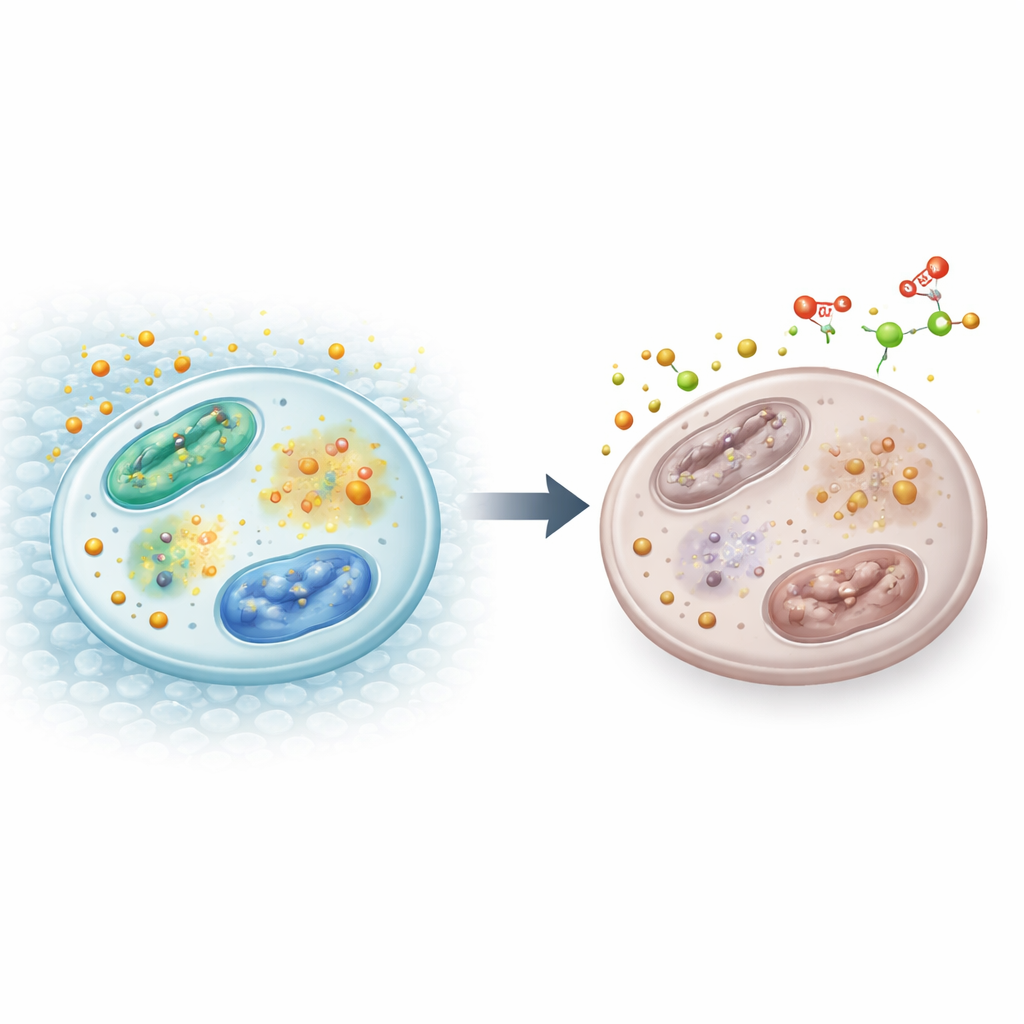
鉄の繊細なバランス
細胞内では、鉄は遊離イオンとして使われるか、あるいは鉄–硫黄クラスターと呼ばれる特殊な構造に組み込まれ、多くの酵素がエネルギー産生やDNA複製などの重要な働きをするのを助けます。鉄は化学状態を容易に変えられるため、有用である一方で潜在的に有害でもあります。したがって細胞は、利用可能な鉄を小さく厳密に管理されたプールとして維持するために、センサーや調節因子のネットワークに依存しています。IRP1とIRP2という二つのタンパク質は鉄状態を感知し、鉄の取り込み、貯蔵、排出量を調節します。同時に、ビタミンCは多くの酵素が正しく機能するために必要とする化学的に「還元された」形の鉄を維持するのに寄与します。
鉄を制限する別の方法
研究者らは、これまで主に抗酸化剤として、あるいは鉄–硫黄クラスターを直接損傷するものとして考えられてきたレドックス活性化合物テンポルに注目しました。彼らはテンポルがむしろ「抗ビタミンC」のように振る舞うことを見出しました。細胞培養では、テンポルは利用可能な鉄のプールを低下させ、IRP2を安定化させました。これは鉄不足の特徴です。ただし、古典的な鉄捕捉薬とは異なり、テンポルの効果は単に鉄を追加するだけでは完全には回復せず、ミトコンドリアから鉄を強く奪うという形でもありませんでした。代わりに、その影響はほぼ完全にビタミンCの添加で打ち消され、細胞増殖、鉄利用、および鉄–硫黄クラスター依存の酵素活性が回復しました。これはテンポルがビタミンC駆動の鉄の還元的リサイクルに干渉し、鉄をより反応性の低い形へと偏らせるメカニズムを示唆します。
重要な細胞プロセスへの選択的な打撃
テンポルの影響はすべての細胞種で均一ではありませんでした。数十種類のヒトがん細胞株のパネルでは、テンポルをよく耐える株もあれば、増殖が大きく低下する株もありました。感受性の高い細胞では複数の鉄–硫黄クラスター酵素の活性が失われ、特にエネルギー代謝の中心的なミトコンドリア酵素であるACO2の活性低下が目立ちました。遺伝子データセットはACO2により依存する細胞株がテンポルに対して脆弱であることを示し、鉄–硫黄化学に強く依存する細胞ほど鉄のレドックスバランスが乱れると対処しにくいことを示唆します。注目すべきは、体内の多くの組織が経験するより低い酸素レベルに近づけると、鉄–硫黄クラスターと細胞増殖はテンポルから保護される一方で鉄感知応答は妨げられず、標準的な培養条件下で観察される損傷に酸素自体が寄与していることを示した点です。
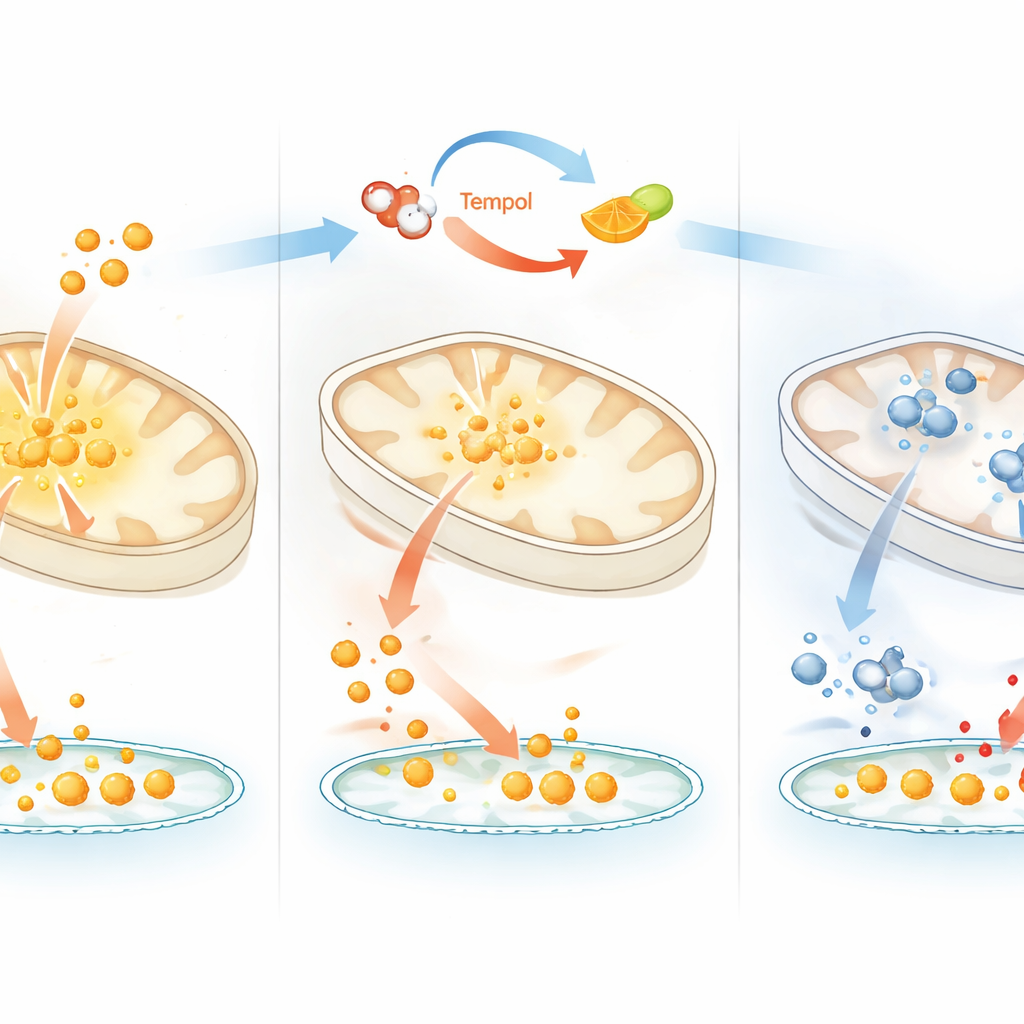
鉄、細胞死、および疾患との関連
代謝以外にも、テンポルのレドックスに基づく鉄制限は二つの顕著なシグナル効果を生みました。第一に、テンポルは迅速にHIF1αを安定化させました。HIF1αは低酸素に応答するタンパク質で、分解には鉄とビタミンCを支持する酵素が必要です。第二に、テンポルは一貫してフェロトーシスを抑制しました。フェロトーシスは膜脂質に対する鉄触媒性の損傷で駆動される一種の細胞死です。どちらの効果も、利用可能な鉄が減少する濃度で現れ、明白な鉄–硫黄クラスターの喪失が起こる前に観察され、鉄の化学状態のわずかなシフトがストレス応答や細胞生存に強く影響することを示しています。著者らは同様の挙動が汎用の抗酸化剤や還元剤では再現されないことも示し、テンポルのビタミンC関連化学の特異性を強調しました。
将来の治療への意味
平たく言えば、本研究はテンポルが主にビタミンCに拮抗することで、細胞が鉄を化学的に「調律」する仕組みを標的的に攪乱することを示しています。これにより多くの酵素が必要とする鉄の形が減少し、鉄駆動の細胞死が抑えられ、ACO2のような鉄–硫黄クラスター酵素に大きく依存する特定の細胞では増殖が遅くなります。鉄の誤管理は脳疾患、感染症、がんに関与しているため、このレドックスベースの鉄制限を理解し利用することは、単に鉄を除去するのではなく、細胞がそれをどう使えるかを変える新たな戦略への道を開きます。
引用: Terzi, E.M., Fujihara, K.M., Molenaars, M. et al. Redox cycling nitroxide limits cellular iron availability and selectively inhibits iron-sulfur cluster metabolism. Cell Death Discov. 12, 165 (2026). https://doi.org/10.1038/s41420-026-03042-w
キーワード: 鉄代謝, テンポル, ビタミンC, 鉄–硫黄クラスター, フェロトーシス