Clear Sky Science · tr
DNA metiltransferaz inhibitasyonu, VHL eksikliğine sahip böbrek hücreli karsinom hücrelerinde terapötik bir zayıflıktır
Bu böbrek kanseri çalışması neden önemli
Böbrek kanseri sıklıkla geç evrede tespit edilir ve standart tedavilere karşı dirençli olabilir. Bu çalışma, böbrek tümörlerinin yaygın bir alt türünde gizli bir zayıflığı ortaya koyuyor: koruyucu bir gen olan VHL kaybolduğunda, kanser hücreleri diğer genleri susturan kimyasal bir sürece olağanüstü derecede bağımlı hale geliyor. Araştırmacılar bu susturma mekanizmasını mevcut ilaçlarla engelleyerek VHL‑eksik tümör hücrelerini diğer hücreleri koruyarak öldürebildiler; bu da hastalar için daha kişiselleştirilmiş yeni bir tedavi yoluna işaret ediyor.
Böbrek tümörlerinde yaygın bir kusur
Temiz hücreli tipteki çoğu böbrek kanseri, normalde hücrelerin oksijeni algılamasına ve damar büyümesi ile metabolizmayı kontrol altında tutmasına yardımcı olan VHL geninde hasar taşır. VHL eksik olduğunda hücreler, HIF‑2α adında bir faktör tarafından yönlendirilen kronik bir "düşük oksijen" moduna geçer. Daha önceki çalışmalar bu tür tümörlerin ayrıca özellikle gen açma bölgelerinin yakınında DNA üzerinde metil grubu adı verilen ekstra kimyasal işaretler taşıdığını göstermişti. Bu işaretler, normalde kanser büyümesini sınırlayan genleri kapatabilir. Yeni çalışma basit bir soruyu sordu: VHL‑eksik tümörler bu anormal DNA etiketlemeye dayanıyorsa, bu bağımlılık onların Achilles topuğu haline getirilebilir mi?
Zayıf noktayı hedef alan ilaçların bulunması
Çalışma, genetik olarak özdeş fakat VHL açısından farklı çiftler halinde böbrek kanseri hücre hatları kullandı: bir partner VHL’den yoksun, diğeri ise VHL geri kazandırılmıştı. Bu hücreleri DNA’nın nasıl paketlendiğini ve işaretlendiğini kontrol eden çeşitli "epigenetik" düzenleyicilere yönelik 128 küçük molekülden oluşan bir kütüphaneye maruz bıraktılar. Her bileşiğin hücre çoğalmasını ne kadar yavaşlattığını karşılaştırarak VHL‑eksik hücreler üzerinde özellikle toksik olan ajanları aradılar; bu strateji sentetik letalite olarak bilinir. Birkaç aday öne çıktı, fakat DNA’ya metil etiketleri ekleyen enzimleri—DNA metiltransferazları—engelleyen ilaçlar, onaylı ilaçlar decitabine ve azacitidine ile iki deneysel bileşiği de içerecek şekilde öne çıktı. Birden fazla böbrek kanseri hattında ve VHL devre dışı bırakılmış akciğer ve karaciğer kanseri modellerinde bu ilaçlar tercihli olarak VHL‑eksik hücreleri öldürdü.
DNA etiketlemenin VHL kaybını hücre ölümüyle nasıl bağladığı
Daha derine inen araştırmacılar, VHL‑eksik hücrelerin bu ilaçlara neden bu kadar hassas olduğunu keşfettiler. VHL kaybı, sürekli HIF‑2α aktivasyonuna yol açar; bu da hücre bölünmesi sırasında metil işaretlerini koruyan başlıca DNA‑etiketleme enzimi olan DNMT1 düzeylerini artırır. Hasta tümör verileri DNMT1’in normal böbrek dokusuna göre böbrek kanserlerinde daha bol olduğunu ve HIF‑2α ile paralel olarak arttığını doğruladı. Bu yükselmiş DNMT1 yaygın DNA hipermetilasyonuna katkıda bulunur. Araştırmacılar DNMT1, DNMT3A veya DNMT3B’yi genetik araçlarla tek tek azalttıklarında, VHL‑eksik hücreler kısmen ilaç etkisini taklit eden şekilde ölmeye başladı ve böylece DNA metilasyonunun kendisinin—sadece ilacın hedef dışı etkilerinin değil—anahtar olduğunu doğruladılar. VHL‑eksik böbrek tümörleri taşınmış farelerde decitabine ile tedavi tümör büyümesini belirgin şekilde yavaşlattı; belirgin kilo kaybı veya toksisite gözlenmedi, bu da bu zayıflığın canlı organizmalarda da geçerli olduğunu destekliyor.
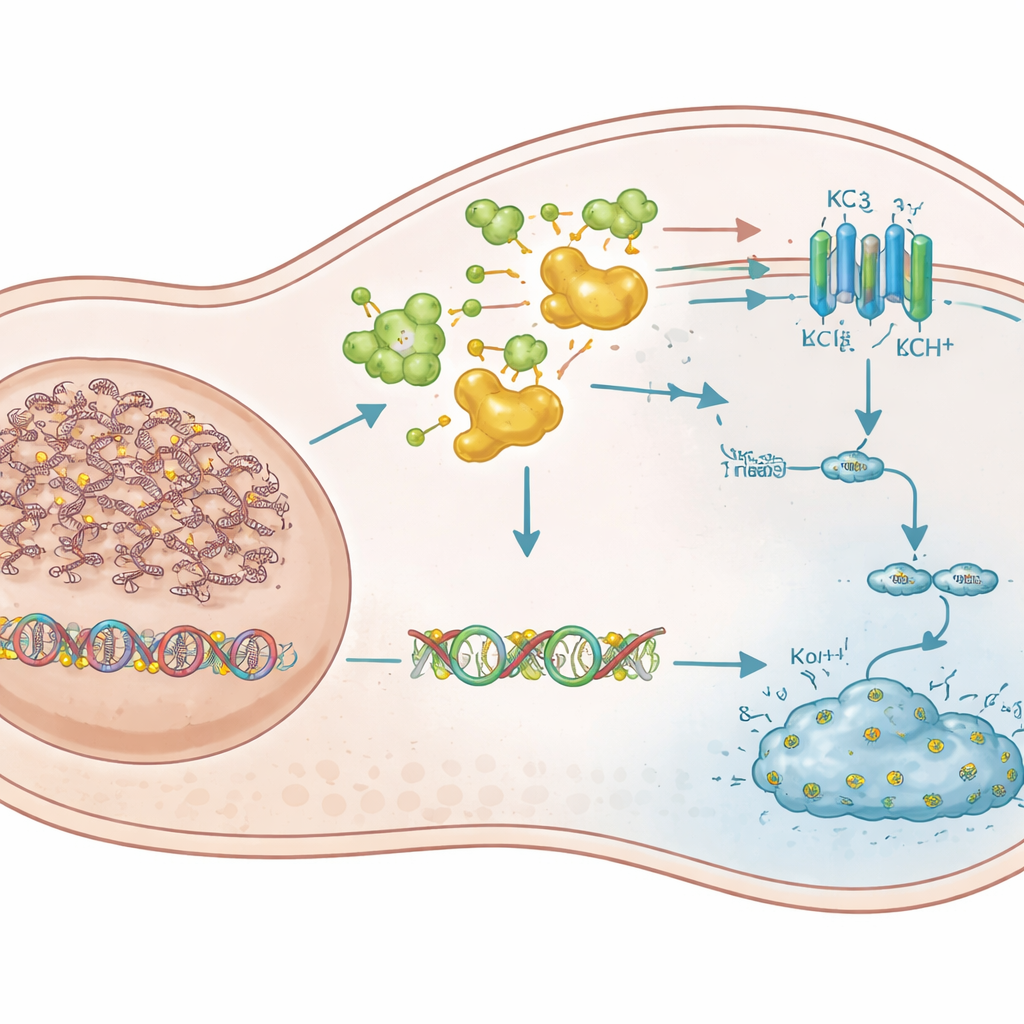
Susturulmuş bir bekçi gen geri dönüyor
Hangi metilasyonla susturulmuş genlerin en önemli olduğunu belirlemek için yazarlar, decitabine tedavisinden önce ve sonra VHL‑eksik ve VHL‑geri kazandırılmış hücrelerde gen aktivitesini karşılaştırdı. Susturulmuş fakat ilacın etkisiyle yeniden uyanan tümör baskılayıcı olarak bilinen veya şüphelenilen genlere odaklandılar. 14 güçlü aday arasından KCNK3 isimli bir gen kritik oyuncu olarak öne çıktı. KCNK3 bir potasyum kanalı—potasyum iyonlarının akışını kontrol eden hücre zarı üzerindeki küçük bir gözenek—kodlar. VHL‑eksik böbrek kanseri hücrelerinde KCNK3’ün başlangıç bölgesi yoğun bir şekilde metillenmişti ve aktivitesi neredeyse yoktu. DNMT‑engelleyici ilaçlar bu metil işaretlerini kaldırdı, KCNK3 düzeylerini geri getirdi ve güçlü büyüme inhibisyonu ile hücre ölümünü tetikledi. KCNK3 deneysel olarak tekrar aktifleştirildiğinde hücreler bölünmeyi durdurdu; KCNK3 bastırıldığında decitabine’in öldürücü etkisi hem kültürde hem de fare tümörlerinde büyük ölçüde ortadan kalktı. Hasta veri setleri ayrıca KCNK3’ün böbrek tümörlerinde normal böbreğe göre daha fazla metillendiğini ve daha yüksek metilasyonun daha kötü sağkalım tahmin ettiğini gösterdi.
Hücreleri kendi kendini yok etmeye iten sinyal yolları
KCNK3’ü geri getirmek sadece bir iyon kanalını yeniden açmaktan daha fazlasını yaptı. Decitabine tedavisi altında KCNK3 ile ve KCNK3 olmadan hücrelerin RNA dizilemesi, KCNK3 yeniden aktivasyonunun besin stresi, tümör nekroz faktörü‑alfa (TNF‑α) ve MAPK yolları olarak bilinen kilit stres‑yanıt yollarıyla ilişkili sinyalleri artırdığını ortaya koydu. Bunlar da hücresel intihar mekanizmasına beslenir. Normal KCNK3’e sahip hücrelerde decitabine TNF‑α düzeylerini yükseltti, aşağı akım sinyallemeyi aktive etti, hayatta kalma proteini BCL‑2’yi azalttı ve kırılmış kaspaz‑3 ve PARP kesilmesi gibi efektör proteinleri artırdı. KCNK3 azaltıldığında bu değişiklikler sönümlendi ve hücreler apoptoza karşı dirençli oldu. Ortaya çıkan tablo şu: VHL‑eksik hücrelerde DNMT kaynaklı metilasyon KCNK3’ü kapatır ve ölüm sinyallerini zayıflatır; DNMT inhibitörleri bu frenleri kaldırır, KCNK3’ü yeniden uyandırır ve hücreleri TNF‑α ve MAPK‑yönlendirmeli bir kendi kendini yok etme yoluna iter.
Bu hastalar için ne anlama gelebilir
Bir arada değerlendirildiğinde çalışma, DNA metiltransferaz inhibitörlerinin VHL‑eksik böbrek tümörlerinin belirli bir bağlantısını sömürdüğünü öne sürüyor: VHL kaybı HIF‑2α’yı yükseltir, bu da DNMT1’i artırır ve sonuçta KCNK3 gibi koruyucu genleri susturur. Bu susturmayı ilaçlarla geri almak, güçlü ölüm yollarını yeniden aktifleştirerek bozulmuş hücreleri seçici şekilde öldürür. Decitabine ve azacitidine zaten kan kanserlerinde kullanıldığından, bu keşif VHL mutasyonu ve yüksek KCNK3 metilasyonu taşıyan böbrek tümörlerine sahip hastalar için bu ilaçların veya benzer ajanların yeniden değerlendirilmesi olasılığını gündeme getiriyor. Daha fazla klinik testle VHL durumu ve KCNK3 metilasyonunun ölçülmesi, bireyleri bu yerleşik zayıflıktan yararlanan epigenetik terapilere eşlemede yardımcı olabilir.
Atıf: Pu, Y., Wang, Z., Tao, S. et al. DNA methyltransferase inhibition is a therapeutic vulnerability in VHL-deficient renal cell carcinoma cells. Exp Mol Med 58, 798–812 (2026). https://doi.org/10.1038/s12276-026-01663-w
Anahtar kelimeler: böbrek hücreli karsinom, VHL mutasyonu, DNA metilasyonu, DNMT inhibitörleri, KCNK3