Clear Sky Science · de
Hemmung von DNA‑Methyltransferasen ist eine therapeutische Verwundbarkeit in VHL‑defizienten Nierenzellkarzinom‑Zellen
Warum diese Nierenkrebs‑Studie wichtig ist
Nierenkrebs wird oft spät entdeckt und kann gegenüber Standardbehandlungen hartnäckig resistent sein. Diese Studie deckt eine verborgene Schwachstelle in einem häufigen Subtyp von Nierentumoren auf: Geht ein wichtiges Schutzgen namens VHL verloren, werden die Krebszellen ungewöhnlich abhängig von einem chemischen Prozess, der andere Gene stummschaltet. Durch das Blockieren dieser Stummschalt‑Maschinerie mit bereits verfügbaren Wirkstoffen konnten die Forscher VHL‑defiziente Tumorzellen gezielt abtöten, während andere Zellen verschont blieben. Das weist auf einen neuen, gezielteren Behandlungsansatz für Patienten hin.
Ein häufiger Defekt in Nierentumoren
Die meisten klarzelligen Nierenkarzinome tragen Schäden im VHL‑Gen, das normalerweise Zellen dabei hilft, Sauerstoff wahrzunehmen und das Wachstum von Blutgefäßen sowie den Stoffwechsel zu kontrollieren. Fehlt VHL, schalten die Zellen in einen chronischen "Niedrig‑Sauerstoff"‑Zustand um, angetrieben von einem Faktor namens HIF‑2α. Frühere Arbeiten zeigten, dass solche Tumoren außerdem vermehrt chemische Markierungen, sogenannte Methylgruppen, auf ihrer DNA tragen, besonders in der Nähe von Gen‑Einschaltern. Diese Markierungen können Gene ausschalten, die normalerweise das Krebswachstum bremsen. Die neue Studie stellte eine einfache Frage: Wenn VHL‑defiziente Tumoren auf diese abnorme DNA‑Markierung angewiesen sind, lässt sich diese Abhängigkeit zur Achillesferse machen?
Wirkstoffe finden, die die Schwachstelle treffen
Das Team verwendete Paare von Nierenkrebs‑Zelllinien, die genetisch identisch waren bis auf VHL: Ein Partner hatte kein VHL, beim anderen war es wiederhergestellt. Diese Zellen setzten sie einer Bibliothek von 128 kleinen Molekülen aus, die verschiedene epigenetische Regulatoren anvisieren – Proteine, die steuern, wie DNA verpackt und markiert wird. Durch den Vergleich, wie stark jede Verbindung das Zellwachstum bremste, suchten sie nach Wirkstoffen, die besonders toxisch für VHL‑defiziente Zellen sind, eine Strategie, die als synthetische Letalität bekannt ist. Mehrere Kandidaten zeigten sich, doch besonders auffällig waren Substanzen, die DNA‑Methyltransferasen blockieren – Enzyme, die Methylgruppen an DNA anfügen –, darunter die zugelassenen Medikamente Decitabin und Azacitidin sowie zwei experimentelle Verbindungen. Über verschiedene Nierenkrebs‑Linien hinweg und sogar in Lungen‑ und Leberkrebsmodellen mit deaktiviertem VHL töteten diese Wirkstoffe bevorzugt VHL‑defiziente Zellen.
Wie die DNA‑Markierung VHL‑Verlust mit Zelltod verbindet
Bei tiefergehenden Untersuchungen fanden die Forschenden heraus, warum VHL‑defiziente Zellen so empfindlich auf diese Wirkstoffe reagieren. Der Verlust von VHL führt zu einer dauerhaften Aktivierung von HIF‑2α, was wiederum die Menge von DNMT1 erhöht, dem Haupt‑DNA‑Markierungsenzym, das Methyl‑Marken während der Zellteilung erhält. Patientendaten bestätigten, dass DNMT1 in Nierenkrebs häufiger vorkommt als im normalen Nierengewebe und mit HIF‑2α zunimmt. Dieses erhöhte DNMT1 trägt zu einer weitreichenden DNA‑Hypermethylierung bei. Als das Team DNMT1, DNMT3A oder DNMT3B einzeln genetisch reduzierte, begannen VHL‑defiziente Zellen zu sterben; das ahmte teilweise die Wirkung der Medikamente nach und bestätigte, dass die Blockade der DNA‑Methylierung selbst – und nicht nur Nebenwirkungen der Wirkstoffe – entscheidend ist. Bei Mäusen mit implantierten VHL‑defizienten Nierentumoren verlangsamte Decitabin die Tumorwachstumsrate deutlich, ohne offensichtlichen Gewichtsverlust oder Toxizität, was darauf hindeutet, dass diese Verwundbarkeit auch in lebenden Organismen relevant ist.
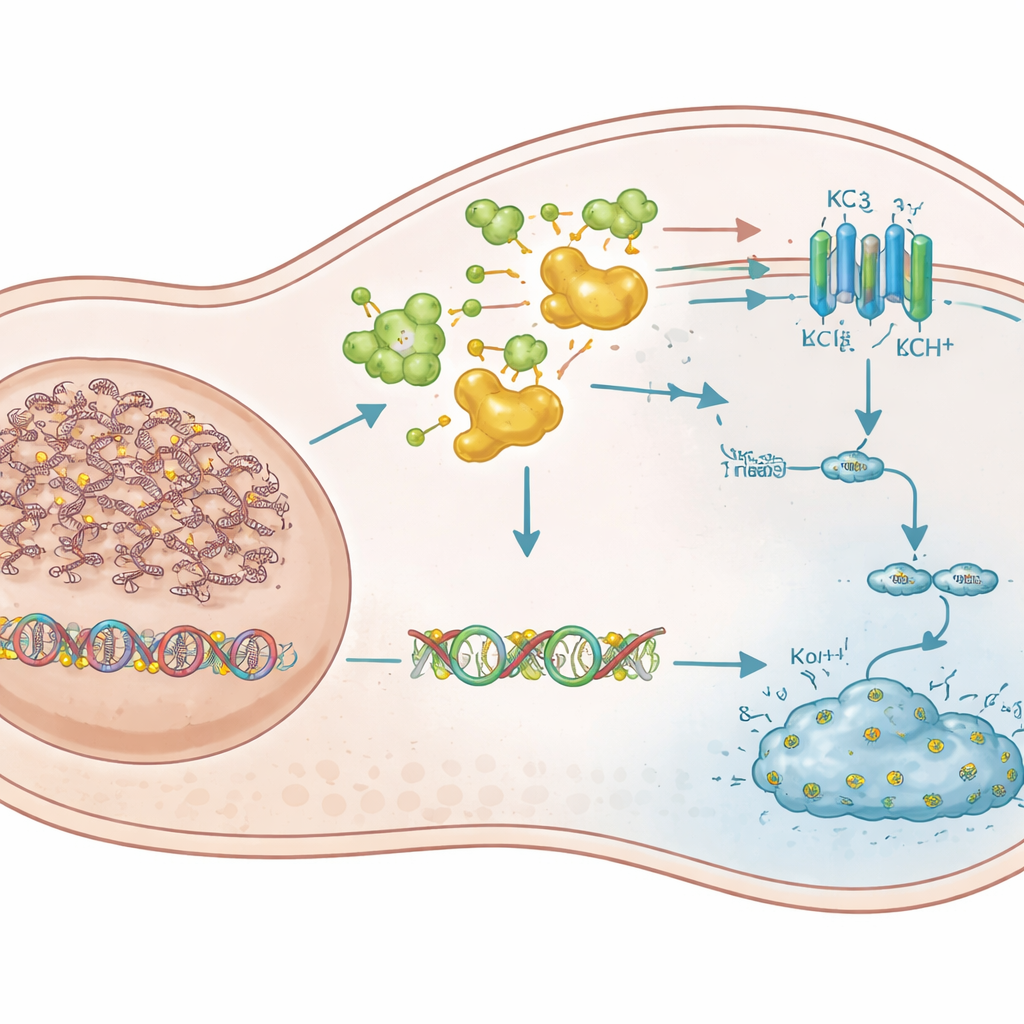
Ein stummgelegener Wächtergen kehrt zurück
Um herauszufinden, welche methylierungsgeschalteten Gene am wichtigsten sind, verglichen die Autoren die Genaktivität in VHL‑defizienten und VHL‑wiederhergestellten Zellen vor und nach Decitabin‑Behandlung. Sie konzentrierten sich auf Gene, die als Tumorsuppressoren bekannt oder verdächtigt sind, in VHL‑defizienten Zellen abgeschaltet, durch das Medikament jedoch wieder erweckt wurden. Von 14 starken Kandidaten stach ein Gen hervor: KCNK3. KCNK3 kodiert für einen Kaliumkanal – eine winzige Pore in der Zellmembran, die den Fluss von Kaliumionen steuert. Bei VHL‑defizienten Nierenkrebszellen war der vordere Abschnitt des KCNK3‑Gens stark methyliert und seine Aktivität nahezu nicht vorhanden. DNMT‑blockierende Wirkstoffe entfernten diese Methylmarken, stellten KCNK3‑Spiegel wieder her und lösten starkes Wachstumshemmung und Zelltod aus. Wenn KCNK3 experimentell reaktiviert wurde, stellten die Zellen das Teilen ein; wurde es herunterreguliert, verschwand der tödliche Effekt von Decitabin weitgehend – sowohl in Zellkulturen als auch in Mäusetumoren. Patientendatensätze zeigten außerdem, dass KCNK3 in Nierentumoren stärker methyliert ist als im normalen Nierengewebe und dass höhere Methylierung mit schlechterm Überleben korreliert.
Signalwege, die Zellen in den Selbstmord treiben
Die Wiederherstellung von KCNK3 bewirkte mehr, als nur einen Ionenkanal zu öffnen. RNA‑Sequenzierung von Zellen mit und ohne KCNK3 unter Decitabin‑Behandlung zeigte, dass die Reaktivierung von KCNK3 Signale verstärkt, die mit Nährstoffstress, Tumor‑Nekrose‑Faktor‑alpha (TNF‑α) und wichtigen Stressantwortwegen, den MAPK‑Signalwegen, verbunden sind. Diese wiederum speisen die zelluläre Selbstmordmaschinerie. In Zellen mit normalem KCNK3 erhöhte Decitabin die TNF‑α‑Spiegel und aktivierte nachgeschaltete Signalwege, während es das Überlebensprotein BCL‑2 senkte und Ausführerproteine wie gespaltenes Caspase‑3 und PARP‑Spaltung vermehrt erscheinen ließ. War KCNK3 vermindert, blieben diese Veränderungen abgeschwächt und die Zellen widerstanden der Apoptose. Das entstehende Bild ist, dass in VHL‑defizienten Zellen DNMT‑getriebene Methylierung KCNK3 abschaltet und Todessignale dämpft; DNMT‑Inhibitoren nehmen diese Bremse weg, wecken KCNK3 und treiben die Zellen über einen TNF‑α‑ und MAPK‑gesteuerten Weg in die Selbstzerstörung.
Was das für Patienten bedeuten könnte
In der Summe legen die Ergebnisse nahe, dass Inhibitoren von DNA‑Methyltransferasen eine spezifische Verdrahtung von VHL‑defizienten Nierentumoren ausnutzen: VHL‑Verlust hebt HIF‑2α an, was DNMT1 erhöht, das wiederum schützende Gene wie KCNK3 stilllegt. Die Aufhebung dieser Stummschaltung mit Wirkstoffen tötet selektiv die defekten Zellen, indem sie starke Todeswege reaktiviert. Da Decitabin und Azacitidin bereits bei Blutkrebserkrankungen eingesetzt werden, eröffnet diese Entdeckung die Möglichkeit, sie oder verwandte Substanzen für Patienten mit VHL‑mutierten Nierentumoren und hoher KCNK3‑Methylierung umzunutzen. Mit weiteren klinischen Prüfungen könnten VHL‑Status und KCNK3‑Methylierung helfen, Patienten gezielt Epigenetik‑Therapien zuzuordnen, die diese eingebaute Schwäche ausnutzen.
Zitation: Pu, Y., Wang, Z., Tao, S. et al. DNA methyltransferase inhibition is a therapeutic vulnerability in VHL-deficient renal cell carcinoma cells. Exp Mol Med 58, 798–812 (2026). https://doi.org/10.1038/s12276-026-01663-w
Schlüsselwörter: Nierenzellkarzinom, VHL‑Mutation, DNA‑Methylierung, DNMT‑Inhibitoren, KCNK3