Clear Sky Science · pt
Inibição de metiltransferases de DNA é uma vulnerabilidade terapêutica em células de carcinoma renal deficientes em VHL
Por que este estudo sobre câncer de rim importa
O câncer renal frequentemente é diagnosticado tardiamente e pode ser resistente aos tratamentos habituais. Este estudo revela uma fraqueza oculta em um subtipo comum de tumores renais: quando um gene protetor chave chamado VHL é perdido, as células tumorais passam a depender de modo incomum de um processo químico que silencia outros genes. Ao bloquear essa maquinaria de silenciamento com drogas já disponíveis, os pesquisadores conseguiram eliminar células tumorais deficientes em VHL poupando outras, apontando para uma abordagem nova e mais personalizada para tratar pacientes.
Uma falha comum nos tumores renais
A maioria dos cânceres renais do tipo de células claras apresenta alterações no gene VHL, que normalmente ajuda as células a detectar oxigênio e a controlar o crescimento de vasos sanguíneos e o metabolismo. Quando o VHL está ausente, as células entram em um modo crônico de “falso baixo oxigênio” impulsionado por um fator chamado HIF‑2α. Trabalhos anteriores mostraram que esses tumores também acumulam marcas químicas extras — grupos metil — no DNA, especialmente perto de interruptores que ligam genes. Essas marcas podem desligar genes que normalmente contêm o crescimento cancerígeno. O novo estudo buscou responder a uma pergunta simples: se tumores deficientes em VHL dependem dessa marcação anômala do DNA, essa dependência poderia ser transformada em seu calcanhar de Aquiles?
Encontrando drogas que atinjam o ponto fraco
A equipe usou pares de linhas celulares de câncer renal geneticamente idênticas, exceto pelo VHL: um membro do par carecia de VHL, o outro o tinha restaurado. Eles expuseram essas células a uma biblioteca de 128 pequenas moléculas direcionadas a diferentes reguladores “epigenéticos” — proteínas que controlam como o DNA é embalado e marcado. Ao comparar o quanto cada composto retardava o crescimento celular, buscaram agentes especialmente tóxicos para células deficientes em VHL, uma estratégia conhecida como letalidade sintética. Surgiram vários candidatos, mas se destacaram drogas que bloqueiam metiltransferases de DNA — enzimas que adicionam marcas metil ao DNA — incluindo os medicamentos aprovados decitabina e azacitidina e dois compostos experimentais. Em várias linhas de câncer renal e mesmo em modelos de pulmão e fígado nos quais VHL foi desativado, essas drogas mataram preferencialmente as células deficientes em VHL.
Como a marcação do DNA liga perda de VHL à morte celular
Ao investigar mais a fundo, os pesquisadores descobriram por que as células deficientes em VHL são tão sensíveis a essas drogas. A perda de VHL leva à ativação constante de HIF‑2α, que por sua vez aumenta os níveis de DNMT1, a principal enzima que mantém as marcas metil durante a divisão celular. Dados de pacientes confirmaram que DNMT1 é mais abundante em cânceres renais do que em tecido renal normal e aumenta em conjunto com HIF‑2α. Esse DNMT1 elevado contribui para uma hipermetilação generalizada do DNA. Quando a equipe reduziu DNMT1, DNMT3A ou DNMT3B individualmente com ferramentas genéticas, células deficientes em VHL começaram a morrer, imitando em parte o efeito das drogas e confirmando que bloquear a metilação do DNA em si — e não apenas ações fora do alvo dos fármacos — é determinante. Em camundongos implantados com tumores renais deficientes em VHL, o tratamento com decitabina desacelerou fortemente o crescimento tumoral sem perda de peso ou toxicidade óbvias, sustentando a ideia de que essa vulnerabilidade existe em organismos vivos.
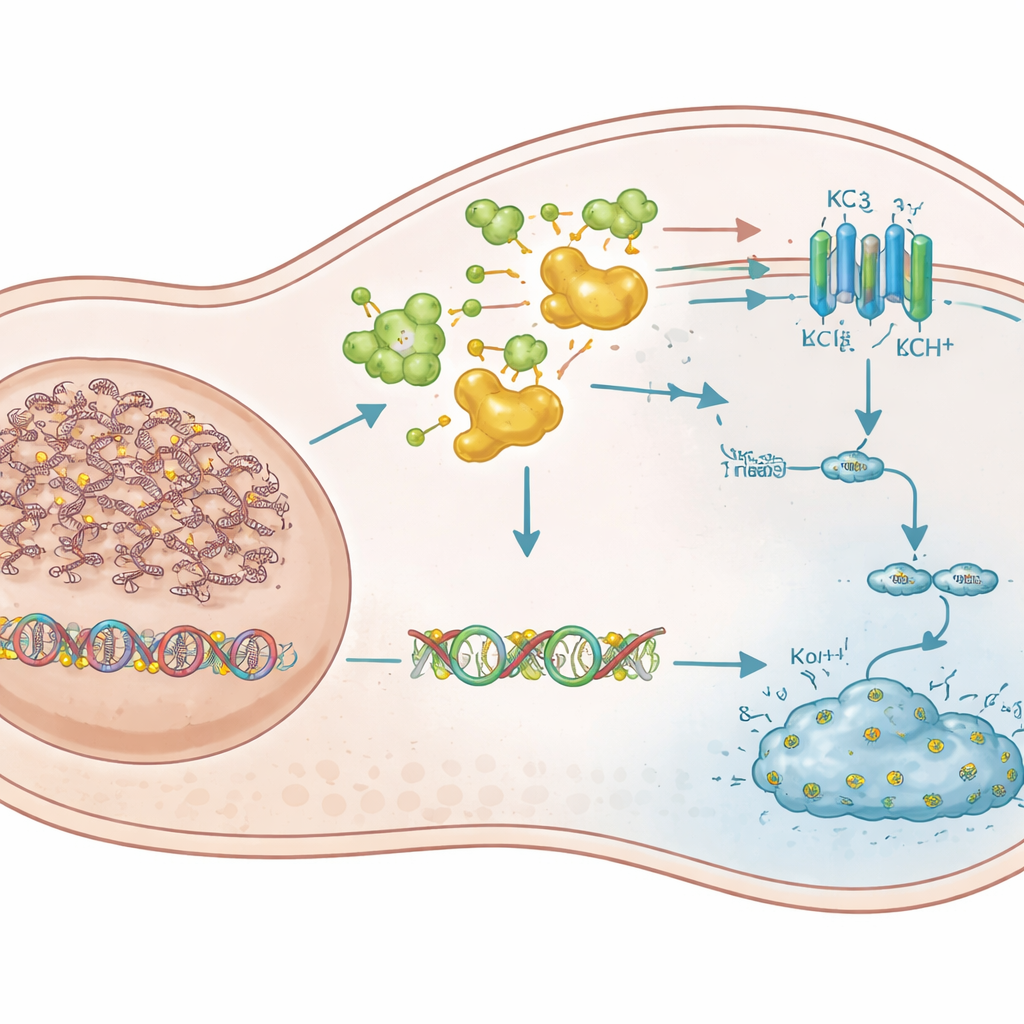
Um gene guardião silenciado retorna
Para identificar quais genes silenciados por metilação eram mais importantes, os autores compararam a atividade gênica em células deficientes e restauradas para VHL antes e depois do tratamento com decitabina. Eles se concentraram em genes conhecidos ou suspeitos de atuar como supressores tumorais que estavam desligados em células deficientes em VHL, mas reativados pela droga. De 14 fortes candidatos, um gene, KCNK3, emergiu como o ator crítico. KCNK3 codifica um canal de potássio — um pequeno poro na membrana celular que controla o fluxo de íons potássio. Nas células de carcinoma renal deficientes em VHL, a região inicial do gene KCNK3 estava fortemente metilada e sua atividade era praticamente ausente. Drogas que bloqueiam DNMTs removeram essas marcas metil, restauraram os níveis de KCNK3 e desencadearam forte inibição do crescimento e morte celular. Quando KCNK3 foi reativado experimentalmente, as células pararam de se dividir; quando foi silenciado, o efeito letal da decitabina desapareceu em grande parte, tanto em placas quanto em tumores de camundongo. Conjuntos de dados de pacientes mostraram ainda que KCNK3 é mais metilado em tumores renais do que no rim normal e que maior metilação prevê pior sobrevida.
Cascatas de sinalização que empurram as células para a autodestruição
Restaurar KCNK3 fez mais do que simplesmente reabrir um canal iônico. Sequenciamento de RNA de células com e sem KCNK3 sob tratamento com decitabina revelou que a reativação de KCNK3 aumenta sinais ligados ao estresse nutricional, ao fator de necrose tumoral alfa (TNF‑α) e a vias de resposta ao estresse conhecidas como MAPK. Estas, por sua vez, alimentam a maquinaria de suicídio celular. Em células com KCNK3 normal, a decitabina elevou os níveis de TNF‑α e ativou sinalização a jusante enquanto reduzía a proteína de sobrevivência BCL‑2 e aumentava proteínas executoras como caspase‑3 clivada e clivagem de PARP. Quando KCNK3 foi depletado, essas mudanças foram atenuadas e as células resistiram à apoptose. O quadro que emerge é que, em células deficientes em VHL, a metilação dirigida por DNMTs desliga KCNK3 e enfraquece sinais de morte; inibidores de DNMT removem esse freio, reativam KCNK3 e empurram as células por um caminho de autodestruição dependente de TNF‑α e MAPK.
O que isso pode significar para pacientes
Em conjunto, o trabalho sugere que inibidores de metiltransferases de DNA exploram uma conexão específica em tumores renais deficientes em VHL: perda de VHL eleva HIF‑2α, que aumenta DNMT1, o que por sua vez silencia genes protetores como KCNK3. Reverter esse silenciamento com drogas mata seletivamente as células defeituosas ao reativar potentes vias de morte. Como decitabina e azacitidina já são usados em cânceres do sangue, essa descoberta abre a possibilidade de reposicioná‑los, ou agentes relacionados, para pacientes cujos tumores renais têm mutações em VHL e alta metilação de KCNK3. Com testes clínicos adicionais, medir o status de VHL e a metilação de KCNK3 poderia ajudar a direcionar indivíduos para terapias epigenéticas que aproveitam essa fraqueza intrínseca.
Citação: Pu, Y., Wang, Z., Tao, S. et al. DNA methyltransferase inhibition is a therapeutic vulnerability in VHL-deficient renal cell carcinoma cells. Exp Mol Med 58, 798–812 (2026). https://doi.org/10.1038/s12276-026-01663-w
Palavras-chave: carcinoma de células renais, mutação VHL, metilação do DNA, inibidores de DNMT, KCNK3