Clear Sky Science · sv
Hämning av DNA‑metyltransferaser är en terapeutisk svaghet i VHL‑defekta njurcellscarcinomceller
Varför denna njurcancerstudie är viktig
Njurcancer upptäcks ofta sent och kan vara svårbehandlad med standardterapier. Denna studie avslöjar en dold svaghet i en vanlig undergrupp av njurtumörer: när en viktig skyddande gen kallad VHL förloras blir cancercellerna ovanligt beroende av en kemisk process som tystar andra gener. Genom att blockera den tystningsmaskineriet med redan befintliga läkemedel kunde forskarna döda VHL‑defekta tumörceller samtidigt som andra celler skons, vilket pekar mot ett nytt, mer skräddarsytt sätt att behandla patienter.
En vanlig brist i njurtumörer
De flesta njurcancer av klarcellstypen bär skador i VHL‑genen, som normalt hjälper celler att känna av syre och hålla blodkärlsbildning och ämnesomsättning under kontroll. När VHL saknas går cellerna in i ett kroniskt "lågsyraläge" som drivs av en faktor kallad HIF‑2α. Tidigare arbete visade att sådana tumörer också bär extra kemiska markörer, så kallade metylgrupper, på sitt DNA, särskilt intill geners på‑switchar. Dessa markörer kan stänga av gener som normalt hämmar cancerutveckling. Den nya studien ställde en enkel fråga: om VHL‑defekta tumörer är beroende av denna onormala DNA‑märkning, kan beroendet vändas till deras akilleshäl?
Att hitta läkemedel som träffar svagheten
Gruppen använde par av njurcancercellinjer som var genetiskt identiska förutom VHL: en partner saknade VHL medan den andra hade VHL återställt. De exponerade dessa celler för ett bibliotek med 128 småmolekyler som riktar sig mot olika "epigenetiska" regulatorer—proteiner som styr hur DNA packas och markeras. Genom att jämföra hur väl varje förening bromsade celltillväxt sökte de efter medel som var särskilt toxiska för VHL‑defekta celler, en strategi känd som syntetisk letalitet. Flera kandidater framträdde, men läkemedel som blockerar DNA‑metyltransferaser—enzymer som sätter metylgrupper på DNA—stod ut, inklusive de godkända preparaten decitabin och azacitidin samt två experimentella föreningar. I flera njurcancerlinjer och även i lung‑ och levercancermodeller där VHL inaktiverats dödade dessa läkemedel i förtur VHL‑defekta celler.
Hur DNA‑märkning kopplar VHL‑förlust till celldöd
När de grävde djupare upptäckte forskarna varför VHL‑defekta celler är så känsliga för dessa läkemedel. Förlust av VHL leder till konstant aktivering av HIF‑2α, vilket i sin tur ökar nivåerna av DNMT1, huvudenzymet som upprätthåller metylmärken under celldelning. Patienttumördata bekräftade att DNMT1 är mer rikligt uttryckt i njurcancer än i normal njurvävnad och ökar i takt med HIF‑2α. Detta förhöjda DNMT1 bidrar till utbredd DNA‑hypermetylering. När teamet minskade DNMT1, DNMT3A eller DNMT3B individuellt med genetiska verktyg började VHL‑defekta celler dö, vilket delvis efterliknade läkemedelseffekten och bekräftade att blockad av DNA‑metylering i sig—inte bara icke‑specifika läkemedelseffekter—är avgörande. I möss med inplanterade VHL‑defekta njurtumörer bromsade behandling med decitabin tumörtillväxten kraftigt utan tydlig viktminskning eller toxisk påverkan, vilket stödjer idén att denna sårbarhet gäller i levande organismer.
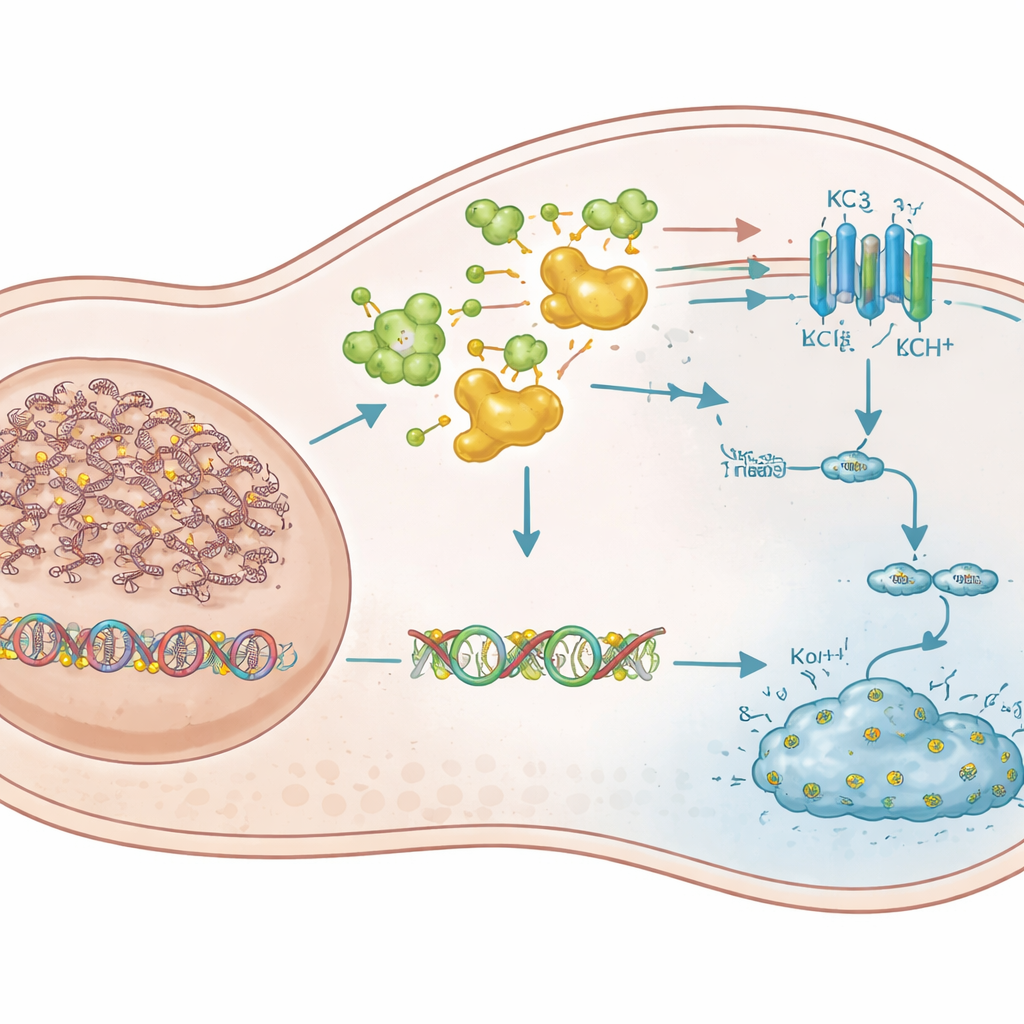
En tystad grindvakt-gen återvänder
För att identifiera vilka metylations‑tysta gener som var viktigast jämförde författarna genaktivitet i VHL‑defekta och VHL‑återställda celler före och efter decitabinbehandling. De fokuserade på gener som är kända eller misstänkta tumörsuppressorer, som var avstängda i VHL‑defekta celler men återväcktes av läkemedlet. Av 14 starka kandidater framträdde en gen, KCNK3, som den kritiska spelaren. KCNK3 kodar för en kaliumkanal—en liten por i cellmembranet som kontrollerar flödet av kaliumjoner. I VHL‑defekta njurcancerceller var den första delen av KCNK3‑genen kraftigt metylerad och dess aktivitet var nästintill obefintlig. DNMT‑blockerande läkemedel avlägsnade dessa metylmärken, återställde KCNK3‑nivåerna och utlöste stark tillväxtinhibering och celldöd. När KCNK3 experimentellt återaktiverades stoppade cellerna delningen; när den slogs ner försvann i stor utsträckning den dödliga effekten av decitabin både i odlingsskålar och i musstumörer. Patientdataset visade dessutom att KCNK3 är mer metylerad i njurtumörer än i normal njurvävnad och att högre metylering förutspår sämre överlevnad.
Signalsystem som skjuter celler mot självförstörelse
Återställandet av KCNK3 gjorde mer än att bara öppna en jonkanal. RNA‑sekvensering av celler med och utan KCNK3 under decitabinbehandling visade att KCNK3‑reaktivering förstärker signaler kopplade till näringsstress, tumörnekrosfaktor‑alfa (TNF‑α) och viktiga stressresponsvägar kända som MAPK‑vägarna. Dessa leder i sin tur in i cellens självmordsprogram. I celler med normalt KCNK3 ökade decitabin TNF‑α‑nivåerna och aktiverade nedströms signalering samtidigt som överlevnadsproteinet BCL‑2 minskade och verkställarproteiner som klyvt caspas‑3 och PARP ökade. När KCNK3 var depleterat dämpades dessa förändringar och cellerna motstod apoptos. Den framväxande bilden är att i VHL‑defekta celler stänger DNMT‑driven metylering av KCNK3 av dödssignaler; DNMT‑hämmare tar bort denna broms, återväcker KCNK3 och driver cellerna längs en TNF‑α‑ och MAPK‑driven väg mot självförstörelse.
Vad detta kan innebära för patienter
Tillsammans tyder arbetet på att DNA‑metyltransferashämmare utnyttjar en specifik koppling i VHL‑defekta njurtumörer: VHL‑förlust höjer HIF‑2α, vilket ökar DNMT1, vilket i sin tur tystar skyddande gener som KCNK3. Att upphäva denna tystnad med läkemedel dödar selektivt de defekta cellerna genom att reaktivera kraftfulla dödsvägar. Eftersom decitabin och azacitidin redan används vid blodcancersjukdomar öppnar denna upptäckt möjligheten att återanvända dem, eller närliggande preparat, för patienter vars njurtumörer bär VHL‑mutationer och hög KCNK3‑metylering. Med vidare klinisk prövning skulle mätning av VHL‑status och KCNK3‑metylering kunna hjälpa till att matcha individer med epigenetiska terapier som utnyttjar denna inneboende svaghet.
Citering: Pu, Y., Wang, Z., Tao, S. et al. DNA methyltransferase inhibition is a therapeutic vulnerability in VHL-deficient renal cell carcinoma cells. Exp Mol Med 58, 798–812 (2026). https://doi.org/10.1038/s12276-026-01663-w
Nyckelord: njurcellscarcinom, VHL‑mutation, DNA‑metylering, DNMT‑hämmare, KCNK3