Clear Sky Science · pl
Hamowanie metylotransferaz DNA to terapeutyczna słabość w komórkach raka nerki z defektem VHL
Dlaczego to badanie raka nerek jest istotne
Rak nerki często wykrywany jest późno i może być oporny na standardowe terapie. To badanie ujawnia ukrytą słabość w powszechnym podtypie guzów nerkowych: gdy tracony jest kluczowy gen ochronny o nazwie VHL, komórki nowotworowe stają się wyjątkowo zależne od procesu chemicznego wyciszającego inne geny. Blokując ten mechanizm wyciszania za pomocą już dostępnych leków, badacze byli w stanie zabić komórki nowotworowe pozbawione VHL, oszczędzając inne komórki, co wskazuje na nową, bardziej ukierunkowaną drogę leczenia pacjentów.
Wspólny defekt w guzach nerek
Większość raków nerek typu jasnokomórkowego ma uszkodzenia w genie VHL, który normalnie pomaga komórkom wyczuwać tlen oraz kontrolować wzrost naczyń i metabolizm. Gdy VHL jest nieobecny, komórki przełączają się na przewlekły „stan niskiego tlenu” napędzany czynnikiem o nazwie HIF‑2α. Wcześniejsze badania pokazały, że takie guzy mają też dodatkowe znaczniki chemiczne, zwane grupami metylowymi, na DNA, szczególnie w pobliżu przełączników aktywujących geny. Te znaczniki mogą wyłączać geny, które normalnie powstrzymują rozwój nowotworu. Nowe badanie postawiło proste pytanie: jeśli guzy pozbawione VHL polegają na tym nieprawidłowym znakowaniu DNA, czy zależność ta może stać się ich piętą achillesową?
Poszukiwanie leków trafiających w słaby punkt
Zespół użył par linii komórkowych raka nerki identycznych genetycznie, z wyjątkiem VHL: jeden partner pozbawiony był VHL, drugi miał go przywróconego. Ekspozycji poddano bibliotekę 128 małych cząsteczek celujących w różne regulatory „epigenetyczne” — białka kontrolujące, jak DNA jest upakowane i oznakowane. Porównując, jak każdy związek hamował wzrost komórek, szukano środków szczególnie toksycznych dla komórek pozbawionych VHL, strategii znanej jako śmiertelność syntetyczna. Pojawiło się kilka kandydatów, lecz wyróżniły się leki blokujące metylotransferazy DNA — enzymy dodające grupy metylowe do DNA — w tym zatwierdzone leki deacytabina i azacytydyna oraz dwa związki eksperymentalne. W wielu liniach raka nerki, a nawet w modelach raka płuca i wątroby z wyłączonym VHL, leki te preferencyjnie zabijały komórki pozbawione VHL.
Jak znakowanie DNA łączy utratę VHL ze śmiercią komórek
Pogłębiając analizę, badacze odkryli, dlaczego komórki bez VHL są tak wrażliwe na te leki. Utrata VHL prowadzi do stałej aktywacji HIF‑2α, co z kolei zwiększa poziomy DNMT1 — głównego enzymu znakującego DNA, który utrzymuje znaki metylowe podczas podziału komórek. Dane z guzów pacjentów potwierdziły, że DNMT1 jest bardziej obfity w rakach nerek niż w normalnej tkance nerkowej i wzrasta równolegle z HIF‑2α. Podwyższony DNMT1 przyczynia się do rozległej hipermetylacji DNA. Gdy zespół zmniejszał poziomy DNMT1, DNMT3A lub DNMT3B pojedynczo za pomocą narzędzi genetycznych, komórki pozbawione VHL zaczynały obumierać, częściowo naśladując efekt leku i potwierdzając, że kluczowe jest blokowanie metylacji DNA — a nie jedynie działania uboczne leków. U myszy z wszczepionymi nowotworami nerek pozbawionymi VHL, leczenie deacytabiną gwałtownie spowolniło wzrost guzów bez oczywistej utraty masy ciała czy toksyczności, wspierając tezę, że ta słabość działa także in vivo.
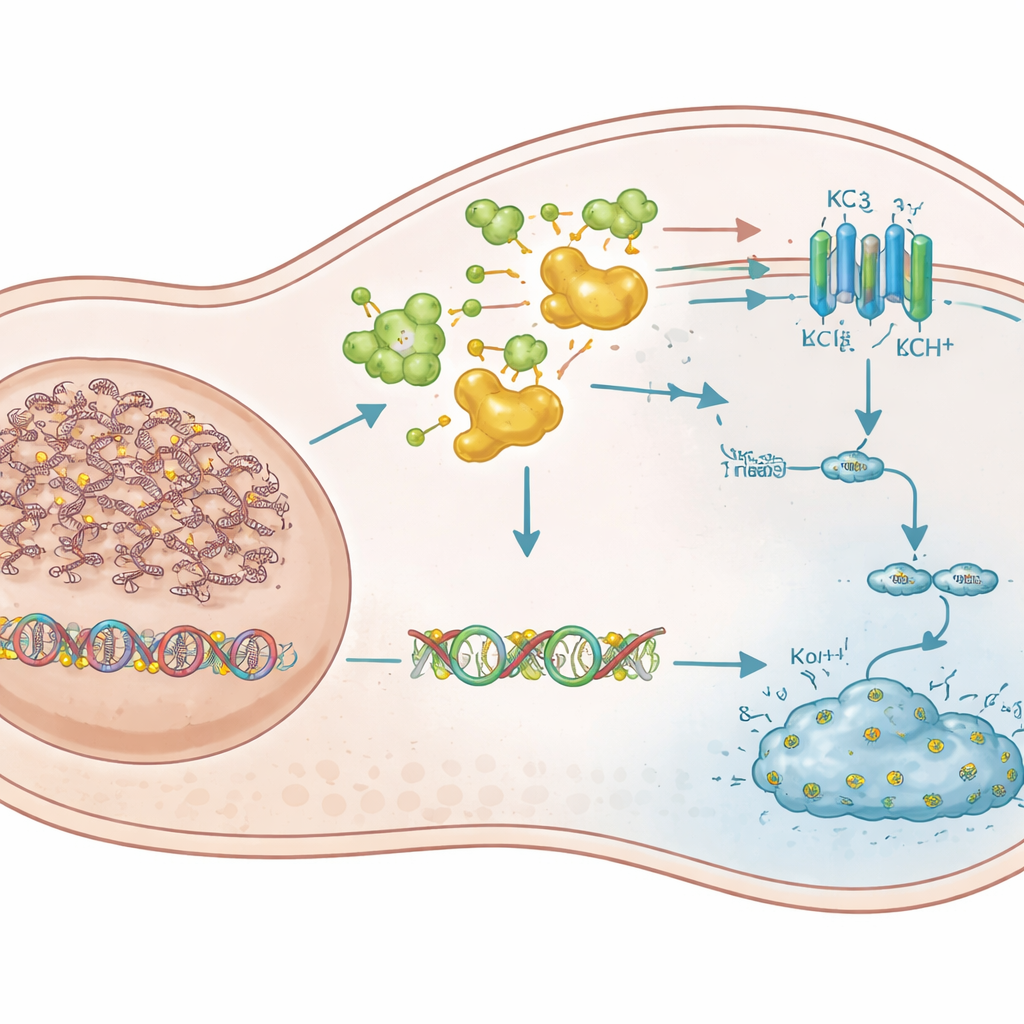
Powrót wyciszonego genu strażnika
Aby ustalić, które wyciszone przez metylację geny są najważniejsze, autorzy porównali aktywność genów w komórkach pozbawionych VHL i przywróconym VHL przed i po leczeniu deacytabiną. Skupili się na genach znanych lub podejrzewanych o działanie jako supresory nowotworu, które były wyłączone w komórkach bez VHL, ale przebudzone przez lek. Z 14 silnych kandydatów jeden gen, KCNK3, wyróżnił się jako kluczowy gracz. KCNK3 koduje kanał potasowy — drobny otwór w błonie komórkowej kontrolujący przepływ jonów potasu. W komórkach raka nerki pozbawionych VHL pierwsza część genu KCNK3 była silnie zmethylowana, a jego aktywność niemal nie występowała. Leki blokujące DNMT usunęły te oznaczenia metylowe, przywróciły poziomy KCNK3 i wywołały silne zahamowanie wzrostu oraz śmierć komórek. Gdy KCNK3 został eksperymentalnie włączony, komórki przestały się dzielić; gdy był wyciszony, śmiertelny efekt deacytabiny w dużej mierze znikał zarówno w hodowlach, jak i w guzach mysich. Dane od pacjentów dodatkowo wykazały, że KCNK3 jest bardziej zmethylowany w guzach nerek niż w normalnej nerce i że wyższa metylacja przewiduje gorsze przeżycie.
Szlaki sygnałowe wpędzające komórki w samozniszczenie
Przywrócenie KCNK3 robiło więcej niż przywrócić kanał jonowy. Sekwencjonowanie RNA komórek z i bez KCNK3 podczas leczenia deacytabiną ujawniło, że reaktywacja KCNK3 wzmacnia sygnały związane ze stresem odżywczym, czynnikiem martwicy nowotworu alfa (TNF‑α) oraz kluczowymi szlakami odpowiedzi na stres znanymi jako szlaki MAPK. Te sygnały z kolei aktywują mechanizmy samobójcze komórki. W komórkach z normalnym KCNK3 deacytabina zwiększała poziomy TNF‑α i aktywowała dalsze sygnałowanie, jednocześnie obniżając białko przeżyciowe BCL‑2 i zwiększając białka egzekucyjne, takie jak sfalaktynowany kaspaza‑3 i rozszczepienie PARP. Gdy KCNK3 był usunięty, te zmiany były osłabione i komórki wykazywały oporność na apoptozę. Powstający obraz wskazuje, że w komórkach pozbawionych VHL metylacja napędzana przez DNMT wyłącza KCNK3 i tłumi sygnały śmierci; inhibitory DNMT usuwają tę blokadę, reaktywują KCNK3 i popychają komórki w kierunku samozniszczenia napędzanego przez TNF‑α i szlaki MAPK.
Co to może znaczyć dla pacjentów
Podsumowując, praca sugeruje, że inhibitory metylotransferaz DNA wykorzystują specyficzne połączenia w guzach nerek pozbawionych VHL: utrata VHL uwalnia HIF‑2α, który podnosi DNMT1, co z kolei ucisza geny ochronne, takie jak KCNK3. Cofnięcie tego wyciszenia za pomocą leków selektywnie zabija defektywne komórki przez reaktywację potężnych ścieżek prowadzących do śmierci. Ponieważ deacytabina i azacytydyna są już stosowane w nowotworach krwi, odkrycie to otwiera możliwość ponownego wykorzystania ich lub pokrewnych związków u pacjentów, których guzy nerkowe niosą mutacje VHL i wysoką metylację KCNK3. Po dalszych badaniach klinicznych określanie statusu VHL i metylacji KCNK3 mogłoby pomóc dopasować pacjentów do terapii epigenetycznych wykorzystujących tę wrodzoną słabość.
Cytowanie: Pu, Y., Wang, Z., Tao, S. et al. DNA methyltransferase inhibition is a therapeutic vulnerability in VHL-deficient renal cell carcinoma cells. Exp Mol Med 58, 798–812 (2026). https://doi.org/10.1038/s12276-026-01663-w
Słowa kluczowe: rak nerki, mutacja VHL, metylacja DNA, inhibitory DNMT, KCNK3