Clear Sky Science · sv
Vrede mot medelvärdet: ett perspektiv på att mäta fitness hos enskilda fagpartiklar
Varför små virus spelar roll i vardagen
Bakteriofager – virus som infekterar bakterier – är de mest talrika biologiska enheterna på jorden och undersöks som verktyg för att bekämpa antibiotikaresistenta infektioner, rengöra industrirör och forma hälsosamma mikrobiom. Ändå kommer nästan all vår kunskap om dem från metoder som beräknar genomsnittlig beteende för biljoner partiklar samtidigt. Denna artikel hävdar att för att verkligen utnyttja fager för vetenskap och medicin måste vi lära oss att mäta vad varje enskild viruspartikel gör, inte bara vad massan gör i genomsnitt.
Från massmedelvärden till individuella berättelser
Klassiska fagexperiment uppfanns i början av 1900‑talet, när virus först upptäcktes och visualiserades. Dessa verktyg – såsom plackassayer och enstegs tillväxtkurvor – har varit oerhört framgångsrika för att kartlägga fagers allmänna livscykel: hur de fäster vid en bakterie, injicerar sitt genetiska material, kopierar sig själva och spränger cellen. Men de fungerar genom att blanda ihop stora populationer av virus och bakterier och sedan läsa av ett enda tal, som en genomsnittlig infektionsfrekvens eller genomsnittligt antal avkommor. Eventuella skillnader mellan enskilda viruspartiklar suddas ut och lämnar en jämn bild som kan dölja de extrema variationer som är viktigast för evolution, ekologi och terapi.
Följa enskilda virus genom en infektion
Nya bildtekniker och flödesbaserade metoder börjar avslöja denna dolda mångfald. Med avancerade optiska mikroskop kan forskare nu märka fager med fluorescerande färgämnen eller genmodifierade lysande proteiner och följa deras rörelser som ljusa prickar. Dessa experiment visar att när fager först möter en bakterieyta beter de sig inte alla likadant: vissa studsar snabbt bort, andra vandrar längs ytan och en del fäster sig hårt. Den tid varje partikel tillbringar fäst kan variera över många sekunder, och rörelsemönstret för bundna respektive obundna partiklar visar att det finns flera interaktionslägen snarare än ett enhetligt adsorptionssteg.
Se virala genom och lyseringar en cell i taget
Mikroskopi har också använts för att fånga ögonblicket när en fags genetiska material går in i en cell. Genom att färga viralt DNA har forskare observerat glöden flytta sig från kapsiden in i bakterien, och de finner att vissa genom strömmar in snabbt medan andra pausar eller stannar upp i flera minuter innan de fullbordar inträdet. På liknande sätt kan tidsförloppavbildning av enskilda infekterade celler avgöra när varje cell lyserar, och visa en spridning av lysistider även för genetiskt identiska virus i samma förhållanden. Mikfluidiska enheter som håller bakterier i små kanaler, kombinerat med fluorescerande rapportörer för fagkomponenter, låter nu forskare följa individuella infektioner från första kontakt genom genomintrång, virusproduktion och lysering i just samma cell.
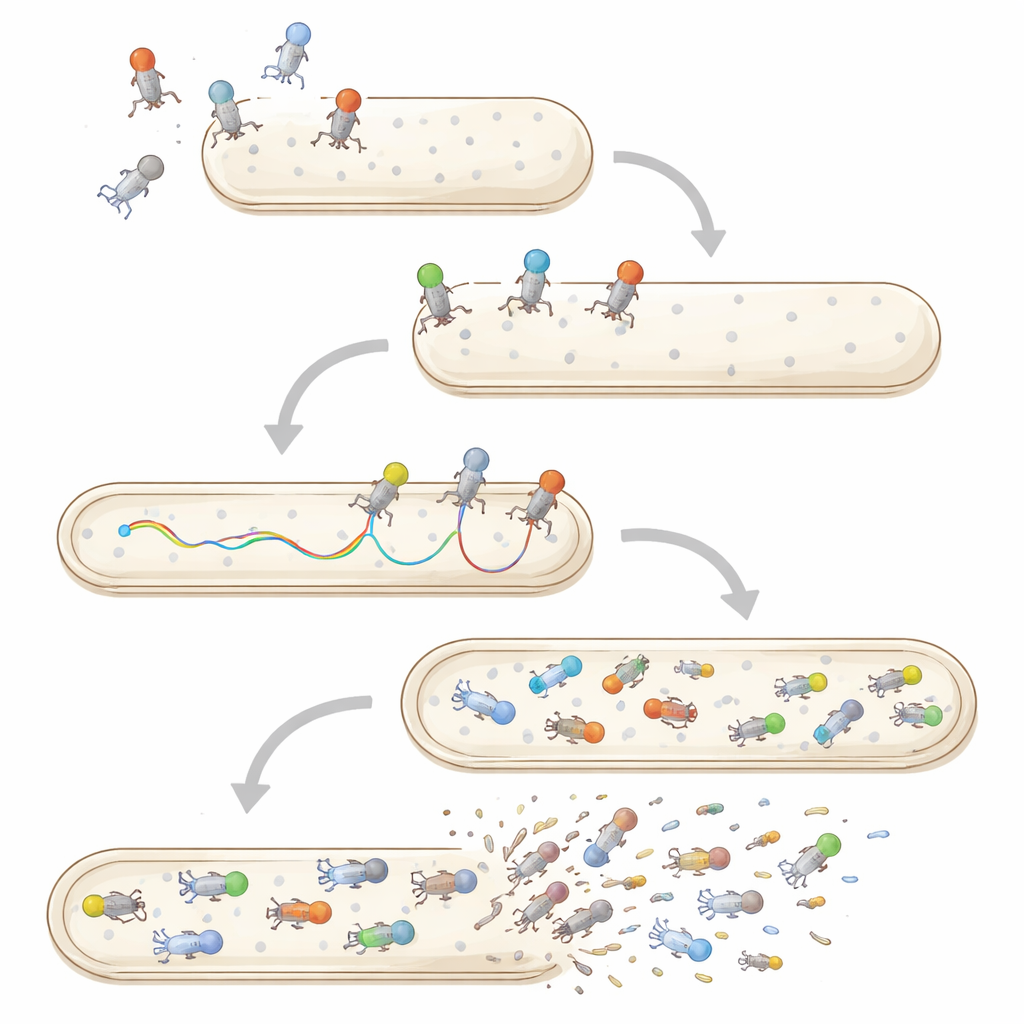
Multipla infektioner, stabilitet och liv bortom bakterier
Enpartikel- och enkelcellsmetoder omformar också hur vi ser på samtidig infektion och virusöverlevnad. När flera fager angriper samma bakterie visar avbildning och flödescytometri att deras genom inte alla går in eller replikerar lika; vissa blockeras eller fördröjs och en stam kan dominera avkommorna. Utanför bakterier möter enskilda fagpartiklar påfrestningar såsom värme, surhet eller angrepp av mänskliga och djurceller. Traditionella tester rapporterar endast hur många virus som i genomsnitt förblir infektiva efter sådan exponering, men nyare metoder följer enskilda partiklar som diffunderar genom slem eller blir upptagna av däggdjursceller, vilket antyder stora skillnader i vilka virus som består eller snabbt tas bort.
Vad detta betyder för framtida medicin och teknologi
Författarna menar att att omfamna variation på individnivå kommer vara avgörande för både grundläggande biologi och fagbasserade teknologier. Evolution verkar på skillnader mellan partiklar, så att förstå vilka enskilda fager som binder snabbast, injicerar mest pålitligt, replikerar mest effektivt eller förblir stabila längst kan förklara hur virala stammar anpassar sig i hav, jord och mikrobiom. Samma information kan vägleda utformningen av säkrare, mer effektiva fagterapier och industriella tillämpningar – till exempel att välja kortlivade fager för engångsavsanering eller långlivade, mycket stabila fager för att leverera användbara gener till bakterier. Genom att gå från medelvärden till enpartikelmätningar kan forskare bättre kontrollera vilka virala egenskaper de väljer och tillverkar, och göra fager till mer förutsägbara och kraftfulla verktyg.
Citering: Antani, J.D., Turner, P.E. Rage against the mean: a perspective on measuring fitness of individual phage particles. npj Viruses 4, 21 (2026). https://doi.org/10.1038/s44298-026-00187-4
Nyckelord: bakteriofager, enpartikelvirologi, fagterapi, optisk mikroskopi, viral evolution