Clear Sky Science · es
Rabia contra la media: una perspectiva sobre la medición de la aptitud de partículas individuales de fagos
Por qué los virus diminutos importan en la vida cotidiana
Los bacteriófagos —virus que infectan bacterias— son las entidades biológicas más abundantes de la Tierra y se exploran como herramientas para combatir infecciones resistentes a antibióticos, limpiar tuberías industriales y moldear microbiomas saludables. Sin embargo, casi todo lo que sabemos sobre ellos proviene de métodos que promedian el comportamiento de trillones de partículas a la vez. Este artículo sostiene que, para aprovechar verdaderamente los fagos en la ciencia y la medicina, debemos aprender a medir lo que hace cada partícula viral individual, no solo lo que hace la multitud en promedio.
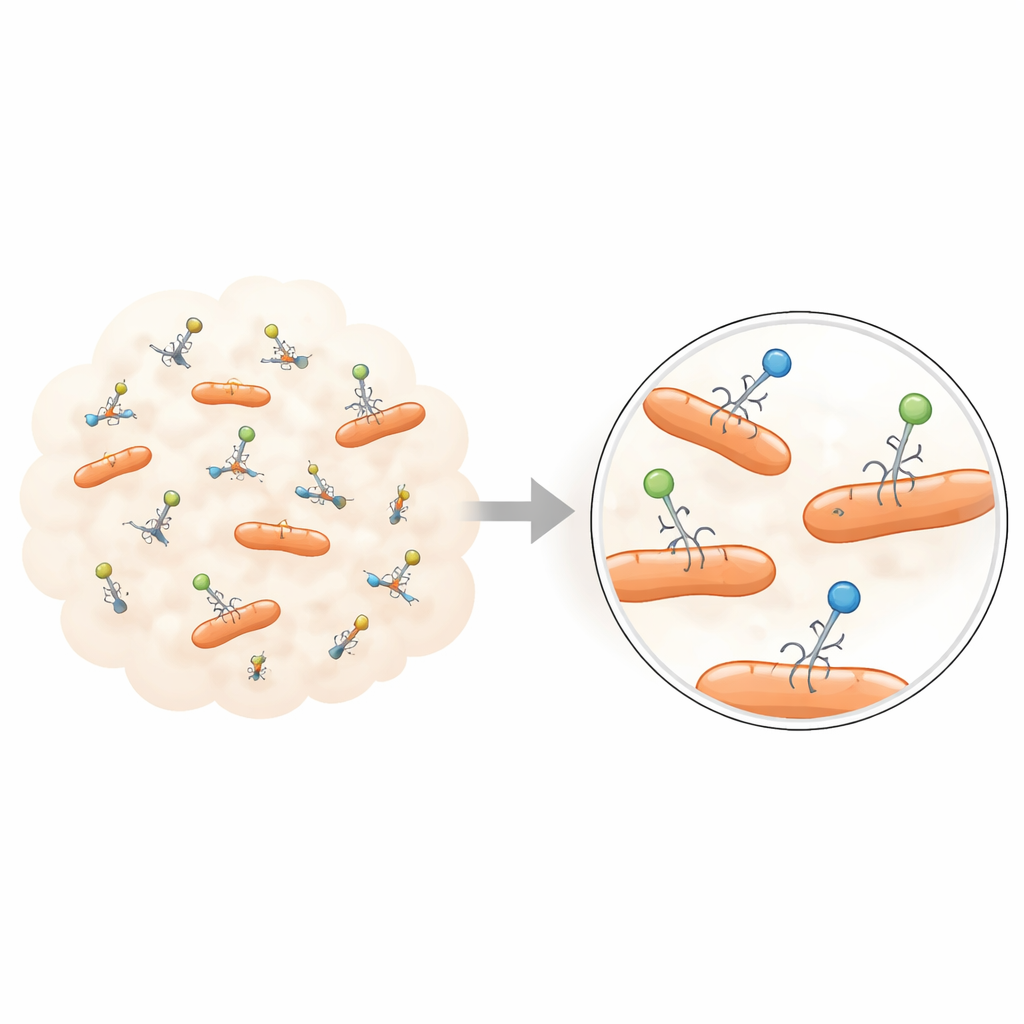
De los promedios de la multitud a historias individuales
Los experimentos clásicos con fagos se inventaron a principios del siglo XX, cuando los virus fueron descubiertos y visualizados por primera vez. Estas herramientas —como los ensayos de placas y las curvas de crecimiento de un solo paso— han sido enormemente exitosas para mapear el ciclo de vida general de los fagos: cómo se adhieren a una bacteria, inyectan su material genético, se reproducen y hacen estallar la célula. Pero funcionan mezclando grandes poblaciones de virus y bacterias y luego leyendo un solo número, como una tasa de infección media o un número medio de descendientes. Cualquier diferencia entre partículas virales individuales se diluye, dejando una imagen uniforme que puede ocultar los extremos que más importan para la evolución, la ecología y la terapia.
Seguir virus individuales durante una infección
Nuevas tecnologías de imagen y basadas en flujo están empezando a revelar esta diversidad oculta. Con microscopios ópticos avanzados, los investigadores ahora pueden marcar fagos con colorantes fluorescentes o proteínas luminosas diseñadas y seguir su movimiento como puntos brillantes. Estos experimentos muestran que cuando los fagos encuentran por primera vez la superficie de una célula bacteriana, no todos se comportan igual: algunos rebotan rápido, otros deambulan por la superficie y una fracción se aferra con fuerza. El tiempo que cada partícula permanece adherida puede variar durante muchos segundos, y el movimiento de las partículas unidas frente a las no unidas revela que existen múltiples estados de interacción en lugar de un único paso de adsorción uniforme.
Observar genomas virales y lisis célula a célula
La microscopía también se ha usado para capturar el momento en que el material genético de un fago entra en una célula. Tiñendo el ADN viral, los científicos han observado el brillo pasar desde la cápside hacia la bacteria, y encuentran que algunos genomas entran rápidamente mientras que otros se detienen o pausan durante minutos antes de completar la entrada. De manera similar, la adquisición de imágenes en lapso de tiempo de células individuales infectadas puede precisar cuándo estalla cada célula, mostrando una distribución de tiempos de lisis incluso para virus genéticamente idénticos en las mismas condiciones. Dispositivos microfluídicos que mantienen bacterias en canales diminutos, combinados con reporteros fluorescentes para componentes del fago, permiten ahora a los investigadores seguir infecciones individuales desde el primer contacto hasta la entrada del genoma, la producción viral y la lisis dentro de una misma célula.
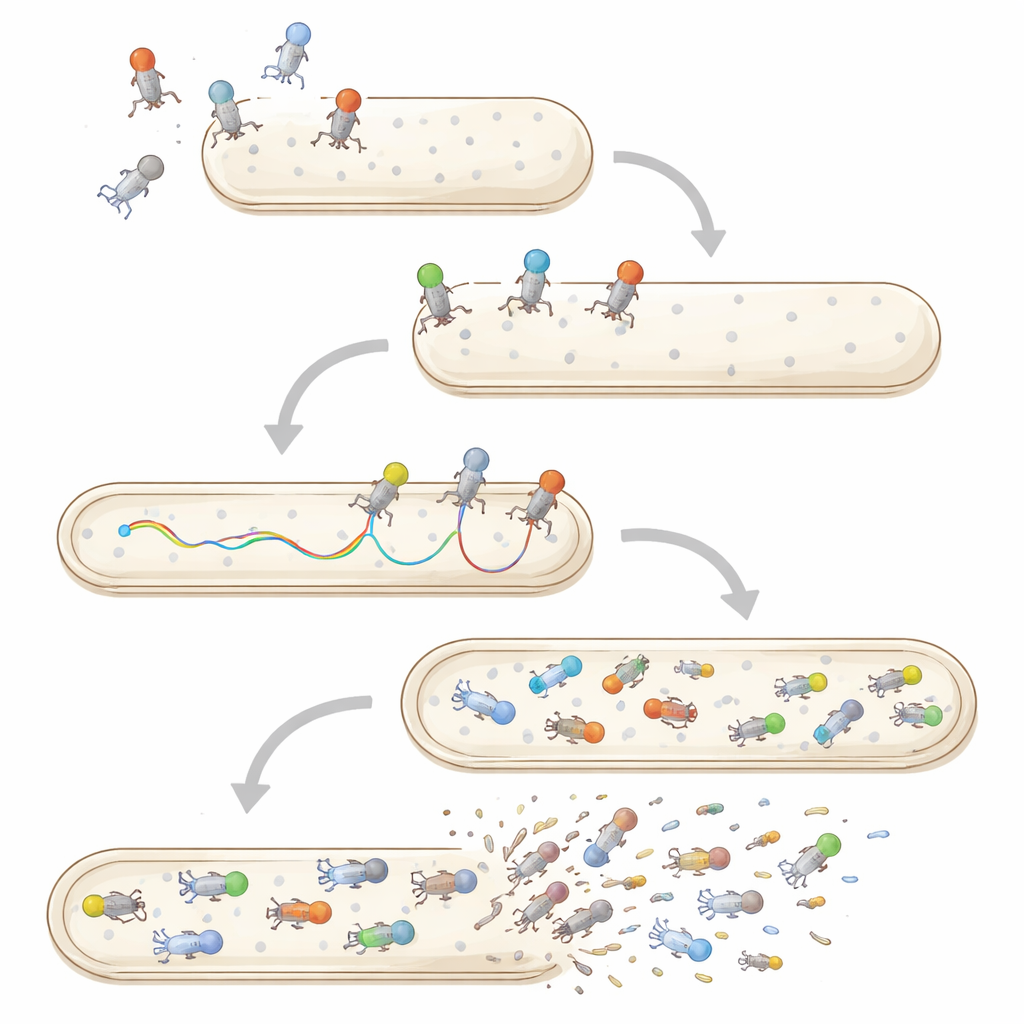
Infecciones múltiples, estabilidad y vida más allá de las bacterias
Los métodos de partícula única y de célula única también están remodelando nuestra visión sobre la coinfección y la supervivencia viral. Cuando varios fagos atacan la misma bacteria, la imagen y la citometría de flujo revelan que sus genomas no entran ni se replican por igual; algunos quedan bloqueados o retrasados, y una línea puede dominar la descendencia. Fuera de las bacterias, las partículas individuales de fagos enfrentan tensiones como el calor, la acidez o el ataque por células humanas y animales. Las pruebas tradicionales solo indican cuántos virus permanecen infecciosos en promedio tras tales exposiciones, pero enfoques más recientes observan partículas únicas difundiendo a través del moco o siendo engullidas por células de mamíferos, lo que sugiere grandes diferencias en cuáles virus persisten o se eliminan rápidamente.
Qué significa esto para la medicina y la tecnología futuras
Los autores sostienen que abrazar esta variación a nivel individual será crucial tanto para la biología básica como para las tecnologías basadas en fagos. La evolución actúa sobre las diferencias entre partículas, por lo que entender qué fagos individuales se unen más rápido, inyectan con mayor fiabilidad, se replican con mayor eficiencia o permanecen estables por más tiempo puede explicar cómo las cepas virales se adaptan en océanos, suelos y microbiomas. La misma información puede guiar el diseño de terapias con fagos e aplicaciones industriales más seguras y eficaces —por ejemplo, elegir fagos de vida corta para descontaminaciones puntuales o fagos de larga duración y alta estabilidad para entregar genes útiles a bacterias. Al pasar de promedios a medidas de partícula única, los investigadores pueden controlar mejor qué rasgos virales seleccionan y fabrican, convirtiendo a los fagos en herramientas más previsibles y potentes.
Cita: Antani, J.D., Turner, P.E. Rage against the mean: a perspective on measuring fitness of individual phage particles. npj Viruses 4, 21 (2026). https://doi.org/10.1038/s44298-026-00187-4
Palabras clave: bacteriófagos, virología de partícula única, terapia con fagos, microscopía óptica, evolución viral