Clear Sky Science · de
Wut gegen den Mittelwert: eine Perspektive zur Messung der Fitness einzelner Phagenpartikel
Warum winzige Viren für den Alltag wichtig sind
Bakteriophagen – Viren, die Bakterien infizieren – sind die häufigsten biologischen Entitäten auf der Erde und werden als Werkzeuge zur Bekämpfung antibiotikaresistenter Infektionen, zur Reinigung industrieller Rohrleitungen und zur Gestaltung gesunder Mikrobiome erforscht. Doch fast alles, was wir über sie wissen, stammt aus Methoden, die das Verhalten von Billionen Partikeln gleichzeitig mitteln. Dieser Artikel argumentiert, dass wir, um Phagen wirklich für Wissenschaft und Medizin nutzbar zu machen, lernen müssen, zu messen, was jedes einzelne Viruspartikel tut, und nicht nur, was die Masse im Durchschnitt tut.
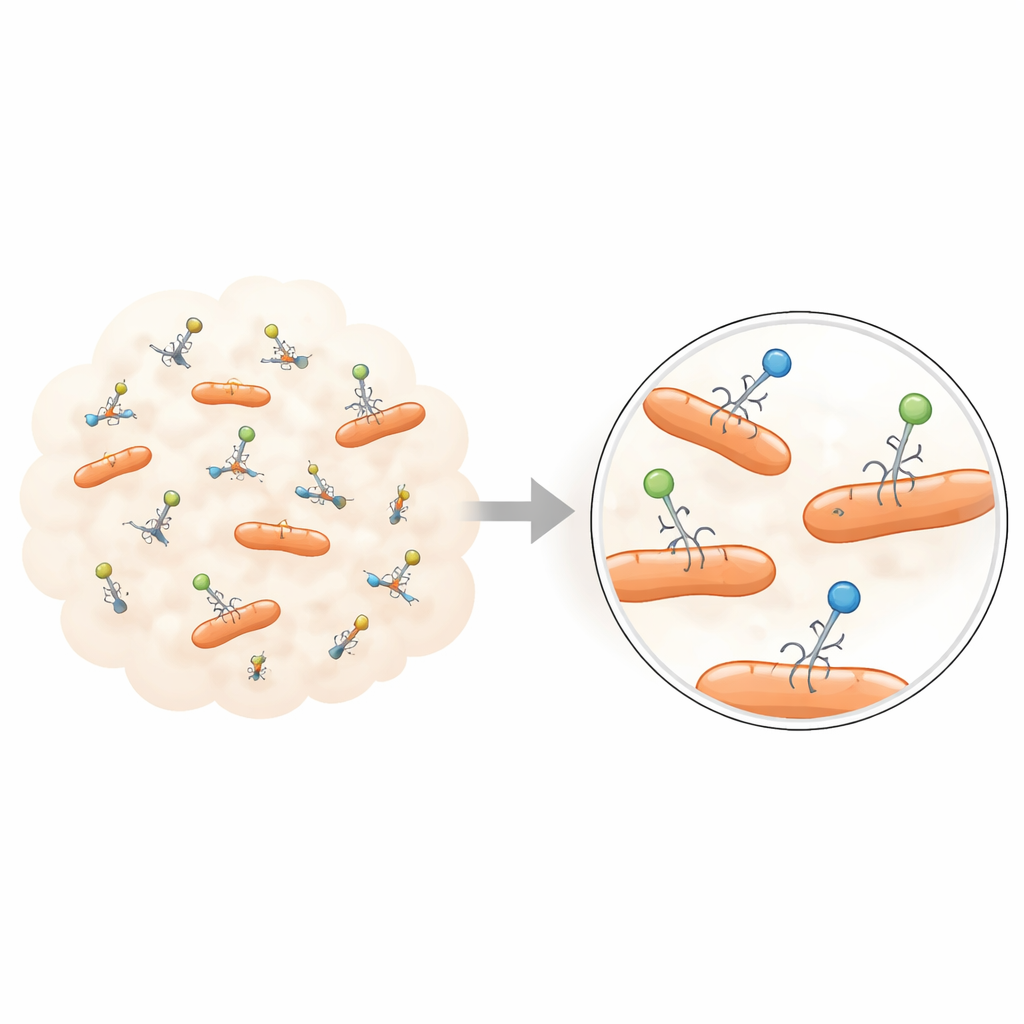
Von Durchschnittswerten zur individuellen Geschichte
Klassische Phagenexperimente entstanden Anfang des 20. Jahrhunderts, als Viren erstmals entdeckt und sichtbar gemacht wurden. Diese Werkzeuge – wie Plaque-Assays und Ein-Schritt-Wachstumskurven – waren außerordentlich erfolgreich darin, den allgemeinen Lebenszyklus von Phagen zu kartieren: wie sie an ein Bakterium anheften, ihr Erbgut injizieren, sich vermehren und die Zelle zum Platzen bringen. Sie funktionieren jedoch, indem sie riesige Populationen von Viren und Bakterien verschmelzen und dann eine einzige Zahl ablesen, etwa eine durchschnittliche Infektionsrate oder eine durchschnittliche Anzahl von Nachkommen. Jegliche Unterschiede zwischen einzelnen Viruspartikeln werden ausgewaschen, so dass ein geglättetes Bild entsteht, das die Extreme verdecken kann, die für Evolution, Ökologie und Therapie am wichtigsten sind.
Einzelne Viren durch eine Infektion verfolgen
Neue Bildgebungs- und Durchfluss-basierte Technologien beginnen, diese verborgene Vielfalt zu enthüllen. Mit fortschrittlichen optischen Mikroskopen können Forscher Phagen inzwischen mit fluoreszenten Farbstoffen oder gentechnisch erzeugten Leuchtproteinen markieren und ihre Bewegung als helle Punkte verfolgen. Diese Experimente zeigen, dass Phagen beim ersten Kontakt mit der Bakterienoberfläche nicht alle gleich reagieren: manche prallen schnell ab, andere wandern entlang der Oberfläche, und ein Teil heftet sich fest an. Die Zeit, die ein Partikel angeheftet verbringt, kann sich über viele Sekunden erstrecken, und die Bewegung gebundener gegenüber ungebundener Partikel legt nahe, dass es mehrere Wechselwirkungszustände gibt statt eines einheitlichen Adsorptionsschritts.
Virale Genome und Lysepunkte Zelle für Zelle beobachten
Mikroskopie wurde auch eingesetzt, um den Moment einzufangen, in dem das Erbgut eines Phagen in eine Zelle gelangt. Durch Anfärben viraler DNA beobachteten Wissenschaftler, wie das Leuchten sich vom Kapsid in das Bakterium bewegt, und stellten fest, dass einige Genome schnell hineinströmen, während andere pausieren oder minutenlang stocken, bevor der Eintritt abgeschlossen ist. Ebenso kann Zeitrafferaufzeichnung einzelner infizierter Zellen genau zeigen, wann jede Zelle platzt, wobei sich auch bei genetisch identischen Viren unter gleichen Bedingungen eine Verteilung der Lysenzeiten ergibt. Mikrofluidische Vorrichtungen, die Bakterien in winzigen Kanälen halten, kombiniert mit fluoreszenten Reportern für Phagenkomponenten, ermöglichen es Forschern nun, einzelne Infektionen vom ersten Kontakt über Genomeintritt, Virenproduktion bis zur Lyse in ein und derselben Zelle zu verfolgen.
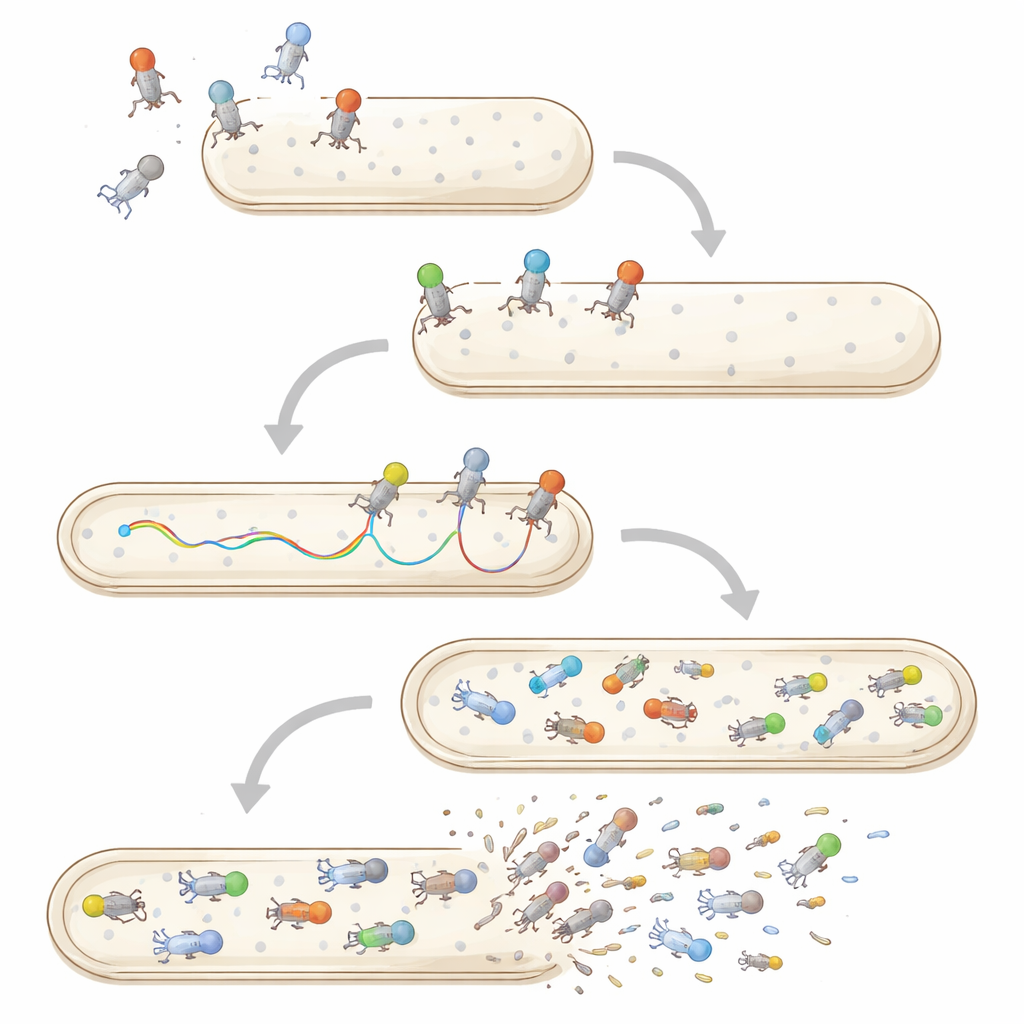
Mehrfachinfektionen, Stabilität und Leben jenseits von Bakterien
Einzelpartikel- und Einzelzellmethoden verändern auch unser Verständnis von Koinfektion und Virusüberleben. Wenn mehrere Phagen dasselbe Bakterium angreifen, zeigen Bildgebung und Durchflusszytometrie, dass ihre Genome nicht alle gleichermaßen eintreten oder replizieren; einige werden blockiert oder verzögert, und eine Linie kann bei den Nachkommen dominieren. Außerhalb von Bakterien sind einzelne Phagenpartikel Belastungen wie Hitze, Säure oder Angriffen durch menschliche und tierische Zellen ausgesetzt. Traditionelle Tests berichten nur, wie viele Viren nach einer solchen Einwirkung im Durchschnitt infektiös bleiben, doch neuere Ansätze beobachten einzelne Partikel, die durch Schleim diffundieren oder von Säugetierzellen aufgenommen werden, und deuten damit auf große Unterschiede hin, welche Viren persistieren oder schnell entfernt werden.
Was das für künftige Medizin und Technik bedeutet
Die Autoren argumentieren, dass die Akzeptanz dieser Variabilität auf Einzelebene sowohl für die Grundlagenbiologie als auch für phagenbasierte Technologien entscheidend sein wird. Evolution wirkt auf Unterschiede zwischen Partikeln, daher kann das Verständnis, welche einzelnen Phagen am schnellsten binden, am zuverlässigsten injizieren, am effizientesten replizieren oder am längsten stabil bleiben, erklären, wie virale Stämme sich in Ozeanen, Böden und Mikrobiomen anpassen. Dieselben Informationen können die Gestaltung sichererer, wirksamerer Phagentherapien und industrieller Anwendungen leiten – beispielsweise die Wahl kurzlebiger Phagen für einmalige Dekontaminationen oder langlebiger, hochstabiler Phagen zum Einbringen nützlicher Gene in Bakterien. Durch den Übergang von Durchschnittswerten zu Einzelpartikelmessungen können Forscher besser steuern, welche viralen Eigenschaften sie selektieren und herstellen, und Phagen zu vorhersehbareren und wirkungsvolleren Werkzeugen machen.
Zitation: Antani, J.D., Turner, P.E. Rage against the mean: a perspective on measuring fitness of individual phage particles. npj Viruses 4, 21 (2026). https://doi.org/10.1038/s44298-026-00187-4
Schlüsselwörter: Bakteriophagen, Einzelpartikel-Virologie, Phagentherapie, optische Mikroskopie, virale Evolution