Clear Sky Science · fr
Rage contre la moyenne : une perspective sur la mesure de la fitness des particules de phage individuelles
Pourquoi les tout petits virus comptent dans la vie quotidienne
Les bactériophages — virus qui infectent les bactéries — sont les entités biologiques les plus abondantes sur Terre et suscitent des recherches en tant qu’outils pour lutter contre les infections résistantes aux antibiotiques, nettoyer les conduites industrielles et façonner des microbiotes sains. Pourtant, presque tout ce que nous savons vient de méthodes qui font la moyenne du comportement de trillions de particules à la fois. Cet article soutient que, pour exploiter pleinement les phages en science et en médecine, il faut apprendre à mesurer ce que fait chaque particule virale individuelle, et pas seulement ce que fait la foule en moyenne.
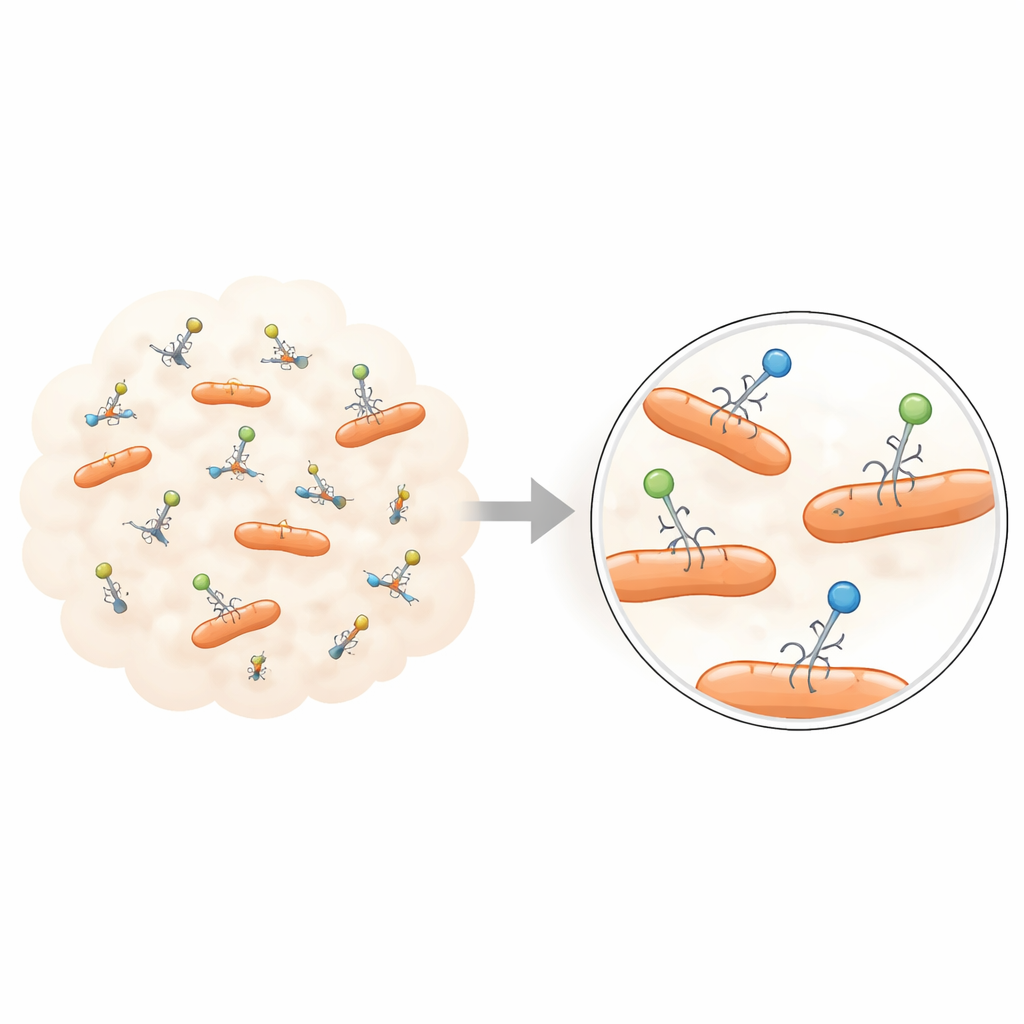
Des moyennes de foule aux histoires individuelles
Les expériences classiques sur les phages ont été inventées au début du XXe siècle, lorsque les virus ont été découverts et visualisés pour la première fois. Ces outils — comme les tests de plaques et les courbes de croissance en un seul pas — ont été extrêmement efficaces pour cartographier le cycle de vie général des phages : comment ils s’attachent à une bactérie, injectent leur matériel génétique, se répliquent et font éclater la cellule. Mais ils fonctionnent en mélangeant d’énormes populations de virus et de bactéries puis en ne lisant qu’un seul chiffre, comme un taux d’infection moyen ou un nombre moyen de descendants. Toutes les différences entre particules virales individuelles sont estompées, laissant une image lisse qui peut masquer les extrêmes qui comptent le plus pour l’évolution, l’écologie et la thérapie.
Suivre des virus individuels au cours d’une infection
De nouvelles technologies d’imagerie et basées sur le flux commencent à révéler cette diversité cachée. À l’aide de microscopes optiques avancés, les chercheurs peuvent maintenant marquer les phages avec des colorants fluorescents ou des protéines lumineuses ingénierées et suivre leur mouvement sous forme de points lumineux. Ces expériences montrent que, lorsque les phages rencontrent pour la première fois la surface d’une cellule bactérienne, ils ne se comportent pas tous de la même façon : certains rebondissent rapidement, d’autres errent le long de la surface, et une fraction s’attache fermement. Le temps que chaque particule passe attachée peut varier sur de nombreuses secondes, et le mouvement des particules liées versus non liées révèle qu’il existe plusieurs états d’interaction plutôt qu’une étape d’adsorption unique et uniforme.
Observer les génomes viraux et les éclatements cellule par cellule
La microscopie a également servi à saisir le moment où le matériel génétique d’un phage pénètre dans une cellule. En colorant l’ADN viral, les scientifiques ont vu la fluorescence se déplacer du capsid vers la bactérie, et constatent que certains génomes affluent rapidement tandis que d’autres font des pauses ou s’interrompent pendant des minutes avant d’achever l’entrée. De même, l’imagerie en temps réel de cellules individuellement infectées peut localiser le moment précis de la lyse de chaque cellule, montrant une dispersion des temps de lyse même pour des virus génétiquement identiques dans les mêmes conditions. Des dispositifs microfluidiques qui maintiennent les bactéries dans de minuscules canaux, combinés à des rapporteurs fluorescents pour les composants du phage, permettent désormais aux chercheurs de suivre des infections individuelles du premier contact jusqu’à l’entrée du génome, la production virale et la lyse au sein d’une même cellule.
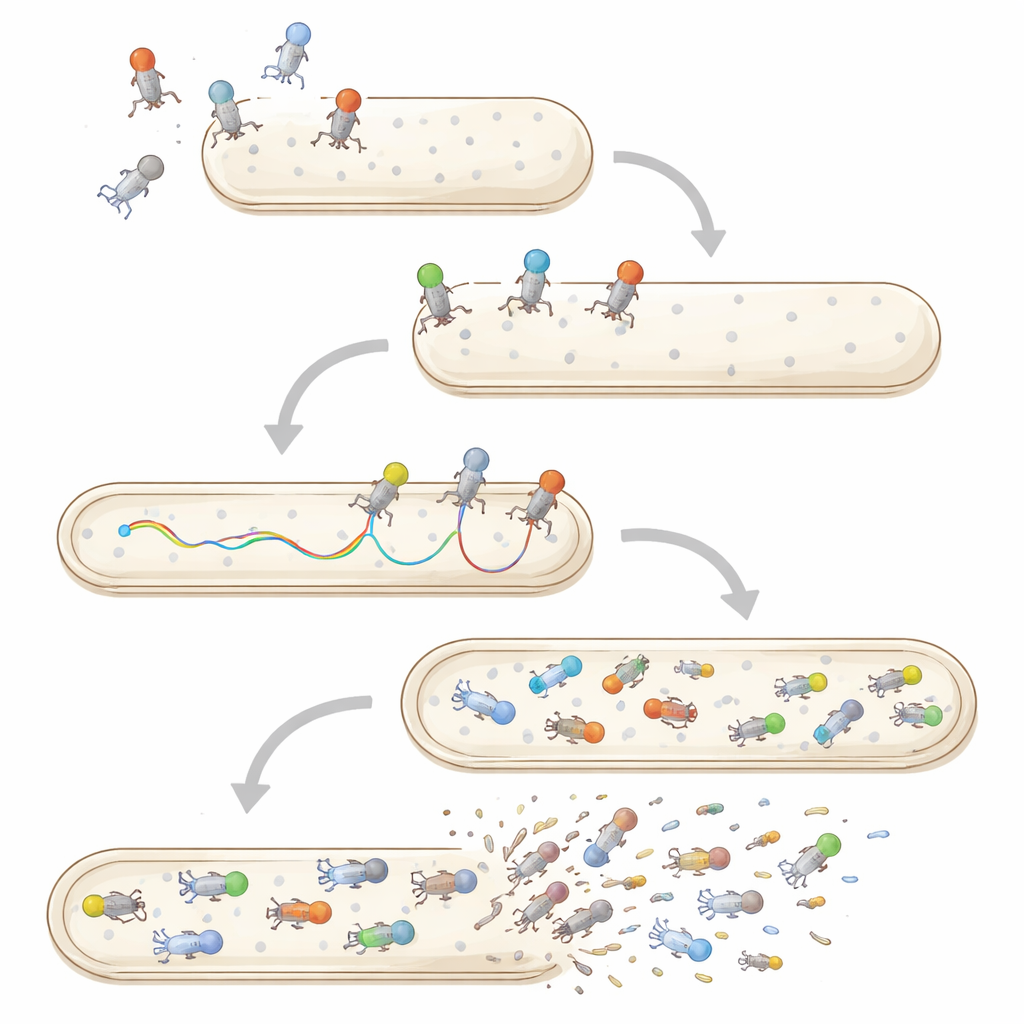
Co‑infections multiples, stabilité et vie au‑delà des bactéries
Les méthodes à particule unique et à cellule unique transforment aussi notre vision de la co‑infection et de la survie virale. Lorsqu’un même nombre de phages attaquent une bactérie, l’imagerie et la cytométrie en flux montrent que leurs génomes n’entrent pas ou ne se répliquent pas tous de manière égale : certains sont bloqués ou retardés, et une lignée peut dominer la descendance. En dehors des bactéries, les particules de phage individuelles subissent des stress tels que la chaleur, l’acidité ou l’attaque par des cellules humaines et animales. Les tests traditionnels ne rapportent que le nombre de virus restant infectieux en moyenne après une telle exposition, mais les approches plus récentes observent des particules uniques diffusant dans le mucus ou étant englouties par des cellules de mammifères, laissant entrevoir de grandes différences quant à quels virus persistent ou sont rapidement éliminés.
Ce que cela implique pour la médecine et la technologie futures
Les auteurs soutiennent que l’acceptation de cette variation au niveau individuel sera cruciale pour la biologie fondamentale et pour les technologies à base de phages. L’évolution agit sur les différences entre particules, donc comprendre quels phages individuels se lient le plus vite, injectent le plus fiablement, se répliquent le plus efficacement ou restent stables le plus longtemps peut expliquer comment des souches virales s’adaptent dans les océans, le sol et les microbiotes. Les mêmes informations peuvent orienter la conception de thérapies phagiques et d’applications industrielles plus sûres et plus efficaces — par exemple, choisir des phages à durée de vie courte pour une décontamination ponctuelle ou des phages très stables et de longue durée pour délivrer des gènes utiles aux bactéries. En passant des moyennes aux mesures sur particule unique, les chercheurs pourront mieux contrôler les traits viraux qu’ils sélectionnent et fabriquent, faisant des phages des outils plus prévisibles et puissants.
Citation: Antani, J.D., Turner, P.E. Rage against the mean: a perspective on measuring fitness of individual phage particles. npj Viruses 4, 21 (2026). https://doi.org/10.1038/s44298-026-00187-4
Mots-clés: bactériophages, virologie à particule unique, thérapie phagique, microscopie optique, évolution virale