Clear Sky Science · nl
Woede tegen het gemiddelde: een perspectief op het meten van de fitheid van individuele fagdeeltjes
Waarom kleine virussen van belang zijn voor het dagelijks leven
Bacteriofagen — virussen die bacteriën infecteren — zijn de meest talrijke biologische entiteiten op aarde en worden onderzocht als instrumenten om antibiotica‑resistente infecties te bestrijden, industriële leidingen te reinigen en gezonde microbiomen te vormen. Toch is bijna alles wat we over hen weten afkomstig van methoden die het gedrag van biljoenen deeltjes tegelijk middelen. Dit artikel betoogt dat we, om fagen echt in te zetten voor wetenschap en geneeskunde, moeten leren meten wat elk individueel virusdeeltje doet, niet alleen wat de massa gemiddeld doet.
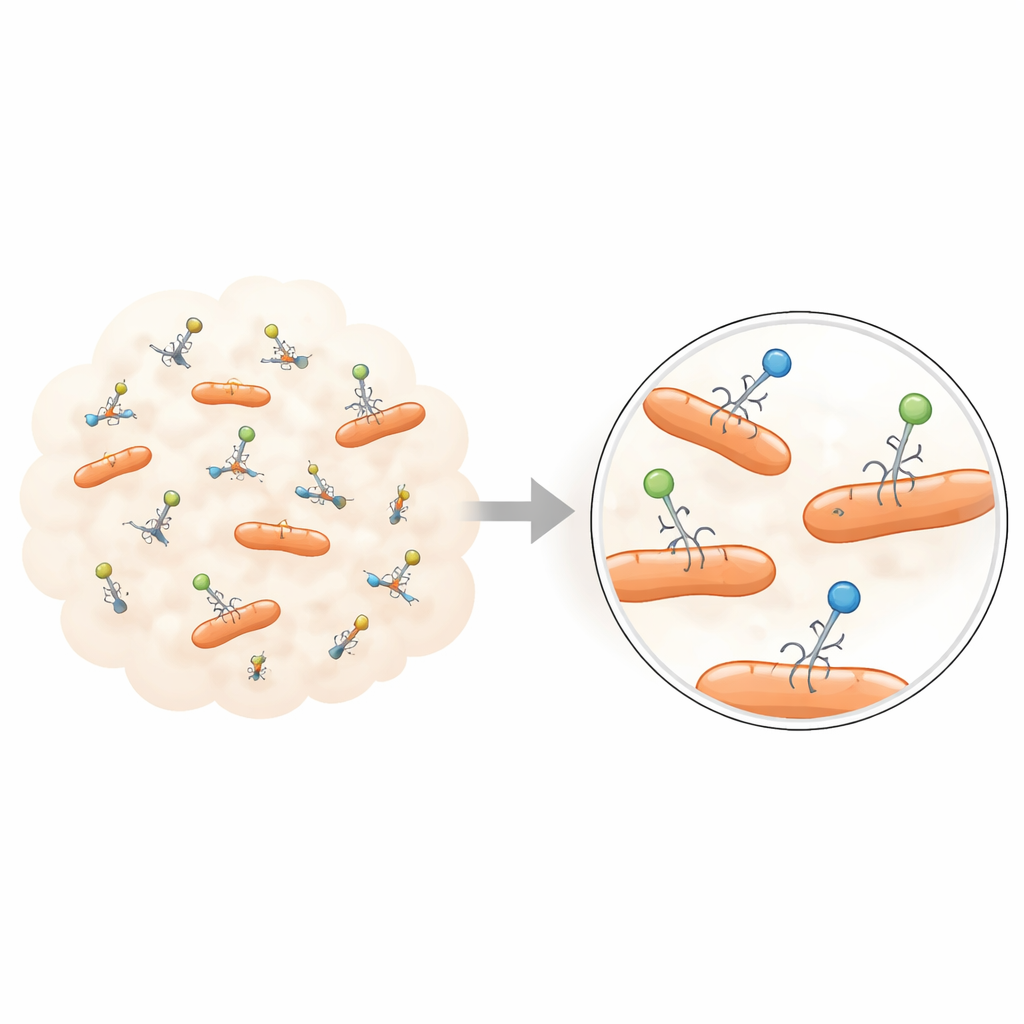
Van groepsgemiddelden naar individuele verhalen
De klassieke fagexperimenten werden uitgevonden begin twintigste eeuw, toen virussen voor het eerst werden ontdekt en zichtbaar gemaakt. Deze instrumenten — zoals plaque‑assays en één‑stap groeicurven — zijn enorm succesvol geweest in het in kaart brengen van de algemene levenscyclus van fagen: hoe ze zich aan een bacterie hechten, hun genetisch materiaal injecteren, kopieën van zichzelf maken en de cel doen barsten. Maar ze werken door enorme populaties virussen en bacteriën samen te voegen en dan één enkel getal af te lezen, zoals een gemiddelde infectiesnelheid of gemiddeld aantal nakomelingen. Alle verschillen tussen individuele virusdeeltjes worden zo weggepoetst, waardoor een glad beeld ontstaat dat de extremen kan verbergen die het meest van belang zijn voor evolutie, ecologie en therapie.
Enkele virussen volgen tijdens een infectie
Nieuwe beeldvormings‑ en flowgebaseerde technologieën beginnen deze verborgen diversiteit zichtbaar te maken. Met geavanceerde optische microscopen kunnen onderzoekers nu fagen labelen met fluorescente kleurstoffen of geconstrueerde lichtgevende eiwitten en hun beweging als heldere stippen volgen. Deze experimenten tonen dat wanneer fagen voor het eerst een bacteriële celoppervlakte tegenkomen, ze zich niet allemaal hetzelfde gedragen: sommige stuiten snel af, andere dwalen over het oppervlak, en een fractie hecht zich stevig vast. De tijd die elk deeltje bevestigd doorbrengt kan over vele seconden variëren, en de beweging van gebonden versus niet‑gebonden deeltjes laat zien dat er meerdere interactiestaten zijn in plaats van één uniforme adsorptiestap.
Virale genomen en barsten cel voor cel volgen
Microscopie is ook gebruikt om het moment te vangen waarop het genetisch materiaal van een faga de cel binnengaat. Door viraal DNA te kleuren hebben wetenschappers het licht zien verplaatsen van de capsid naar de bacterie, en ze vinden dat sommige genomen snel naar binnen stromen terwijl andere pauzeren of minutenlang stagneren voordat de binnenkomst voltooid is. Evenzo kan tijdsverloopmicroscopie van individuele geïnfecteerde cellen precies vastleggen wanneer elke cel barst, waarbij een spreiding van lytische tijden zichtbaar is, zelfs voor genetisch identieke virussen onder dezelfde omstandigheden. Microfluidische apparaten die bacteriën in kleine kanalen vasthouden, gecombineerd met fluorescerende reporters voor fagelementen, stellen onderzoekers nu in staat individuele infecties te volgen vanaf het eerste contact via genoominvoer, virale productie en lysis binnen één en dezelfde cel.
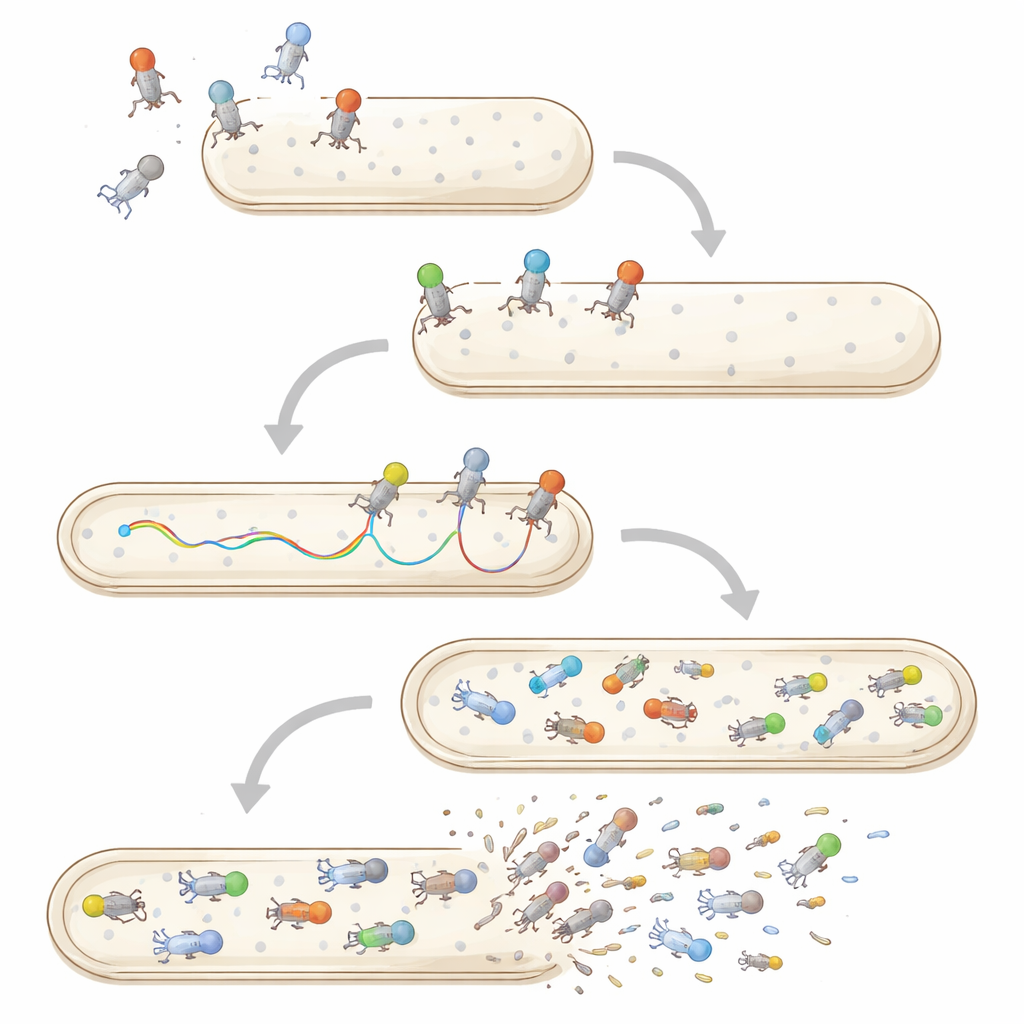
Meervoudige infecties, stabiliteit en leven buiten bacteriën
Enkele‑deeltje en enkele‑celmethoden herzien ook onze opvattingen over co‑infectie en virusoverleving. Wanneer meerdere fagen dezelfde bacterie aanvallen, tonen beeldvorming en flowcytometrie dat hun genomen niet allemaal evenredig binnenkomen of repliceren; sommige worden geblokkeerd of vertraagd, en één lijn kan de nakomelingen domineren. Buiten bacteriën ondervinden individuele fagdeeltjes stress zoals warmte, zuurgraad of aanval door menselijke en dierlijke cellen. Traditionele tests rapporteren alleen hoeveel virussen gemiddeld infectieus blijven na blootstelling, maar nieuwere benaderingen volgen individuele deeltjes die door slijm diffunderen of door zoogdiercellen worden opgenomen, wat duidt op grote verschillen in welke virussen aanhouden of snel worden verwijderd.
Wat dit betekent voor toekomstige geneeskunde en technologie
De auteurs betogen dat het omarmen van deze variatie op individueel niveau cruciaal zal zijn voor zowel fundamentele biologie als fage‑gebaseerde technologieën. Evolutie werkt op verschillen tussen deeltjes, dus begrijpen welke individuele fagen het snelst binden, het betrouwbaarst injecteren, het efficiëntst repliceren of het langst stabiel blijven kan verklaren hoe virale stammen zich aanpassen in oceanen, grond en microbiomen. Diezelfde informatie kan het ontwerp van veiligere, effectievere fagetherapieën en industriële toepassingen sturen — bijvoorbeeld door kortlevende fagen te kiezen voor eenmalige desinfectie of langlevende, zeer stabiele fagen voor het afleveren van nuttige genen aan bacteriën. Door van gemiddelden naar metingen per enkel deeltje te bewegen, kunnen onderzoekers beter beheersen welke virale eigenschappen ze selecteren en produceren, en zo fagen veranderlijker en krachtiger maken als hulpmiddelen.
Bronvermelding: Antani, J.D., Turner, P.E. Rage against the mean: a perspective on measuring fitness of individual phage particles. npj Viruses 4, 21 (2026). https://doi.org/10.1038/s44298-026-00187-4
Trefwoorden: bacteriofagen, enkele-deeltje virologie, fagetherapie, optische microscopie, virale evolutie