Clear Sky Science · sv
Biokompatibilitet, inflammatorisk respons och antibakteriella egenskaper hos enflaskadätare på gingivala fibroblaster och humana pulp stamceller
Varför limmet i din fyllning spelar roll
När du får en tand lagad beror behandlingens framgång inte bara på själva fyllningen utan också på det ”lim” som binder den till tanden. Dessa moderna bindvätskor, ofta kallade universella eller enflaskdsadhesiver, lovar starka, långvariga reparationer och till och med viss skyddseffekt mot kariesframkallande bakterier. Men eftersom de ligger intill tandens levande vävnad och tandköttet måste de vara både skonsamma och hållfasta. Denna studie ställer en enkel men viktig fråga: hur snälla är dessa lim mot våra celler, och hur väl håller de skadliga bakterier borta?
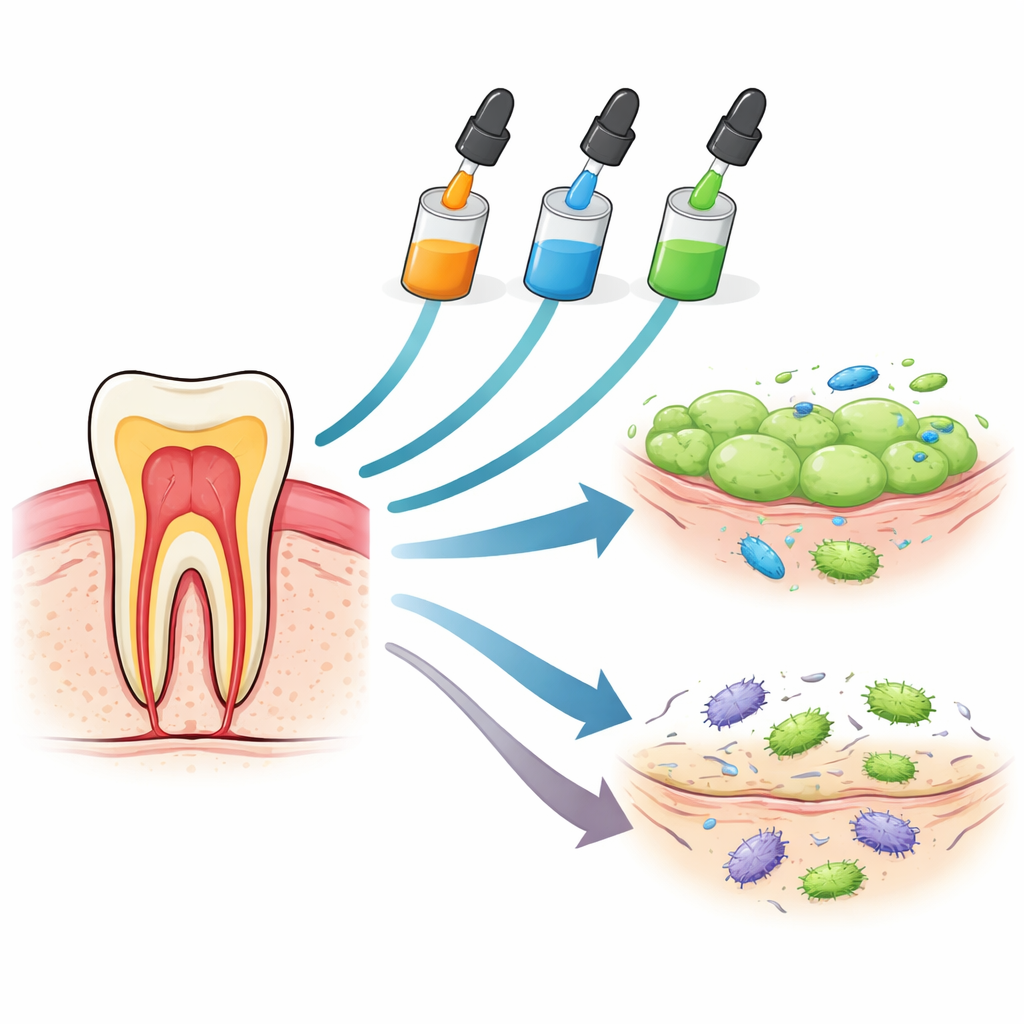
Tre lim under mikroskopet
Forskarna jämförde tre vanliga enflaskade dentala adhesiver: Huge Bond, Single Bond Universal och G-Premio Bond. Alla är utformade för att förenkla tandvårdsarbetet genom att kombinera flera steg i en vätska som kan binda till emalj, dentin och även vissa keramer och metaller. I laboratorium förde teamet dessa material i kontakt med två typer av humana celler som exponeras direkt vid verkliga tandbehandlingar: bindvävsceller från tandköttet (gingivala fibroblaster) och stamceller från den mjuka vävnaden inne i tanden (tandpulpsstamceller). De följde sedan hur många celler som överlevde efter mycket kort kontakt (en minut), efter en timme och efter sex timmar, mätte också kemiska signaler för irritation och testade hur väl adhesiverna kunde hämma tillväxten av vanliga kariesbakterier.
Hur cellerna reagerade över tid
Omedelbart efter kontakt verkade alla tre adhesiverna relativt säkra. Vid en minuters kontakt höll cellöverlevnaden sig nära normal för både gingivala och pulpceller, vilket tyder på att ett kort möte i sig inte är starkt skadligt. Men skillnader framträdde med tiden. Efter en timme visade Huge Bond redan en påtaglig minskning av levande celler, särskilt bland pulpcellerna, medan Single Bond och G-Premio orsakade mildare förändringar. Efter sex timmar var bilden tydligare: både Huge Bond och Single Bond ledde till markant cellförlust i både gum- och pulpceller, medan G-Premio, även om det fortfarande minskade cellantalet, var mindre skadligt totalt sett. Dessa mönster stämmer överens med vad som är känt om byggstenarna i många adhesiver—hartsbeståndsdelar som, om de inte fullständigt härdas med ljus, kan lakas ut och stressa eller döda känsliga celler.
Signaler för irritation och kampen mot bakterier
Cellöverlevnad var bara en del av bilden. Teamet mätte också en viktig larmsignal som celler frigör när de är irriterade eller inflammerade, en molekyl ofta kopplad till tidig vävnadsskada. Efter sex timmars kontakt med adhesiverna producerade både gum- och pulpceller mycket högre nivåer av denna signal, särskilt vid exponering för Huge Bond, därefter Single Bond, medan G-Premio återigen var minst provocerande. Samtidigt visade materialen användbar antibakteriell aktivitet. När de placerades i brunnar på agarmedia inokulerade med Lactobacilli och Streptococcus mutans—två huvudsakliga kariesbildande bakterier—skapade alla tre klara zoner där bakterier inte kunde växa. Huge Bond gav de största bakteriefria zonerna för båda arterna, G-Premio något mindre och Single Bond minst, vilket indikerar att samma sura och reaktiva komponenter som stör humana celler också tillfälligt kan undertrycka skadliga munmikrober.
Vad ingredienserna berättar
Studien kopplar dessa biologiska effekter till innehållet i varje flaska. Adhesiverna innehåller olika blandningar av hartsmolekyler, sura bindningsmedel, lösningsmedel och små fyllnadsämnen. Vissa vanliga hartsingredienser är kända för att vara särskilt problematiska när de förblir oreaktiva, eftersom de kan tränga igenom tandens hårda vävnader och nå levande pulpa eller läcka ut på intilliggande tandkött. Författarna påpekar att metakrylat-typ harts, som ofta används för att skapa starka, hållbara bindningar, är nära kopplade till cellstress, inflammation och till och med programmerad celldöd om härdningen är ofullständig. Samtidigt kan dessa vätskors låga pH och deras funktionella bindningskomponenter temporärt sänka bakteriell aktivitet, vilket förklarar de initiala antibakteriella zonerna som observerades i laboratoriet. G-Premios formulering, som undviker en särskilt mobil harts och förlitar sig på en skräddarsydd blandning av bindningsmolekyler, kan förklara varför den visade det mildaste beteendet gentemot pulpceller samtidigt som den fortfarande gav viss antibakteriell effekt.
Vad detta betyder för ditt tandläkarbesök
För patienter är slutsatsen inte att frukta dentala adhesiver utan att förstå att deras säkerhet beror både på receptet i flaskan och på hur noggrant de används. Under studiens villkor verkade alla tre produkterna relativt säkra när kontakten med levande celler var kort, som vid ett välkontrollerat kliniskt ingrepp. Vid längre exponering orsakade däremot de mer hartsrika formuleringarna mer celldamage och starkare inflammationssignaler, samtidigt som de erbjöd bättre kortsiktig undertryckning av kariesframkallande bakterier. Författarna drar slutsatsen att den säkraste vägen är att välja material med eftertanke och säkerställa att adhesivet härdas noggrant med ljus så att så få reaktiva restprodukter som möjligt kan läcka ut i tanden och tandköttet. Kort sagt, det ”osynliga” lagret som håller din fyllning på plats är en känslig balans mellan styrka, skydd och skonsamhet mot de vävnader som håller din tand vid liv.
Citering: Ibrahim, A.H., Mustafa, S.S., El-Khazragy, N. et al. Biocompatibility, inflammatory response, and antimicrobial properties of single-bottle adhesives on gingival fibroblast and human dental pulp stem cells. Sci Rep 16, 13886 (2026). https://doi.org/10.1038/s41598-026-49388-0
Nyckelord: dentala adhesiver, biokompatibilitet, tandpulpsstamceller, gingivala fibroblaster, antimikrobiell aktivitet