Clear Sky Science · de
Biokompatibilität, Entzündungsreaktion und antimikrobielle Eigenschaften von Einflaschen-Adhäsiven auf Gingivalfibroblasten und menschlichen pulpalen Stammzellen
Warum der Kleber bei Ihrer Füllung wichtig ist
Wenn ein Zahn gefüllt wird, hängt der Erfolg der Behandlung nicht nur von der Füllung selbst ab, sondern auch von dem „Kleber“, der sie am Zahn befestigt. Diese modernen Haftflüssigkeiten, oft als Universal- oder Einflaschen-Adhäsive bezeichnet, versprechen starke, langlebige Reparaturen und sogar einen gewissen Schutz gegen kariesverursachende Keime. Weil sie jedoch direkt neben dem lebenden Zahngewebe und am Zahnfleisch anliegen, müssen sie zugleich schonend und belastbar sein. Die vorliegende Studie stellt eine einfache, aber wichtige Frage: Wie verträglich sind diese Kleber für unsere Zellen und wie gut halten sie schädliche Bakterien fern?
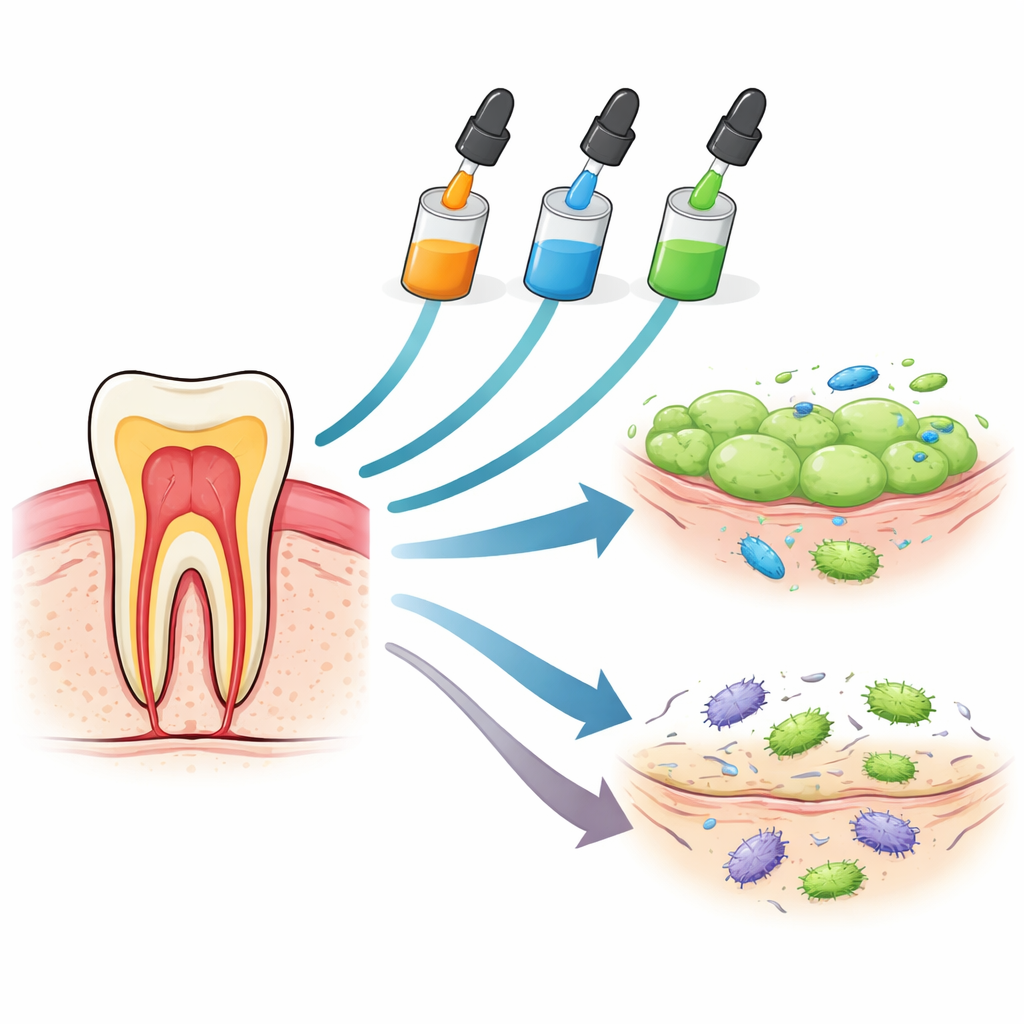
Drei Kleber unter dem Mikroskop
Die Forschenden verglichen drei weitverbreitete Einflaschen-Zahnadhäsive: Huge Bond, Single Bond Universal und G-Premio Bond. Alle drei sind darauf ausgelegt, zahnärztliche Arbeit zu vereinfachen, indem mehrere Schritte in einer Flüssigkeit zusammengefasst werden, die an Schmelz, Dentin und sogar an manchen Keramiken und Metallen haftet. Im Labor brachten die Wissenschaftler diese Materialien mit zwei Arten menschlicher Zellen in Kontakt, die bei realen zahnärztlichen Eingriffen direkt exponiert sind: Bindegewebszellen des Zahnfleischs (Gingivalfibroblasten) und Stammzellen aus dem weichen Gewebe im Zahninneren (pulporale Stammzellen). Sie verfolgten dann, wie viele Zellen nach sehr kurzer Kontaktzeit (eine Minute), nach einer Stunde und nach sechs Stunden überlebten, maßen chemische Signale von Reizung und prüften, wie gut die Adhäsive das Wachstum häufiger kariesverursachender Bakterien hemmen konnten.
Wie die Zellen im Zeitverlauf reagierten
Direkt nach dem Kontakt wirkten alle drei Adhäsive relativ unproblematisch. Nach einer Minute blieb das Zellüberleben sowohl bei Gingival- als auch bei Pulpa-Zellen nahe dem Normalwert, was darauf hindeutet, dass eine kurze Exposition allein nicht stark schädlich ist. Doch im Verlauf der Zeit zeigten sich Unterschiede. Nach einer Stunde zeigte Huge Bond bereits einen deutlichen Rückgang lebensfähiger Zellen, insbesondere bei den Pulpa-Zellen, während Single Bond und G‑Premio mildere Veränderungen bewirkten. Nach sechs Stunden war das Bild klarer: Sowohl Huge Bond als auch Single Bond führten zu ausgeprägtem Zelltod bei Gingiva- und Pulpa-Zellen; G‑Premio verringerte die Zellzahlen ebenfalls, war insgesamt aber weniger schädlich. Diese Muster stimmen mit dem überein, was über die Bausteine vieler Adhäsive bekannt ist — Harzkomponenten, die, wenn sie nicht vollständig durch Lichtpolymerisation ausgehärtet werden, auslaugen und empfindliche Zellen stressen oder abtöten können.
Reizsignale und der Kampf gegen Keime
Das Zellüberleben war nur ein Teil der Geschichte. Das Team maß zudem ein wichtiges Warnsignal, das Zellen bei Reizung oder Entzündung ausschütten — ein Molekül, das oft mit frühem Gewebeschaden verknüpft ist. Nach sechs Stunden Kontakt mit den Adhäsiven produzierten sowohl Gingiva- als auch Pulpa-Zellen deutlich höhere Mengen dieses Signals, besonders nach Exposition gegenüber Huge Bond, gefolgt von Single Bond; G‑Premio war wiederum am wenigsten provozierend. Gleichzeitig zeigten die Materialien nützliche antibakterielle Eigenschaften. Auf Agarplatten mit Lactobacillen und Streptococcus mutans — zwei Hauptakteuren der Kariesentstehung — erzeugten alle drei Adhäsive klare Hemmhöfe, in denen Bakterien nicht wuchsen. Huge Bond bildete die größten bakterienfreien Zonen für beide Arten, G‑Premio etwas kleinere und Single Bond die kleinsten. Das deutet darauf hin, dass dieselben sauren und reaktiven Komponenten, die menschlichen Zellen zusetzen, auch kurzfristig schädliche orale Mikroben unterdrücken können.
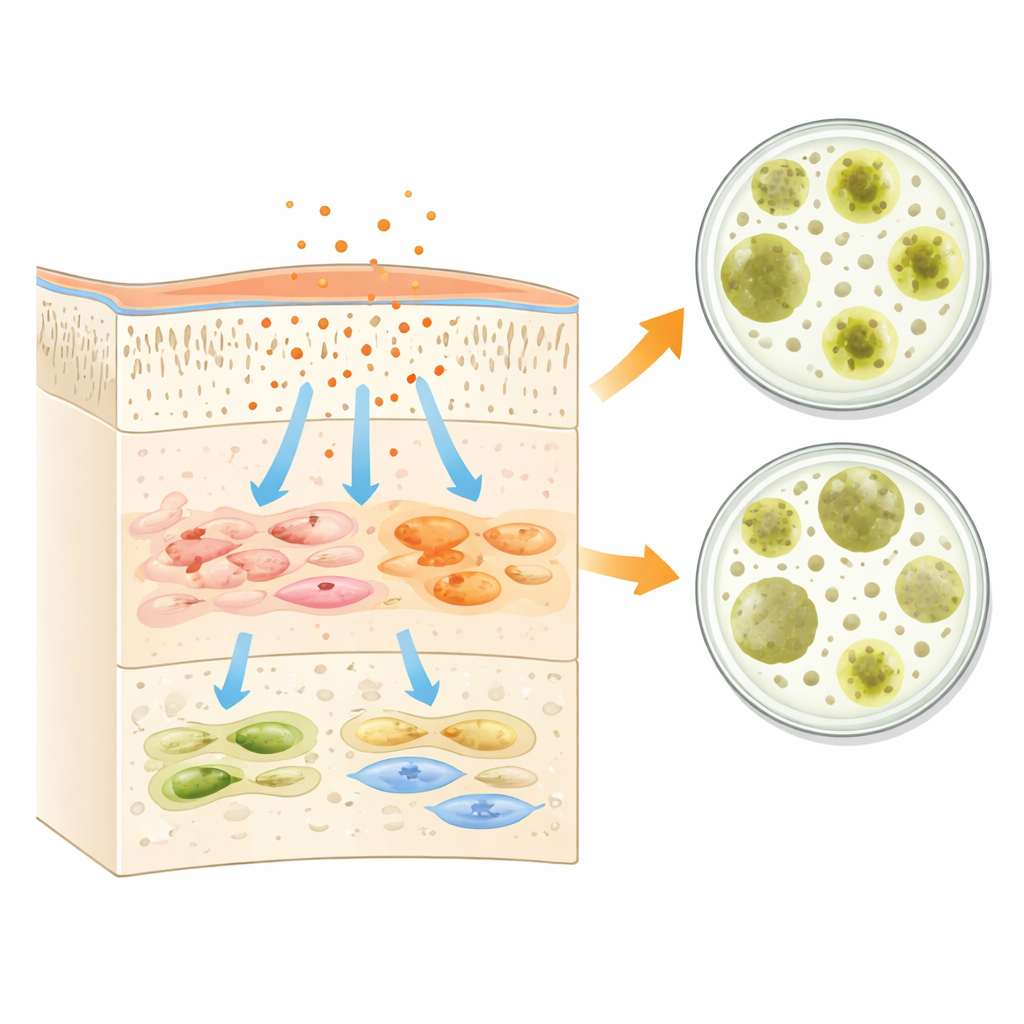
Was die Inhaltsstoffe verraten
Die Studie verbindet diese biologischen Effekte mit der Zusammensetzung der einzelnen Produkte. Die Adhäsive enthalten unterschiedliche Mischungen aus Harzmonomeren, sauren Haftmitteln, Lösungsmitteln und feinen Füllstoffen. Einige verbreitete Harzbestandteile sind besonders problematisch, wenn sie unverbraucht verbleiben, da sie durch harte Zahnhartsubstanzen hindurchtreten und das lebende Pulpagewebe erreichen oder auf benachbartes Zahnfleisch auslaufen können. Die Autorinnen und Autoren weisen darauf hin, dass Methacrylat‑artige Harze, die häufig für feste, dauerhafte Verbindungen verwendet werden, eng mit Zellstress, Entzündung und sogar programmierter Zellteilung verbunden sind, wenn die Aushärtung unvollständig ist. Gleichzeitig kann der niedrige pH‑Wert dieser Flüssigkeiten und ihre funktionellen Haftkomponenten die bakterielle Aktivität vorübergehend verringern, was die anfänglichen antibakteriellen Zonen im Labor erklärt. Die Formulierung von G‑Premio, die auf ein besonders mobileres Harz verzichtet und stattdessen auf eine gezielte Mischung von Haftmolekülen setzt, könnte erklären, warum es gegenüber Pulpa‑Zellen am schonendsten war und dennoch einen gewissen antibakteriellen Effekt aufwies.
Was das für Ihren Zahnarztbesuch bedeutet
Für Patientinnen und Patienten lautet die wichtigste Botschaft nicht, vor Zahnadhäsiven Angst zu haben, sondern zu verstehen, dass ihre Sicherheit sowohl von der Rezeptur in der Flasche als auch von der sorgfältigen Anwendung abhängt. Unter den Bedingungen der Studie erschienen alle drei Produkte relativ sicher, wenn der Kontakt mit lebenden Zellen kurz war, wie bei einem gut kontrollierten klinischen Eingriff. Bei längerer Exposition jedoch führten die harzreicheren Formulierungen zu mehr Zellschäden und stärkeren Entzündungssignalen, selbst wenn sie gleichzeitig eine bessere kurzfristige Unterdrückung kariesverursachender Bakterien bewirkten. Die Autorinnen und Autoren schließen daraus, dass der sicherste Weg darin besteht, Materialien bedacht auszuwählen und sicherzustellen, dass das Adhäsiv gründlich lichtgehärtet wird, damit möglichst wenige reaktive Rückstände in Zahn und Zahnfleisch gelangen. Kurz gesagt: Die „unsichtbare“ Schicht, die Ihre Füllung hält, ist ein sensibles Gleichgewicht zwischen Festigkeit, Schutz und Schonung des Gewebes, das Ihren Zahn lebendig erhält.
Zitation: Ibrahim, A.H., Mustafa, S.S., El-Khazragy, N. et al. Biocompatibility, inflammatory response, and antimicrobial properties of single-bottle adhesives on gingival fibroblast and human dental pulp stem cells. Sci Rep 16, 13886 (2026). https://doi.org/10.1038/s41598-026-49388-0
Schlüsselwörter: Zahnadhäsive, Biokompatibilität, Stammzellen der Pulpa, Gingivalfibroblasten, antimikrobielle Aktivität