Clear Sky Science · it
Biocompatibilità, risposta infiammatoria e proprietà antimicrobiche degli adesivi monocomponente su fibroblasti gengivali e cellule staminali della polpa dentale umana
Perché conta il collante della tua otturazione
Quando ti viene fatta un’otturazione, il successo del trattamento dipende non solo dall’otturazione stessa, ma anche dal “collante” che la lega al dente. Questi moderni liquidi adesivi, chiamati adesivi universali o monocomponente, promettono riparazioni solide e durature e perfino una certa protezione contro i germi che causano carie. Ma poiché stanno a contatto diretto con i tessuti vivi del dente e con le gengive, devono essere al tempo stesso delicati e resistenti. Questo studio pone una domanda semplice ma importante: quanto sono compatibili con le nostre cellule questi collanti e quanto efficacemente ostacolano i batteri nocivi?
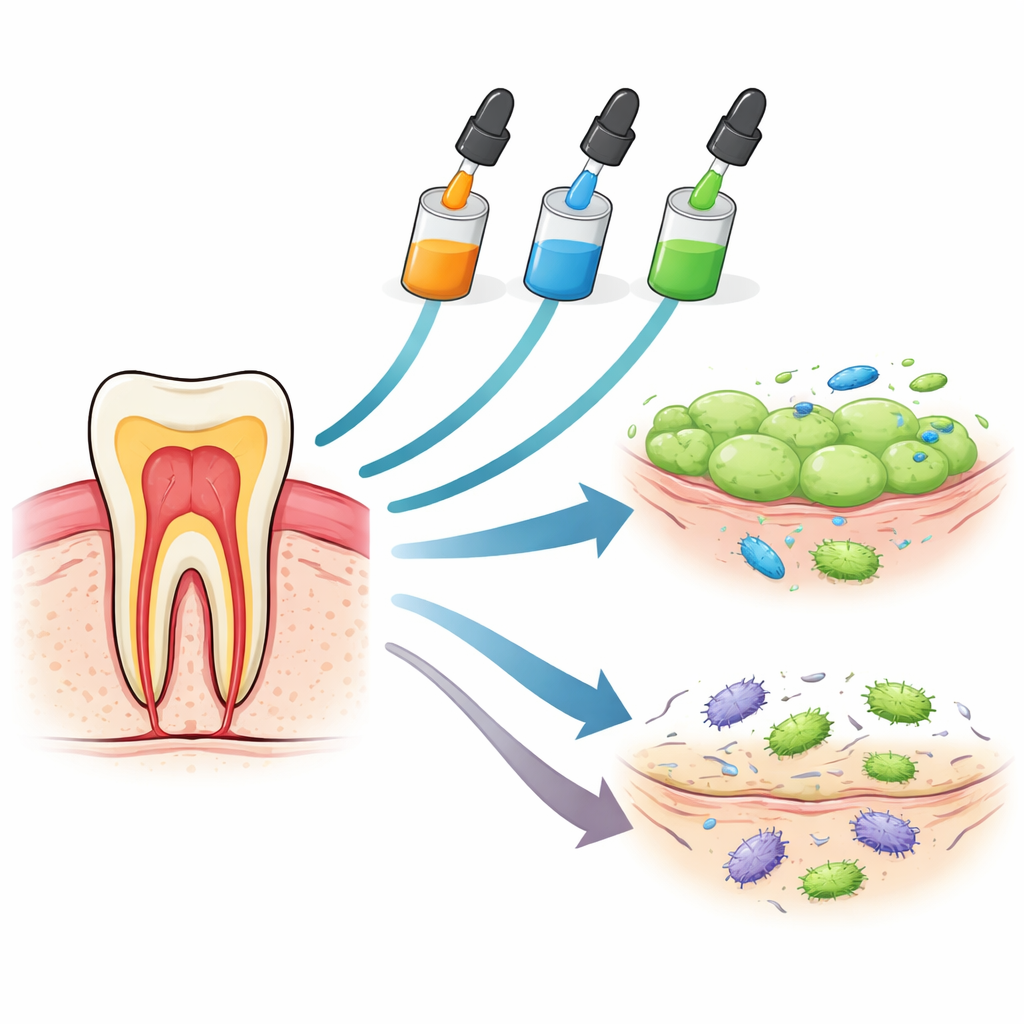
Tre adesivi sotto il microscopio
I ricercatori hanno confrontato tre adesivi dentali monocomponente di uso diffuso: Huge Bond, Single Bond Universal e G-Premio Bond. Tutti sono ideati per semplificare il lavoro odontoiatrico combinando più passaggi in un unico liquido in grado di legarsi a smalto, dentina e anche ad alcune ceramiche e metalli. In laboratorio il gruppo ha messo questi materiali a contatto con due tipi di cellule umane esposte direttamente durante i trattamenti dentali reali: le cellule connettivali gengivali (fibroblasti gengivali) e le cellule staminali provenienti dal tessuto molle interno al dente (cellule staminali della polpa dentale). Hanno quindi seguito la sopravvivenza cellulare dopo un contatto molto breve (un minuto), dopo un’ora e dopo sei ore, hanno misurato segnali chimici di irritazione e hanno testato quanto gli adesivi riuscissero a fermare la crescita dei batteri comuni responsabili di carie.
Come le cellule hanno reagito nel tempo
Subito dopo il contatto, tutti e tre gli adesivi sono risultati relativamente sicuri. Al minuto uno la sopravvivenza cellulare è rimasta vicina alla norma sia per le cellule gengivali sia per quelle della polpa, suggerendo che un incontro breve da solo non è fortemente dannoso. Ma con il passare del tempo sono emerse differenze. Dopo un’ora Huge Bond ha mostrato già un calo evidente delle cellule vive, soprattutto tra quelle della polpa, mentre Single Bond e G-Premio hanno causato variazioni più lievi. Dopo sei ore il quadro è stato più chiaro: sia Huge Bond sia Single Bond hanno determinato una perdita marcata di cellule in entrambi i tipi, mentre G-Premio, pur riducendo il numero di cellule, è risultato complessivamente meno dannoso. Questi modelli corrispondono a quanto noto sui componenti costitutivi di molti adesivi: parti resinose che, se non completamente indurite mediante polimerizzazione luminosa, possono fuoriuscire e stressare o uccidere cellule sensibili.
Segnali di irritazione e lotta contro i germi
La sopravvivenza cellulare è stata solo una parte della storia. Il gruppo ha misurato anche un importante segnale d’allarme che le cellule rilasciano quando sono irritate o infiammate, una molecola spesso collegata a danni tissutali precoci. Dopo sei ore di contatto con gli adesivi, sia le cellule gengivali sia quelle della polpa hanno prodotto livelli molto più elevati di questo segnale, soprattutto in presenza di Huge Bond, seguito da Single Bond, con G-Premio ancora il meno provocatorio. Contemporaneamente, i materiali hanno mostrato un comportamento antibatterico utile. Quando posti in pozzetti su piastre di agar inoculate con Lactobacilli e Streptococcus mutans — due principali batteri responsabili della carie — tutti e tre hanno creato zone chiare in cui i batteri non potevano crescere. Huge Bond ha prodotto le zone prive di batteri più ampie per entrambe le specie, G-Premio un poco più piccole e Single Bond le più ridotte, segnalando che gli stessi componenti acidi e reattivi che disturbano le cellule umane possono anche sopprimere temporaneamente i microrganismi orali dannosi.
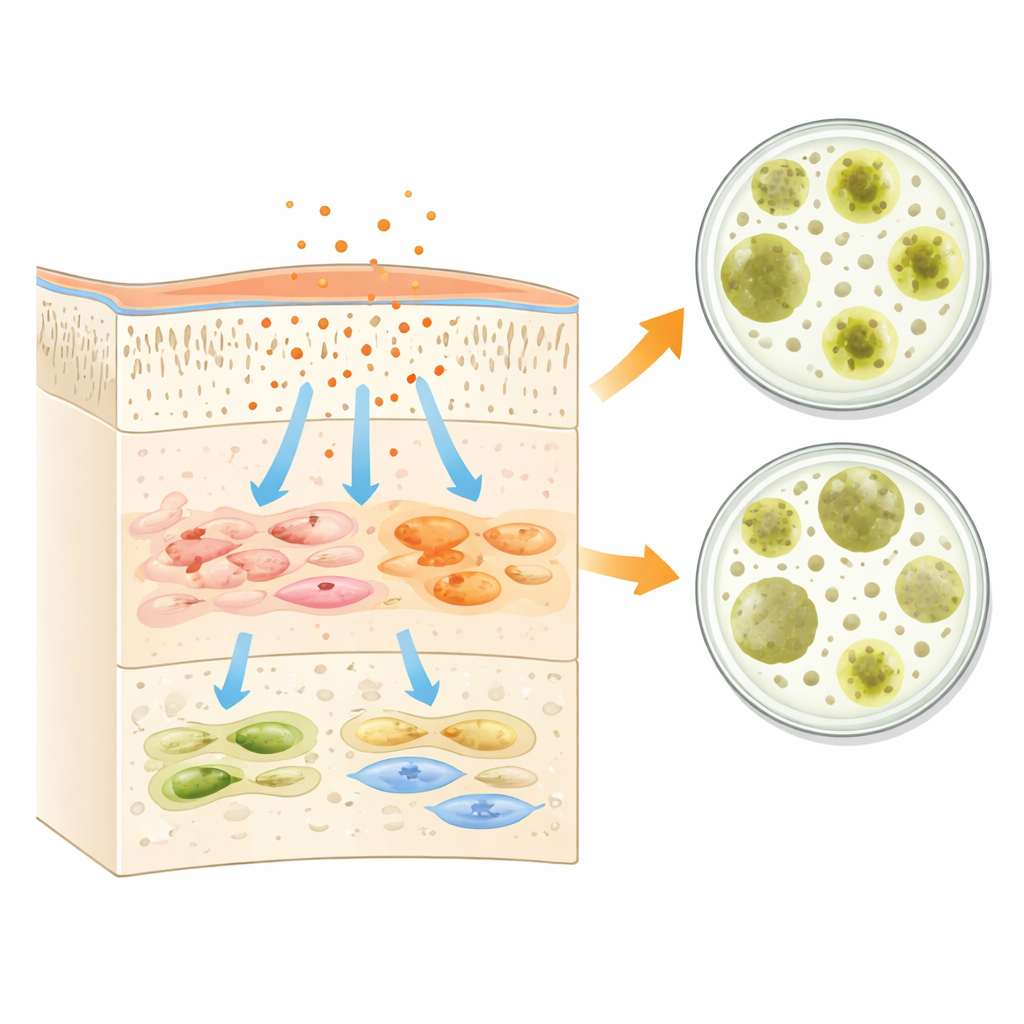
Cosa ci dicono gli ingredienti
Lo studio collega questi effetti biologici a ciò che è contenuto in ciascuna confezione. Gli adesivi contengono diverse miscele di molecole resinose, agenti acidi di legame, solventi e microcariche. Alcuni componenti resinosi comuni sono noti per essere particolarmente problematici quando restano non reagiti, poiché possono penetrare attraverso i tessuti duri del dente e raggiungere la polpa vitale o fuoriuscire sulle gengive vicine. Gli autori sottolineano che le resine di tipo metacrilato, ampiamente impiegate per creare legami forti e duraturi, sono strettamente associate a stress cellulare, infiammazione e persino morte cellulare programmata se la polimerizzazione è incompleta. Allo stesso tempo, il basso pH di questi liquidi e i loro componenti funzionali di legame possono ridurre temporaneamente l’attività batterica, spiegando le zone antibatteriche iniziali osservate in laboratorio. La formulazione di G-Premio, che evita una particolare resina particolarmente mobile e si basa su una miscela mirata di molecole leganti, può spiegare perché ha mostrato il comportamento più gentile verso le cellule della polpa pur mantenendo un certo effetto antibatterico.
Cosa significa per la tua visita dal dentista
Per i pazienti il messaggio non è temere gli adesivi dentali, ma comprendere che la loro sicurezza dipende sia dalla ricetta nella bottiglia sia dall’accuratezza dell’applicazione. Nelle condizioni dello studio, tutti e tre i prodotti sono risultati ragionevolmente sicuri quando il contatto con le cellule vive è stato breve, come in una procedura clinica ben controllata. Tuttavia, a esposizioni più prolungate le formulazioni più ricche di resina hanno causato maggior danno cellulare e segnali infiammatori più forti, pur offrendo una migliore soppressione a breve termine dei batteri che provocano carie. Gli autori concludono che la via più sicura è scegliere i materiali con attenzione e assicurarsi che l’adesivo venga polimerizzato con la luce in modo completo, affinché il minor numero possibile di residui reattivi possa fuoriuscire nel dente e nelle gengive. In breve, lo “strato invisibile” che tiene ferma l’otturazione è un equilibrio delicato tra resistenza, protezione e compatibilità con i tessuti che mantengono vivo il dente.
Citazione: Ibrahim, A.H., Mustafa, S.S., El-Khazragy, N. et al. Biocompatibility, inflammatory response, and antimicrobial properties of single-bottle adhesives on gingival fibroblast and human dental pulp stem cells. Sci Rep 16, 13886 (2026). https://doi.org/10.1038/s41598-026-49388-0
Parole chiave: adesivi dentali, biocompatibilità, cellule staminali della polpa dentale, fibroblasti gengivali, attività antimicrobica