Clear Sky Science · fr
Biocompatibilité, réponse inflammatoire et propriétés antimicrobiennes des adhésifs monocomposants sur des fibroblastes gingivaux et des cellules souches pulpaires humaines
Pourquoi l’adhésif de votre obturation compte
Lorsque l’on réalise une obturation, le succès du traitement dépend non seulement du matériau de restauration, mais aussi de « la colle » qui le fixe à la dent. Ces liquides d’adhésion modernes, dits universels ou monocomposants, promettent des réparations solides et durables et apportent parfois une protection contre les germes responsables de caries. Mais parce qu’ils se placent au contact immédiat des tissus vivants de la dent et des gencives, ils doivent être à la fois efficaces et bien tolérés. Cette étude pose une question simple mais essentielle : ces adhésifs sont-ils compatibles avec nos cellules, et dans quelle mesure freinent-ils les bactéries nuisibles ?
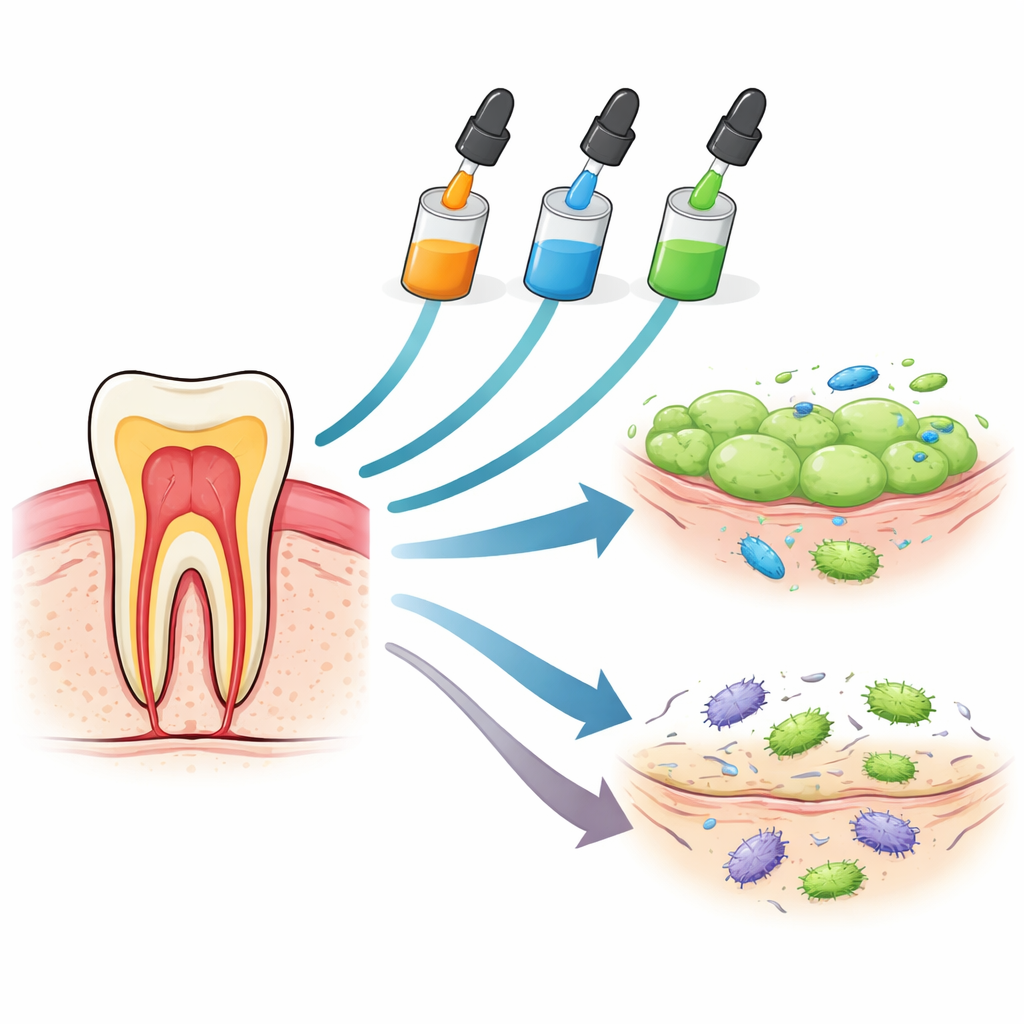
Trois adhésifs passés au microscope
Les chercheurs ont comparé trois adhésifs dentaires monocomposants largement utilisés : Huge Bond, Single Bond Universal et G-Premio Bond. Tous visent à simplifier les gestes cliniques en regroupant plusieurs étapes dans un seul liquide capable d’adhérer à l’émail, à la dentine et parfois à certains céramiques et métaux. En laboratoire, l’équipe a mis ces matériaux en contact avec deux types de cellules humaines exposées lors de traitements dentaires réels : les cellules du tissu conjonctif gingival (fibroblastes gingivaux) et les cellules souches issues du tissu mou de l’intérieur de la dent (cellules souches pulpaires). Ils ont ensuite suivi la survie cellulaire après un contact très court (une minute), après une heure et après six heures, mesuré des signaux chimiques d’irritation et testé la capacité des adhésifs à inhiber la croissance de bactéries courantes responsables de caries.
Réactions cellulaires au fil du temps
Juste après le contact, les trois adhésifs semblaient relativement sûrs. À la minute, la survie cellulaire restait proche de la normale pour les cellules gingivales et pulpaires, suggérant qu’une exposition brève n’est pas fortement délétère. Mais des différences sont apparues avec le temps. Après une heure, Huge Bond montrait déjà une baisse notable du nombre de cellules vivantes, en particulier parmi les cellules pulpaires, tandis que Single Bond et G-Premio entraînaient des altérations plus modérées. Au bout de six heures, le bilan était plus net : Huge Bond et Single Bond provoquaient une perte cellulaire marquée tant chez les fibroblastes gingivaux que chez les cellules pulpaires, et G-Premio, bien qu’ayant aussi réduit les effectifs cellulaires, était globalement moins nocif. Ces tendances correspondent à ce que l’on sait des constituants de nombreux adhésifs : des composants résineux qui, s’ils ne sont pas complètement polymérisés par photopolymérisation, peuvent migrer et stresser ou tuer des cellules sensibles.
Signaux d’irritation et lutte contre les microbes
La survie cellulaire n’était qu’une partie de l’histoire. L’équipe a aussi mesuré un signal d’alarme clé libéré par les cellules en cas d’irritation ou d’inflammation, une molécule souvent liée aux dommages tissulaires précoces. Après six heures de contact avec les adhésifs, les cellules gingivales et pulpaires produisaient des niveaux beaucoup plus élevés de ce marqueur d’alerte, surtout exposées à Huge Bond, puis à Single Bond, G-Premio étant de nouveau le moins provocateur. Parallèlement, les matériaux présentaient un comportement antibactérien utile. Lorsqu’ils furent déposés dans des puits sur des boîtes de gélose ensemencées de Lactobacilles et de Streptococcus mutans — deux bactéries majeures impliquées dans la formation des caries —, les trois adhésifs ont créé des zones d’inhibition claires où la croissance bactérienne était empêchée. Huge Bond a généré les plus larges zones d’absence de bactéries pour les deux espèces, G-Premio des zones un peu plus petites, et Single Bond les plus réduites, ce qui indique que les mêmes composants acides et réactifs qui perturbent les cellules humaines peuvent aussi, temporairement, supprimer l’activité de microbes buccaux nuisibles.
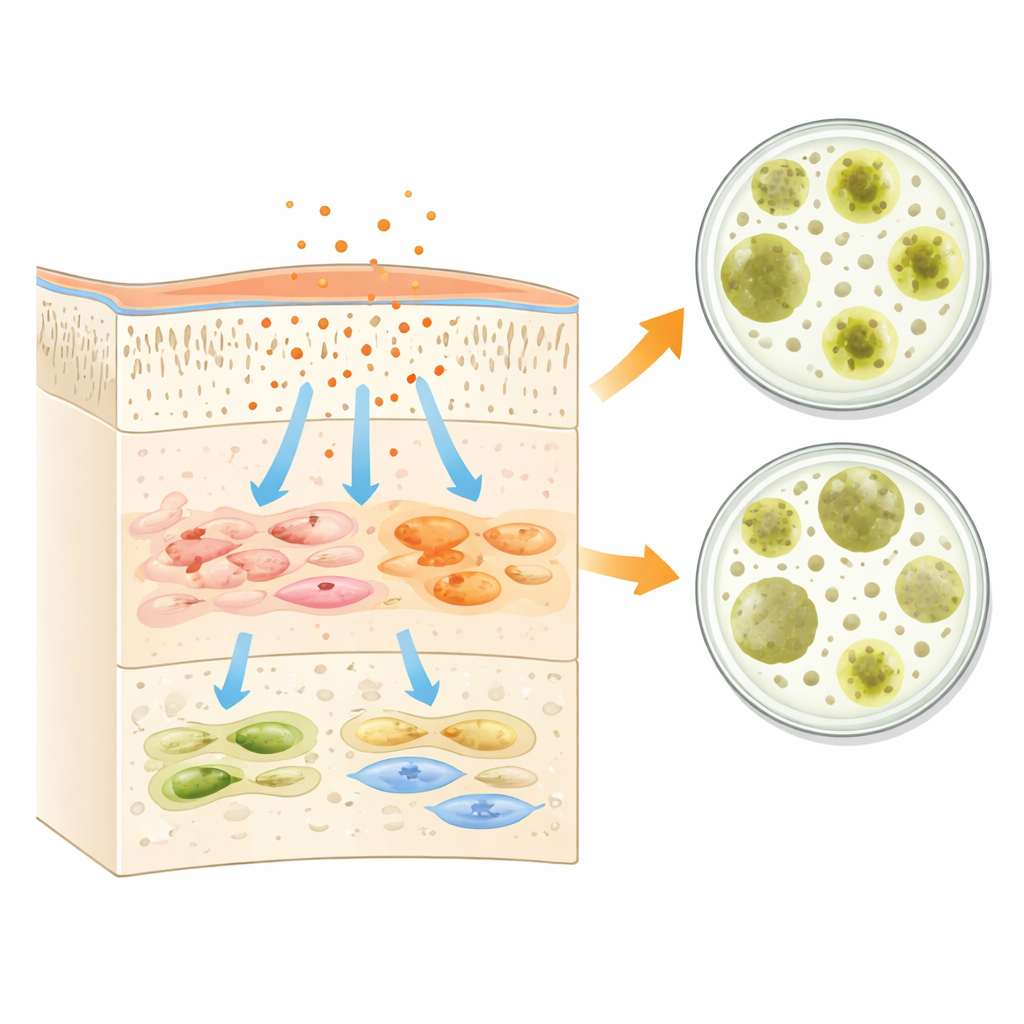
Ce que disent les ingrédients
L’étude relie ces effets biologiques à la composition de chaque flacon. Les adhésifs contiennent des mélanges variables de monomères résineux, d’agents acidifiants, de solvants et de microcharges. Certains monomères résineux courants sont connus pour poser problème lorsqu’ils restent non réticulés, car ils peuvent traverser les tissus minéralisés de la dent et atteindre la pulpe vivante ou suinter sur les gencives voisines. Les auteurs soulignent que les résines de type méthacrylate, largement utilisées pour obtenir des liaisons fortes et durables, sont étroitement associées au stress cellulaire, à l’inflammation et même à la mort cellulaire programmée si la polymérisation est incomplète. En parallèle, le faible pH de ces liquides et leurs composants fonctionnels d’adhésion peuvent temporairement réduire l’activité bactérienne, expliquant les zones antibactériennes observées en laboratoire. La formulation de G-Premio, qui évite un monomère particulièrement mobile et s’appuie sur un mélange ciblé de molécules d’adhésion, pourrait expliquer pourquoi il s’est montré plus doux pour les cellules pulpaires tout en conservant un effet antibactérien partiel.
Ce que cela signifie pour votre intervention dentaire
Pour les patients, la conclusion n’est pas de craindre les adhésifs dentaires, mais de comprendre que leur sécurité dépend autant de la formule du produit que de la manière dont il est employé. Dans les conditions de l’étude, les trois produits paraissaient raisonnablement sûrs en cas de contact bref, comme lors d’une procédure clinique bien contrôlée. En revanche, pour des expositions plus longues, les formulations plus riches en résine provoquaient davantage de dommages cellulaires et des signaux d’inflammation plus prononcés, tout en offrant une suppression à court terme plus efficace des bactéries cariogènes. Les auteurs concluent que la stratégie la plus sûre est de choisir les matériaux avec discernement et de s’assurer d’une photopolymérisation complète de l’adhésif afin que le moins d’éléments réactifs possibles puisse s’échapper vers la dent et les gencives. En bref, la couche « invisible » qui maintient votre obturation en place résulte d’un équilibre délicat entre résistance, protection et tolérance pour les tissus qui assurent la vitalité de la dent.
Citation: Ibrahim, A.H., Mustafa, S.S., El-Khazragy, N. et al. Biocompatibility, inflammatory response, and antimicrobial properties of single-bottle adhesives on gingival fibroblast and human dental pulp stem cells. Sci Rep 16, 13886 (2026). https://doi.org/10.1038/s41598-026-49388-0
Mots-clés: adhésifs dentaires, biocompatibilité, cellules souches de la pulpe dentaire, fibroblastes gingivaux, activité antimicrobienne